由于抗生素长期不合理的使用,导致养殖场环境中耐药菌株不断出现.耐药细菌的产生严重影响了感染性疾病的治疗效果,增加了养殖场细菌感染发生率以及治疗成本[1-2].消毒剂的用途与抗生素不同,例如临床上常用的苯扎溴铵、氯己定等季铵盐类阳离子表面活性剂和双胍类化合物等消毒剂,多用于皮肤黏膜的防腐和表面消毒,在预防和控制致病菌传播或感染等方面起到关键作用.此外,消毒剂对细菌的作用机制与抗生素也不同,消毒剂可同时作用于细菌多个靶位点,如细菌细胞壁和细胞膜,使渗透性增加,内容物漏出,干扰氧化磷酸化过程,抑制膜酶活性等.同时,它还可以作用于细胞内成分,与生物大分子(蛋白质、DNA、RNA)发生交联、与巯基交互作用以及烷基化作用等,使蛋白质变性、抑制酶的活性、破坏DNA等,因此消毒剂可表现出更宽的抗菌活性[3].近年来,消毒剂在我国家畜、家禽、水产和食用真菌的养殖业中的使用越来越多,常用的消毒剂包括季胺盐类化合物、酚类化合物、双胍类、碘及其复合物、醛类、过氧化物和银化合物.然而,越来越多的研究结果表明,同滥用抗生素的后果一样,消毒剂使用的增加同样也会导致细菌对其产生耐药[4-5].细菌对消毒剂耐药是指对常用浓度消毒剂不再敏感的菌株出现,一般认为,当消毒剂对细菌的最小抑菌浓度(Minimal inhibitory concentration,MIC)超过一定值,就认为产生了耐药[3].
目前,7种质粒介导的季铵盐类消毒剂(Quaternary ammonium compounds,QACs)特异抗性基因在大肠埃希菌Escherichia coli中被发现,包括qacE、qacEΔ1、qacF、qacG、qacH、qacI和sugE(p)(质粒型sugE).这些基因编码小蛋白家族多药外排泵(Small multiple resistance,SMR),赋予细菌对QACs的抗药性[5],SMR家族基因可由质粒或整合子介导传播,对QACs的MIC较高的菌株通常是由于其获得了携带这些消毒剂抗性基因的可移动元件,如质粒、Ⅰ型整合子等[6].研究表明,qacI、sugE(p)基因可共存于多重耐药(Multidrug resistance,MDR)质粒,如IncA /C和IncHI2型质粒中[7-8],其可介导对消毒剂高水平耐药,并在大肠埃希菌中广泛传播.另有5种染色体编码基因sugE(c)(染色体型sugE)、emrE、ydgE/ydgF和mdfA等也特异地介导对QACs的抗药性,并可在大肠埃希菌中垂直传播[9].相对革兰阳性细菌,革兰阴性细菌对消毒剂表现出更强的抗药性[10],如大肠埃希菌对苯扎氯铵(Benzalkonium chloride,BC)的MIC为50 mg·L-1,而葡萄球菌对BC的MIC只有0.5 mg·L-1 [11];假单胞菌Pseudomonas sp.对BC的MIC达到了200 mg·L-1,而葡萄球菌对BC的MIC只有4 ~ 11 mg·L-1 [12].尽管国内已经开展了一些对动物源大肠埃希菌中消毒剂抗药性的调查[10, 13],但是极少针对整个养殖场生态环境,包括动物-环境-人源大肠埃希菌中消毒剂抗药性的研究,而且消毒剂的抗药性是否与抗菌药的耐药性相关还不得而知.本研究通过分离不同阶段的猪粪便、猪场周边环境样品和猪场工作人员粪便中大肠埃希菌,研究大肠埃希菌对常用消毒剂和抗菌药耐药情况,同时检测消毒剂抗性基因,分析其与抗菌药耐药表型相关性,为消毒剂的规范合理使用提供科学依据.
1 材料与方法 1.1 培养基及试剂TSA培养基,麦康凯培养基,伊红美蓝培养基(EMB),MH培养基和MHA培养基,均为杭州微生物试剂有限公司产品.
DNA Marker DL500、dNTP和rTaqDNA聚合酶等为TaKaRa有限公司产品.消毒剂苯扎氯铵、十六烷基三甲基溴化铵(Cetyltrimethy ammonium bro- mide,CTAB),三氯生(Triclosan,TCS)和氯己定(Chlorhexidine,CL)等均为普博欣试剂有限公司产品.
1.2 引物的合成消毒剂抗药性基因的10对引物是依据GenBank公布的相关序列设计,由华大基因有限公司合成,如表 1所示.
|
|
表 1 PCR引物序列及条件 Table 1 Primers and PCR conditions used |
从广东省某猪场采集了130份样品,94份来自不同养殖阶段猪的粪便,其中包括哺乳仔猪20份,保育猪20份,育肥猪20份,后备母猪14份,怀孕母猪20份;14份空气样品;8份猪场周边的水样品;7份猪场周边土壤样品;7份猪场人员粪便样品.各类样品采集方法如下:用无菌袋采集猪和猪场人员粪便;在猪场的生产区,包括哺乳仔猪区、保育区、育肥区和备怀母猪区等的通风口放置TSA培养基,放置培养24 h后取回作为空气样品;结合猪场粪便收集、排放路线采集土壤和水样品(冲栏水收集于化粪池,化粪池水通过沟渠排入鱼塘,鱼塘水连接到周围的河道,同时河道里的水被用来浇灌周围蔬菜),即水样从冲栏水、化粪池水、沟渠水、鱼塘水和河道水处收集,每处各取1 L;土壤样本收集每个鱼塘、河道的地泥或蔬菜地土壤,每个采样点收集不同方位3份样品混合,每个采样点各取200 g.所有样品用无菌袋封好后放置于带冰袋的有盖的泡沫箱中,密封好泡沫箱后运回实验室,- 20 ℃条件保存,96 h内处理.
1.3.2 样品处理和菌株的分离鉴定对于水样品,在无菌条件下取20 μL接种于LB肉汤培养基,37 ℃过夜培养;对于土壤和粪便样品,先用无菌生理盐水洗涤稀释后,取20 μL接种于LB肉汤培养基中,37 ℃过夜培养;空气中的TSA培养基,放置培养箱,37 ℃过夜培养.每份样品挑取1个具有大肠埃希菌典型形态的单菌落,接种划线到EMB琼脂平板上37 ℃培养16 ~ 24 h;选择生长良好的紫黑色有金属光泽的菌落通过生化鉴定,纯化后保存于含有体积分数为60%甘油的LB肉汤中,于- 80 ℃条件保存备用.
1.3.3 药敏试验参照CLSI(2013版)指导原则和执行标准[14],采用琼脂二倍稀释法,测定97株大肠埃希菌对4种消毒剂和10种常用抗菌药物的敏感性.测定的消毒剂包括BC、CTAB、TCS和CL,测定的抗生素包括磺胺甲恶唑/甲氧苄啶(SXT)、萘啶酸(NAL)、环丙沙星(CIP)、喹乙醇(OLA)、头孢噻肟(CTX)、头孢西丁(FOX)、阿米卡星(AMK)、多西环素(DOX)、氟苯尼考以及黏菌素(CS),均购自中国药品生物制品检定所.用二倍稀释法把各种药物稀释到所需浓度梯度,分别定量加入高压灭菌过的MH琼脂在平皿中混合均匀,冷却凝固,制成含所需药物浓度的琼脂平板,把稀释至含菌量约为1.0 × 106 CFU·mL-1的菌液用微量多点接种仪接种到MH琼脂平板上,37 ℃倒置培养16 ~ 18 h后观察结果,以完全不见细菌生长的最低药物浓度为该药物对细菌的MIC.10种抗生素MIC试验判断标准则是根据CLSI规定折点值范围判定结果[14].
1.3.4 消毒剂抗性基因检测煮沸法制备模板,无菌接种环刮取大肠埃希菌菌落,置于1.5 mL Eppen- dorf离心管里,加无菌水200 μL,吹打混匀,沸水煮10 min后,迅速冰浴2 ~ 3 min,10 000 r·min-1离心2 min,将上清液置于- 20 ℃条件下储存.PCR扩增体系:rTap酶0.125 μL,dNTP 2.0 μL,10 × buffer 2.5 μL,上、下游引物各0.5 μL,模板2.0 μL,无菌去离子水17.5 μL,总体积25.125 μL.扩增循环条件:94 ℃预变性5 min;95 ℃变性45 s,退火(退火温度如表 1所示)30 s,72 ℃延伸30 s,共进行30个循环;最后72 ℃延伸10 min.扩增产物经15 mg·mL-1琼脂糖凝胶电泳后用凝胶成像系统观察并保存.
1.4 统计分析利用SPSS19.0软件t检验进行数据显著性分析.
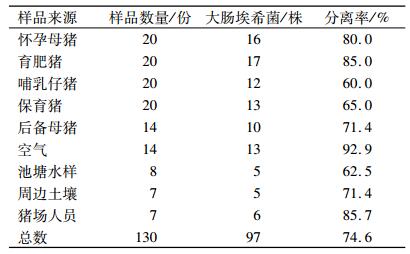
2 结果与分析 2.1 大肠埃希菌分离情况130份样品中共分离鉴定97株大肠埃希菌,分离率达74.6%,详见表 2.不同来源的大肠埃希菌的分离率在60.0% ~ 92.9%范围,可见该猪场及猪场周边环境中大肠埃希菌污染较为严重.
|
|
表 2 大肠埃希菌分离情况 Table 2 Isolation of Escherichia coli |
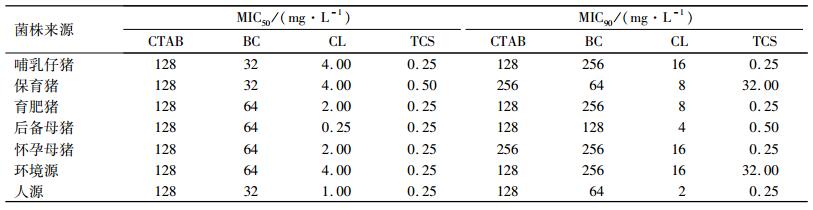
由表 3可看出,不同来源大肠埃希菌对CTAB的MIC50和MIC90均达到128 mg· L-1以上;对BC的MIC50和MIC90分别为32和64 mg·L-1以上;大肠埃希菌对CL和TCS较敏感,MIC50和MIC90分别在0.25 ~ 4.00和0.25 ~ 32.00 mg·L-1之间,环境源大肠埃希菌对CL和TCS的MIC90分别达到16和32 mg·L-1,高于人源大肠埃希菌对应的MIC90.
|
|
表 3 不同来源大肠埃希菌对4种消毒剂的MIC50和MIC90 Table 3 MIC50 and MIC90 of four disinfectants against Escherichia coli isolated from different sources |
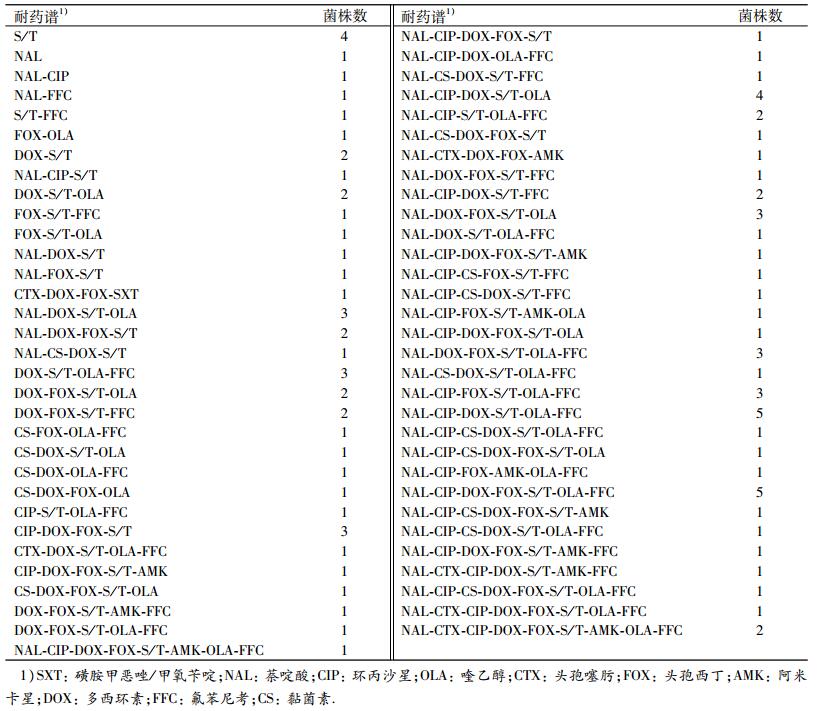
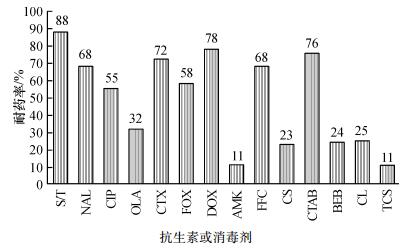
药敏试验结果显示,97株大肠埃希菌对S /T的耐药性最为严重,耐药率达88%;其次是DOX和CTX,耐药率分别为78%和72%;对其他抗生素如NAL、FFC、FOX、CIP和OLA,也有不同程度的耐药.然而,大部分菌株对AMK和CS比较敏感,其耐药率分别为11%和23%(图 1).另外,97株大肠埃希菌对消毒剂CTAB呈现较高的耐药率,为76%,而对另外3种消毒剂BEB,CL和TCS的耐药率相对较低(图 1).97株大肠埃希菌中绝大多数表现为多重耐药(即对3类及3类以上药物耐药),多重耐药率达87.6%.对10种抗菌药物产生了63种耐药谱,其中仅有6株耐1类抗生素,6株耐2类抗生素,85株耐3类及3类以上抗生素(表 4).
|
图 1 97株大肠埃希菌对10种抗生素和4种消毒剂的耐药率 Figure 1 Resistance rates to 10 antibiotics and 4 disinfectants in 97 Escherichia coli isolates |
|
|
表 4 大肠埃希菌对抗生素耐药谱 Table 4 Drug resistance profiles of Escherichia coli isolates |
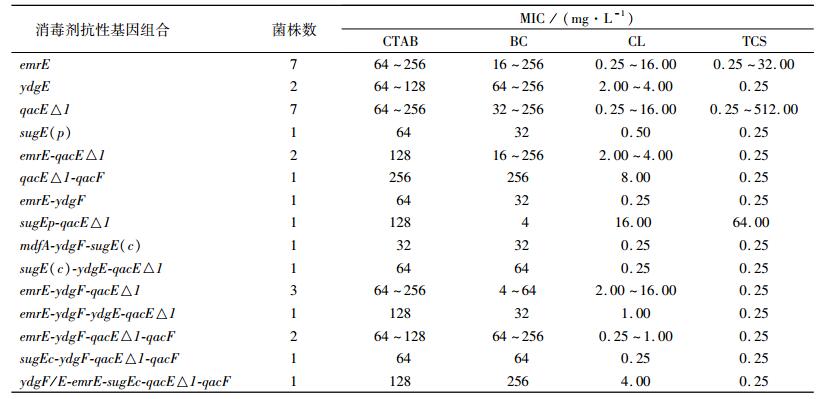
97株大肠埃希菌中,共检出32株大肠埃希菌携带消毒剂抗性基因,检出率为33.0%,其中qacE△1(n = 20,20.6%)和emrE(n = 17,17.5%)基因检出率最高,其次是ydgF(n = 10,10.3%)和qacF(n = 5,5.2%)基因;ydgE(n = 4,4.1%)、sugE(p)(n = 2,2.1%)和mdfA(n = 1,1.0%)等基因检测率最低;qacE和qacG基因没有检测出.根据携带消毒剂抗性基因的个数不同,可将32株携带消毒剂抗性基因大肠埃希菌分为15种不同组合(表 5).
|
|
表 5 大肠埃希菌中消毒剂抗性基因分布 Table 5 Distribution of genes conferring resistances to disinfectant in Escherichia coli isolates |
从菌株来源分析,23 /68(60.5%)株携带消毒剂抗性基因的菌株来自猪粪便样品,其中分离自育肥猪(8 /17,47.1%)和保育猪(6 /13,46.2%)的大肠埃希菌数最多;其次是怀孕母猪(5 /16,31.3%)和后备母猪(3 /10,30.0%);哺乳仔猪最少(1 /12,8.3%). 8 /23(34.8%)株携带消毒剂抗性基因的分离自猪场环境源,其中3 /13(23.1%)株来自空气样品;2 /5(40.0%)株来自土壤样品;3 /5(60.0%)株来自水样品.猪场人员的粪便样品中分离得到1 /6(16.7%)株携带ermE的大肠埃希菌.
2.4 大肠埃希菌对消毒剂抗药性与抗菌药耐药性的关系 2.4.1 消毒剂抗药性表型与抗生素耐药表型的关系通过比较发现,24 /97(24.7%)株大肠埃希菌对季铵盐类消毒剂CTAB和BC表现较高水平的耐受,MIC≥128 mg·L-1(ATCC25922对应的MIC为32和16 mg·L-1).这24株大肠埃希菌不仅表现出对季铵盐类消毒剂耐受,同时对多种抗菌药也表现较高水平的抗药性,如CS耐药率为95.8%;S /T、DOX和FFC耐药率均达到83.3%;喹诺酮类抗生素耐药率为62.5%.该结果表明,大肠埃希菌对季铵盐类消毒剂的抗药性与抗菌药耐药性呈正相关,这与Buffet- Bataillon等[15]的研究结果一致.
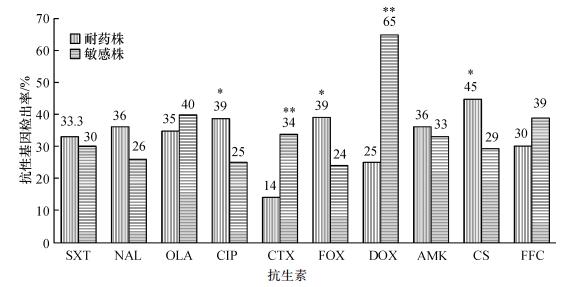
2.4.2 消毒剂抗性基因与抗生素耐药表型的关系大肠埃希菌对季铵盐类消毒剂抗性基因和抗生素的耐药性之间的关系,如图 2所示,在6种抗生素耐药菌株中(SXT、NAL、CIP、FOX、AMK和CS),消毒剂抗性基因检出率分别高于其敏感菌株,而且CIP、FOX和CS耐药菌株分别与其敏感菌株消毒剂抗性基因检出率差异显著(P<0.05).但是,在OLA、CTX、DOX和FFC的耐药菌株的检测率分别低于其敏感菌株消毒剂抗性基因检出率.结果表明,大肠埃希菌消毒剂抗性基因与一些特定的抗生素耐药表型呈正相关,如SXT、NAL、CIP、FOX、AMK以及CS等.
|
图 2 抗生素耐药与消毒剂抗性基因的关系 Figure 2 The relationship between antibiotics resistance and disifectant resistance genes 用t检验法进行分析,抗生素耐药菌株与敏感菌株中消毒剂耐药基因的检测率相比,表示差异极显著(P<0.01),表示差异显著(P<0.05). |
针对养殖场及动物性食品中大肠埃希菌污染的情况已有较多报道[13],这些研究主要是围绕猪体内细菌抗生素的耐药情况,而对猪场及周边环境细菌污染及耐药情况,尤其是消毒剂抗药性的研究很少.本研究中97株大肠埃希菌分离于养殖场中各阶段猪粪便样品、空气样品、池塘水样、周边土壤以及工作人员粪便样品,分离率为74.6%,可见猪场及周边环境中大肠埃希菌污染相当严重.同时,分离于猪粪便样品,周边环境样品(空气、土壤、水样)和猪场人员粪便样品的大肠埃希菌,对QACs消毒剂CTAB和BC均表现较高的MIC,由此我们推测,大肠埃希菌可能是通过以下途径传播的:猪粪便排出后,流入水渠,污染了水源和土壤;水又被用于浇灌农作物,从而导致猪场及周边环境中大肠埃希菌污染严重.结果提示我们,消毒剂的滥用很可能会污染养殖环境,给临床上细菌感染性疾病的治疗带来困难,因此在养殖生产中应规范使用消毒剂,谨防耐药细菌的产生与传播.
通过分析大肠埃希菌对消毒剂的MIC结果及耐药基因检测结果发现,97株大肠埃希菌对季铵盐类消毒剂CTAB和BC的MIC90普遍在128 mg·L-1以上,环境源大肠埃希菌对消毒剂BC和CL的MIC90普遍高于其他来源的大肠埃希菌.例如环境源大肠埃希菌对BC和CL的MIC90分别为256和16 mg·L-1,而保育猪粪源大肠埃希菌对BC和CL的MIC90为64和8 mg·L-1.在32株携带消毒剂抗性基因的大肠埃希菌中,23株(71.8%)来自猪粪便样品,其中分离自育肥猪和保育猪的菌株数最多,猪场环境源大肠埃希菌的消毒剂抗性基因检出率也达到25.0%(8 /32).这可能是由于猪场在使用消毒剂后,残留的部分被排出到环境中,形成一定的消毒剂选择性压力,并最终诱导环境中携带消毒剂抗性基因的细菌富集.令人担忧的是,在人粪源大肠埃希菌中,检测出1株(16.7%)携带ermE基因,这些消毒剂抗性基因可能是通过污染环境或食物传播给人,对人类健康构成威胁[11].
本研究发现,24.7%(24 /97)大肠埃希菌不仅对季铵盐类消毒剂CTAB和BC表现较高水平的耐受,同时对黏菌素、磺胺甲恶唑/甲氧苄啶,多西环素和氟苯尼考耐药率达到83.3% ~ 95.8%,表明大肠埃希菌对季铵盐类消毒剂耐受与抗菌药的抗性之间存在正相关.经统计分析,6种抗生素耐药菌株中(SXT、NAL、CIP、FOX、AMK和CS),消毒剂抗性基因检出率分别高于其敏感菌株,而且CIP、FOX和CS耐药菌株分别与其敏感菌株的消毒剂抗性基因检出率差异显著(P<0.05).可见,大肠埃希菌消毒剂抗性基因与一些抗生素耐药表型存在密切关联,如CIP、FOX、AMK和CS等.这类在消毒剂和抗生素共筛选(Co-selection)压力下存活的细菌,可以称之为“抗生素-消毒剂耐药菌株”.细菌能同时获得消毒剂抗药性和抗生素耐药性,其机制可能是通过交叉耐药(Cross-resistance)实现,即不同的药物对同一靶位作用或使用同一作用途径;一般由单个外排泵介导,同时可以泵出QACs和其他抗菌物质[16],如葡萄球菌中qacC基因可赋予宿主对β-内酰胺药物的抗性[17].第2种机制为共同耐药(Co-resistance),指赋予耐药表型的基因存在于同一个可移动元件上,如质粒、Ⅰ类整合子等.这些移动元件可携带2个或更多的耐药基因,并可以导致更为广泛的水平传播[18].有研究发现,临床分离的多重耐药菌株,如耐甲氧西林金黄色葡萄球菌、铜绿假单胞菌等,其消毒剂抗性基因携带率非常高[19-20].Soumet等[21]研究发现大肠埃希菌长期暴露在QACs亚抑菌浓度下,可导致对抗生素耐药菌株的筛选,给临床治疗带来更大的挑战.本研究中,87%大肠埃希菌为多重耐药菌株,对消毒剂同样表现较高的抗药性,与之前的报道一致.这类抗生素-消毒剂联合耐药菌株对抗生素或消毒剂的使用不再有效,一旦感染动物或污染环境甚至传播给人类,则可能引起公共卫生安全问题,因此合理使用抗生素和消毒剂十分必要.动物养殖业的良好操作规范,低密度养殖和营养均衡,可以使动物健康生长并减少对抗生素和消毒剂的依赖;同时污水应通过生物降解、吸附、化学制剂及其他经济有效手段,去除耐药菌株,从根本上减少耐药菌株的传播.
| [1] |
HOLZEL C S, HARMS K S, BAUER J, et al. Diversity of antimicrobial resistance genes and class-1-integrons in phylogenetically related porcine and human Escherichia coli[J]. Vet Microbiol, 2012, 160(3 /4): 403-412. (  0) 0) |
| [2] |
XIONG W, SUN Y, ZHANG T, et al. Antibiotics, antibiotic resistance genes, and bacterial community composition in fresh water aquaculture environment in China[J]. Microb Ecol, 2015, 70(2): 425-432. DOI:10.1007/s00248-015-0583-x (  0) 0) |
| [3] |
MCDONNELL G, RUSSELI A D. Antiseptics and disinfectants: Activity, action, and resistance[J]. Clin Microbiol Rev, 1999, 12(1): 147-179. (  0) 0) |
| [4] |
BJORLAND J, STEINUM T, KVITLE B, et al. Widespread distribution of disinfectant resistance genes among Staphylococci of bovine and caprine origin in Norway[J]. J Clin Microbiol, 2005, 43(9): 4363-4368. DOI:10.1128/JCM.43.9.4363-4368.2005 (  0) 0) |
| [5] |
BAY D C, ROMMENS K L, TURNER R J. Small multidrug resistance proteins: A multidrug transporter family that continues to grow[J]. Biochim Biophys Acta, 2008, 1778(9): 1814-1838. DOI:10.1016/j.bbamem.2007.08.015 (  0) 0) |
| [6] |
KANG H Y, JEONG Y S, OH J Y, et al. Characterization of antimicrobial resistance and class Ⅰ integrons found in Escherichia coli isolates from humans and animals in Korea[J]. J Antimicrob Chemother, 2005, 55(5): 639-644. DOI:10.1093/jac/dki076 (  0) 0) |
| [7] |
WELCH T J, FRICKE W F, McDERMOTT P F, et al. Multiple antimicrobial resistance in plague: An emerging public health risk[J /OL]. PLoS One, 2007, 2 (3): e309. [2015-01-10] http://journals.plos.org/plosone/article?id=10.1371/journal.pone.0000309.
(  0) 0) |
| [8] |
WELCH T J, EVEHUIS J, WHITE D G, et al. IncA /C plasmid-mediated florfenicol resistance in the catfish pathogen Edwardsiella ictaluri[J]. Antimicrob Agents Chemother, 2009, 53(2): 845-846. DOI:10.1128/AAC.01312-08 (  0) 0) |
| [9] |
BAY D C, TURNER R J. Diversity and evolution of the small multidrug resistance protein family[J]. BMC Evol Biol, 2009, 9: 140. DOI:10.1186/1471-2148-9-140 (  0) 0) |
| [10] |
阮燕平. 革兰氏阴性菌耐消毒剂基因的研究进展[J]. 中国消毒学杂志, 2012, 29(10): 915-917. (  0) 0) |
| [11] |
HAMER D H, GILL C J. From the farm to the kitchen table: The negative impact of antimicrobial use in animals on humans[J]. Nutr Rev, 2002, 60(8): 261-264. DOI:10.1301/002966402320289395 (  0) 0) |
| [12] |
GILBERT P, MCBAIN A J. Potential impact of increased use of biocides in consumer products on prevalence of antibiotic resistance[J]. Clin Microbiol Rev, 2003, 16(2): 189-208. DOI:10.1128/CMR.16.2.189-208.2003 (  0) 0) |
| [13] |
只帅, 席美丽, 刘攻关, 等. 陕西部分地区不同食源性大肠埃希菌耐药性检测[J]. 中国食品学报, 2011, 11(1): 196-201. DOI:10.3969/j.issn.1009-7848.2011.01.029 (  0) 0) |
| [14] |
Clinical and laboratory standards institute. Performance standards for antimi-crobial disk and dilution susceptibility tests for bacteria isolated from animals: Documents VET01-A4E and VET01-S2E[S]. Wayne, PA, USA: CLSI, 2013.
(  0) 0) |
| [15] |
BUFFET-BATAILLON S, BRANGER B, CORMIER M, et al. Effect of higher minimum inhibitory concentrations of quaternary ammonium compounds in clinical E.coli isolates on antibiotic susceptibilities and clinical outcomes[J]. J Hosp Infect, 2011, 79(2): 141-146. DOI:10.1016/j.jhin.2011.06.008 (  0) 0) |
| [16] |
HUETA A, RAYGADA J L, MENDIRATTA K, et al. Multidrug efflux pump over expression in Staphylococcus aureus after single and multiple in vitro exposures to biocides and dyes[J]. Microbiol, 2008, 154(10): 3144-3153. DOI:10.1099/mic.0.2008/021188-0 (  0) 0) |
| [17] |
FUENTES D E, NAVARRO C A, TANTALEAN J C, et al. The product of the qacC gene of Staphylococcus epider-midis CH mediates resistance to beta-lactam antibiotics in gram-positive and gram-negative bacteria[J]. Res Microbiol, 2005, 156(4): 472-477. DOI:10.1016/j.resmic.2005.01.002 (  0) 0) |
| [18] |
SCHLUTER A, SZCZEPANOWSKI R, PUHLER A, et al. Genomics of IncP-1 antibiotic resistance plasmids isolated from waste water treatment plants provide evidence for a widely accessible drug resistance gene pool[J]. FEMS Microbiol Rev, 2007, 31(4): 449-477. DOI:10.1111/j.1574-6976.2007.00074.x (  0) 0) |
| [19] |
费春楠, 刘军, 沈凡, 等. 医院内感染病原菌对常见消毒剂耐药性的研究[J]. 环境与健康杂志, 2007, 24(12): 1011-1012. DOI:10.3969/j.issn.1001-5914.2007.12.033 (  0) 0) |
| [20] |
林辉, 郑剑. 铜绿假单胞菌对消毒剂抗药性的研究进展[J]. 中国消毒学杂志, 2007, 24(3): 269-271. DOI:10.3969/j.issn.1001-7658.2007.03.027 (  0) 0) |
| [21] |
SOUMET C, FOURREAU E, LEGRANDOIS P, et al. Resistance to phenicol compounds followingadaptation to quaternary ammonium compounds in Escherichia coli[J]. Vet Microbiol, 2012, 158(1 /2): 147-152. (  0) 0) |
 2015, Vol. 36
2015, Vol. 36