禽白血病(Avian leukosis,AL)是由甲型反转录病毒属的禽白血病病毒(Avian leukosis virus,ALV)引起的一种禽类肿瘤性传染病,临床上多以生产性能下降、免疫抑制、多个器官组织出现肿瘤为特征[1].通常依据病毒血清中和试验、囊膜糖蛋白特性和宿主范围等将ALV分为A ~ J共10个亚群,其中只有A、B、C、D、E和J亚群ALV来源于鸡.2012年,王鑫等[2]从我国芦花鸡中分离出3株疑似新亚群(K亚群)ALV.
根据ALV的自然传播方式和病毒复制的生物学特性,可将其分为外源性病毒和内源性病毒.外源性ALV是指不会通过宿主细胞染色体传递的病毒,而以病毒粒子形式进行垂直和水平传播,包括A、B、C、D、J亚群,其中A、B、J是常见的外源性ALV,致病力较强.因此,这些外源性病毒是AL净化的重要对象.内源性ALV是指前病毒cDNA可永久性整合进宿主细胞染色体基因组的病毒,可通过染色体垂直传播,主要是指E亚群,一般致病力较弱或不致病,但它可干扰对外源性ALV感染的检测,给ALV的净化工作带来了很大的困难[3].
近年来,AL在我国各地仍然广泛流行[4-5],特别是在2006-2009年间,ALV-J诱发的血管瘤给我国商品蛋鸡造成了巨大的经济损失[6].在《国家中长期动物疫病防治规划(2012-2020)》和《全国肉鸡遗传育种改良计划(2014-2025)》中均将AL列入重点防治对象和疾病净化目标.为了控制ALV的流行,崔治中等[7]拟定针对我国不同种禽场可选择实施不同的ALV净化方案.
外源性ALV的净化检测可从感染鸡的胎粪、泄殖腔拭子、血液、精液和蛋清等样品中进行.在不同公司的禽白血病净化方案中,蛋清通常被列为非常重要的检测对象,即通过p27抗原ELISA频度检测蛋清,根据检测结果淘汰阳性鸡,从而尽可能阻止ALV经种蛋垂直传播.但是这种方法的先天不足在于现有商品化试剂盒不能区分内源性和外源性病毒.目前国内外公认检测外源性ALV的“金标准”是病毒分离.病毒分离常用血浆样品,近年来也有研究开始分析不同品种鸡蛋清病毒分离的结果[8-10].
广东是黄羽肉鸡产业的重要生产和消费大省.近些年来AL也一直困扰黄羽肉鸡产业的健康发展.可喜的是,广东省一些黄羽种鸡品系相继启动了外源性ALV的净化工作.在对蛋清的净化检测结果分析过程中,有不少黄羽种鸡场的管理人员和兽医工作者经常问到同一个问题:即黄羽种鸡场蛋清p27抗原ELISA阳性鸡是否真的为外源性ALV带毒鸡.因此,本研究拟对广东省一黄羽种鸡的蛋清样品进行ALV抗原ELISA检测,进而采集蛋清ELISA阳性样品对应母鸡的血浆样品分别同时接种CEF和DF-1细胞进行病毒分离,以比较蛋清ELISA检测和血浆病毒分离之间的对应关系,从而为该黄羽种鸡群中AL的防控及净化方案提供科学依据.
1 材料与方法 1.1 蛋清样品采集从广东一黄羽种鸡场送检的2 691枚育种核心群种蛋中逐个吸取蛋清1 mL置于1.5 mL离心管,-80 ℃条件下保存备用.
1.2 试剂和仪器ALV抗原检测试剂盒(ALV Antigen Test Kit)为IDEXX公司产品;DMEM、FBS和Trypsin均为Gibco公司产品;pMD18-T载体、Go Taq DNA聚合酶为TaKaRa公司产品;SQ Tissue DNA提取试剂盒、胶回收试剂盒为OMEGA公司产品;大肠埃希菌Escherichia coli感受态细胞DH5α购于天根生化科技有限公司;DF-1细胞为农业部兽用疫苗创制重点实验室保存;鸡胚成纤维细胞(CEF)使用SPF鸡胚(北京梅里亚维通实验动物技术有限公司提供)制备;Bio-tek Elx800型酶标仪、凝胶成像及分析系统、高速低温离心机等仪器均由农业部兽用疫苗创制重点实验室提供.
1.3 蛋清ALV p27抗原ELISA检测将- 80 ℃保存的蛋清反复冻融3次,参照IDEXX公司ALV抗原检测ELISA试剂盒使用说明书进行p27抗原检测,并计算其S/P值.判定标准如下:S/P<0.2为阴性,S/P ≥0.2为阳性.
1.4 细胞培养与病毒分离参照文献[11]并有所改进.根据“1.3”中检测结果,立即采集其中70份不同区间S/P值(S/P ≥2.0,1.5≤S/P<2.0,1.0≤S/P<1.5,0.5≤S/P<1.0,0.2≤S/P<0.5,0.1≤S/P<0.2,S/P<0.1)所对应的母鸡抗凝血,无菌操作分离血浆后分别同时接种于24孔板中的CEF细胞悬液(1.7 × 105 mL-1)和DF-1细胞悬液(1.7 × 105 mL-1)中,每孔接种50 μL血浆,每个样品接种2孔,同时设立DMEM阴性对照和接种已知ALV的阳性对照各2孔,在37 ℃体积分数为5% CO2培养箱中培养,待细胞长至单层,换为体积分数1%的FBS细胞维持液再连续培养7 d,然后将CEF和DF-1细胞培养物反复冻融3次,5 000 r·min-1离心5 min,离心后的细胞上清液- 80 ℃条件下保存备用;细胞沉淀用于提取ALV前病毒基因组DNA.
1.5 细胞上清ELISA检测与数据统计细胞上清ELISA检测操作方法同“1.3”.并使用EXCEL软件对试验数据进行处理和统计分析.
1.6 前病毒DNA的制备参照“1.5”中的检测结果收集“ 1.4”中的CEF阳性且DF-1阴性(CEF+DF-1-)和1份CEF、DF-1均为阴性(CEF - DF-1 -)的CEF细胞沉淀,并随机选取不同区间CEF和DF-1均阳性(CEF+DF-1+)的DF-1细胞沉淀13份(A ~ F每个区间2份,G区间1份),按照SQ Tissue DNA试剂盒OMEGA公司说明书提取基因组DNA,- 20 ℃条件下保存备用.
1.7 引物合成和ALV亚群鉴定参照文献[11]以及GenBank中已公开发表的ALV序列分别合成用于扩增ALV-A、ALV-B、ALV-J和ALV-E的特异性PCR分型鉴定引物,其扩增产物预计大小分别为690、1 100、1 250、545 bp.
1.8 分离株gp85基因的扩增和测序参考文献[12]合成扩增ALV-J gp85基因的特异性引物,其扩增产物预计大小为924 bp.按照琼脂糖凝胶回收试剂盒说明书对PCR产物进行回收,然后将胶回收产物连接到pMD18-T载体,再将连接产物转化大肠埃希菌感受态细胞DH5α,将经菌液PCR鉴定阳性质粒送英潍捷基(上海)贸易有限公司测序.
1.9 gp85基因的序列分析利用DNAStar7.1基因分析软件对测序结果进行核苷酸序列的剪辑和拼接.将分离株的gp85基因核苷酸序列与GenBank中已公开发表的国内外各参考毒株的gp85基因核苷酸序列进行相似性分析,并用MEGA5.0绘制分离毒株与各参考毒株gp85基因序列的系统进化图谱.各亚群ALV参考毒株:RAV-0(M12172),RAV-1(M19113),RAV-2(M14902),PragueC(J02342),SR-D(M22730),HPRS103(Z46390),NX0101(DQ115805),HN06(HQ900844),SCAU11-H(KC149972),SCAU11-XG(KC149971),ADOL-7501(AY027920),CAUGX01(HM640943),WLY13(KJ631311),AHaq02(KF534753),ZH08(HQ316166),GD06SL1(EF107624).
2 结果 2.1 蛋清样品ALV抗原ELISA检测对来自广东一黄羽种鸡场育种核心群的2 691枚种蛋进行了ALV p27抗原ELISA检测,其中共检出243份阳性样品,则该批送检种蛋的ALV p27抗原阳性率为9.03%.
2.2 CEF和DF-1细胞的病毒分离结果根据“2.1”中的检出结果,参照步骤“1.4”,将蛋清对应编号母鸡的血浆样品分别同时用CEF细胞和DF-1细胞进行病毒分离,结果如表 1所示.DF-1细胞病毒分离总阳性率为60%(42 /70),CEF细胞病毒分离总阳性率为70%(49 /70),进一步分析后发现,DF-1细胞病毒分离阳性的样品,其CEF细胞病毒分离结果也均呈阳性.
|
|
表 1 血浆样品细胞培养物的ALV抗原ELISA检测结果1) Table 1 The results of ALV antigen-ELISA test of plasma cell cultures |
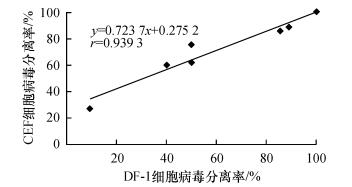
以DF-1细胞病毒分离率(x)为横坐标,CEF细胞病毒分离率( y)为纵坐标,建立回归线性方程(图 1),线性关系方程为y = 0.723 7x + 0.275 2,相关系数为0.939 3,说明这2种细胞的ALV分离结果符合率高度相关,检测结果准确、可靠.
|
图 1 CEF和DF-1细胞病毒分离相关性分析 Figure 1 Correlation analysis of virus isolation in CEF and DF-1 cells |
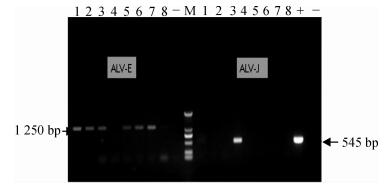
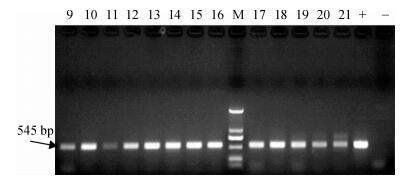
对CEF+DF-1-的全部7份CEF细胞样品及1份CEF -细胞样品分别标记为1 ~ 8,另外从7个不同区间中随机选取13份CEF+DF-1+的DF-1细胞样品标记为9 ~ 21,然后进行PCR亚群鉴定.8份CEF细胞样品中有6份(0.5≤S/P<1.0、S/P<0.1区间各2份,0.2≤S/P<0.5、0.1≤S/P<0.2区间各1份)扩增片段大小为1 250 bp左右,与ALV-E特异性片段大小相一致,有1份(来自0.2≤S/P<0.5区间)片段大小为545 bp,与ALV-J亚群特异性片段大小相一致,阴性细胞没有条带(图 2);而另13份DF-1细胞样品PCR产物的大小均为545 bp,与ALV-J片段大小相一致(图 3),说明该黄羽种鸡育种核心群不仅存在具有复制能力的内源性ALV,而且存在外源性ALV-J.
|
图 2 CEF细胞培养物的ALV PCR检测 Figure 2 ALV PCR detection of CEF cell cultures M:DNA marker DL2000(从上到下依次为:2 000,1 000,750,500,250,100 bp);1 ~ 8:检测样品;+:阳性对照;-:阴性对照. |
|
图 3 DF-1细胞培养物的ALV PCR检测 Figure 3 ALV PCR detection of DF-1 cell cultures M:DNA marker DL2000(从上到下依次为:2 000,1 000,750,500,250,100 bp);9 ~ 21:检测样品;+:阳性对照;-:阴性对照. |
以提取的DF-1细胞培养物cDNA为模板,用gp85特异性引物进行gp85基因的扩增,分离出3株ALV-J,分别命名为GD1401J、GD1402J、GD1403J.其gp85基因大小均为924 bp,与预期大小一致(图 4).

|
图 4 gp85基因的PCR扩增 Figure 4 PCR amplification of the gp85 gene M:DNA marker DL2000;1 ~ 3:GD1401J、GD1402J、GD1403J. |
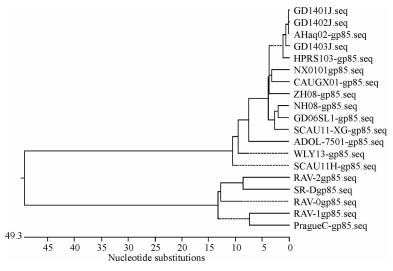
利用DNAStar软件分别对ALV-J分离株GD1401J、GD1402J和GD1403J的gp85基因序列进行剪辑和拼接,结果显示这3个毒株的gp85核苷酸序列长度均为924 bp,它们之间的核苷酸相似性达到98.8% ~ 99.8%.与GenBank中已公开发表的国内外不同ALV分离株gp85基因核苷酸序列进行相似性比较,发现这3个分离株的gp85基因与ALV- A、B、C、D、E亚群的gp85基因相似性只有49.3% ~ 49.9%,与ALV-J的gp85基因相似性高达87.4% ~ 100%.其中,与国外ALV-J分离株ADOL-7501相似性达87.4% ~87.5%;与ALV-J原型株HPRS103的相似性为97.7% ~98.1%;与国内广东地区部分分离株的相似性为92.3% ~ 94.8%,与安徽分离株AHaq02的相似性最高分别为99.8%、100%、99.0%.各亚群的gp85基因系统进化树显示,3个分离株与AHaq02位于同一个进化分支上,而与J亚群原型株HPRS103位于同一个大的进化分支上(图 5).
|
图 5 ALV-J gp85基因的核苷酸序列遗传进化树 Figure 5 Phylogenetic tree of ALV-J gp85 gene |
禽白血病是鸡群中最常见的肿瘤性疾病之一,它不仅会造成病禽的死亡和淘汰,还会引起鸡群生产性能下降、生长迟缓、免疫抑制等现象[1].近几年来该病所带来的损失也趋于严重.广东省作为我国的养禽大省,有多个优质的黄羽肉鸡地方品系,而AL的防控和净化已是十分迫切的生产课题.
目前,应用于ALV的检测方法包括病毒分离、ELISA、间接免疫荧光(IFA)等[13-15],这些方法各有其优缺点.在临床生产上针对鸡群AL的流行病学调查和净化,商品化的ELISA检测试剂盒由于其快速、简便、可大批量检测的特点具有不可替代的优势.因为种蛋具有便于收集保存和不易污染的特点,还有可用于病毒分离鉴定等优点[8].使用蛋清ALV抗原ELISA检测结果判断净化鸡群中个体ALV的感染状态,目前已在国内ALV净化检测和流行病学调查中被广泛应用.但国内外对ALV蛋清样品病毒分离方面的报道较少,笔者曾对蛋清样品进行病毒分离发现有相当比例的蛋清ELISA阳性样品其实是由内源性病毒引起的[9].但蛋清ALV抗原ELISA检测为阳性的鸡是否全部为外源性ALV病毒血症阳性,这个问题值得研究,尤其是对内源性病毒表达不一的各个黄羽肉种鸡品系.
病毒分离鉴定是检测ALV最有效、可靠的技术,常用于病毒分离的细胞有C /O表型的CEF细胞[16]和源于EV-0系胚胎的DF-1细胞系[17],其中CEF细胞对所有的内源性和外源性ALV均易感,而DF-1细胞系能够抗内源性ALV感染,而对所有外源性ALV易感.本研究通过比较蛋清样品对应母鸡的同一份血浆分别在CEF和DF-1不同细胞的病毒分离结果,发现蛋清样品抗原ELISA检测S/P越高,其对应母鸡的血浆样品在2种细胞上的病毒分离率也越高. S/P在2.0以上的蛋清样品其对应母鸡的血浆样品在CEF和DF-1细胞上病毒分离全部为阳性,而S/P低于2.0的蛋清样品对应母鸡的血浆样品在CEF和DF-1细胞上的病毒分离有差异.特别有趣的是S/P小于0.2的蛋清样品,参照ALV抗原ELISA检测试剂盒标准该蛋清对应的母鸡应该被判为阴性,但这些蛋清ELISA阴性鸡的对应血浆样品仍有26.3%(5 /19)病毒分离为外源性ALV(CEF+DF-1+)感染,有15.8%(3 /19)检测出内源性ALV(CEF+DF-1-),尤其值得注意的是,蛋清S/P低于0.1的母鸡其对应血浆样品中也有少数分别分离出了内源性和外源性ALV.对2种细胞病毒分离率进行回归线性分析,结果显示两者之间的相关系数为0.939 3,表明检测结果高度相关,检测结果准确.王明月等[8]从蛋清或泄殖腔棉拭子检测值小于0.2的鸡只中通过病毒分离的方法检测到有10%外源性ALV,这与本研究结果基本一致,充分说明了单独使用蛋清抗原ELISA方法可能会对净化检测结果造成一定程度的“漏检”.
本研究还对来自不同区间的7份CEF+DF-1-和1份阴性对照的CEF细胞沉淀以及13份CEF+DF-1+的DF-1细胞沉淀进行ALV亚群鉴定,结果显示7份CEF细胞沉淀中有6份为内源性ALV-E,1份为ALV-J(来自0.2≤S/P<0.5区间),另13份DF-1细胞沉淀全部为ALV-J,这与徐海鹏等[3]报道的能够从种蛋中分离出内源性ALV结果相一致.相对于血浆病毒分离结果,蛋清S/P小于0.5的阳性结果可造成一定比例的“误判”.这一结果对于净化初期来说似乎是可以接受的代价——即“宁可错杀、不可放过”,但是对于净化后期、尤其是进行净化评估验收或达标检测时,这种仅基于蛋清ELISA的“误判”可能会给净化实施单位造成“不公”,而应该用更合理的方法或者建立“复检机制”.而对于7份CEF+DF-1-中的1份ALV-J PCR阳性结果,可能是由不同方法的敏感性差异造成的.
此外,本研究还发现S/P在1.0 ~ 2.0之间的蛋清样品对应血浆样品病毒分离中分别有11.1%(1 /9)和14.3%(1 /7)的样品为阴性(CEF-DF-1-),究其原因,可能是由具有p27抗原表达但无复制能力的内源性ALV片段(如ev3位点)引起的.研究结果表明:正是由于ALV的感染和排毒时间的不可预测性以及各种检测方法的固有敏感性和特异性差异,无论是蛋清抗原ELISA检测还是经典的病毒分离法,单独使用1种检测方法,均不能1次完全检测出外源性ALV阳性鸡,故本研究也进一步提示在进行ALV的净化过程中需要不同方法组合的多次检测,甚至是多个世代才能更有效地完成ALV的净化工作.本研究结果表明该黄羽肉种鸡育种核心群不仅同时存在缺陷的内源性ALV和完整的具有完全复制能力的内源性ALV,而且也存在需要净化的外源性ALV.因此无论是从蛋清p27阳性率,还是外源性ALV的阳性率,均已经超过拟定的种禽健康标准,该黄羽肉种鸡育种核心群应尽快启动禽白血病的净化.
本研究还分离出3株病毒ALV-J分别命名为GD1401J、GD1402J和GD1403J,对其gp85基因进行序列分析后发现,3个分离株之间的核苷酸相似性高达98.8% ~ 99.8%.与国内外参考毒株的gp85基因进行比较发现,3个分离株与安徽分离株AHaq02相似性最高,同时与J亚群原型株HPRS103位于同一个大的进化分支上.有趣的是,历经多年的演变,该种鸡群分离株的gp85基因与J亚群原型株HPRS103相似性仍高达97.7% ~ 98.1%,说明他们可能来自共同的原始毒株,这些毒株的来源仍需进一步的追溯.
致谢:本试验是与人兽共患病防控制剂国家地方联合工程实验室、广东省动物源性人兽共患病预防与控制重点实验室共同完成.
| [1] |
PAYNE L N, BROWN S R, BUMSTEAD N, et al. A no- vel subgroup of exogenous avian leukosis virus in chickens[J]. J Gen Virol, 1991, 72(Pt 4): 801-807. (  0) 0) |
| [2] |
王鑫, 赵鹏, 崔治中. 我国地方品种鸡分离到的一个禽白血病病毒新亚群的鉴定[J]. 病毒学报, 2012, 28(6): 609-614. (  0) 0) |
| [3] |
徐海鹏, 孟凡峰, 董宣, 等. 种蛋中内源性禽白血病病毒的检测和鉴定[J]. 畜牧兽医学报, 2014, 45(8): 1317-1323. (  0) 0) |
| [4] |
高玉龙, 邵华斌, 罗青平, 等. 2009年我国部分地区禽白血病分子流行病学调查[J]. 中国预防兽医学报, 2010, 32(1): 32-35. (  0) 0) |
| [5] |
GAO Y L, YUN B, QIN L, et al. Molecular epidemiology of avian leukosis virus subgroup J in layer flocks in China[J]. J Clin Microbiol, 2012, 50(3): 953-960. DOI:10.1128/JCM.06179-11 (  0) 0) |
| [6] |
LI Y H, LIU X M, LIU H X, et al. Isolation, identifica- tion, and phylogenetic analysis of two avian leukosis virus subgroup J strains associated with hemangioma and mye- loid leukosis[J]. Vet Microbiol, 2013, 166(3 /4): 356-364. (  0) 0) |
| [7] |
崔治中, 孙淑红, 赵鹏, 等. 对种鸡场禽白血病净化方案的建议[J]. 中国家禽, 2014, 36(1): 3-6. DOI:10.3969/j.issn.1004-6364.2014.01.003 (  0) 0) |
| [8] |
王明月, 窦文文, 陈立坤, 等. 不同组织样品或检测方法对ALV检测结果的影响[J]. 中国兽医学报, 2013, 33(5): 659-663. (  0) 0) |
| [9] |
郝建勇, 徐海娈, 秦建如, 等. 蛋清样品用于禽白血病病毒分离的效果评估[J]. 中国家禽, 2014, 36(16): 21-25. DOI:10.3969/j.issn.1004-6364.2014.16.006 (  0) 0) |
| [10] |
RAJABZADEH M, DADRAS H, MOHAMMADI A. De- tection of avian leukosis virus subgroups in albumen of commercial and native fowl eggs using RT-PCR in Iran[J]. Trop Anim Health Prod, 2010, 42(8): 1829-1836. DOI:10.1007/s11250-010-9645-8 (  0) 0) |
| [11] |
LAI H Z, ZHANG H N, NING Z Y, et al. Isolation and characterization of emerging subgroup J avian leukosis vi- rus associated with hemangioma in egg-type chickens[J]. Vet Microbiol, 2011, 151(3 /4): 275-283. (  0) 0) |
| [12] |
LI L J, ZENG X W, HUA Y P, et al. Genetic diversity and phylogenetic analysis of glycoprotein gp85 of avian leukosis virus subgroup J wild-bird isolates from Northeast China[J]. Arch Virol, 2014, 159(7): 1821-1826. DOI:10.1007/s00705-014-2004-8 (  0) 0) |
| [13] |
QIU Y, LI X, FU L, et al. Development and characteriza- tion of monoclonal antibodies to subgroup A avian leukosis virus[J]. Vet Comp Oncol, 2014, 12(1): 47-51. DOI:10.1111/vco.2014.12.issue-1 (  0) 0) |
| [14] |
YUN B L, LI D L, ZHU H B, et al. Development of an antigen-capture ELISA for the detection of avian leukosis virus p27 antigen[J]. J Virol Methods, 2013, 187(2): 278-283. DOI:10.1016/j.jviromet.2012.11.027 (  0) 0) |
| [15] |
冯敏, 谭利强, 代曼曼, 等. 种禽场A亚群禽白血病病原学调查及分离株遗传进化分析[J]. 华南农业大学学报, 2014, 4(35): 11-15. (  0) 0) |
| [16] |
ZHANG H M, BACON L D, FADLY A M. Development of an endogenous virus-free line of chickens susceptible to all subgroups of avian leukosis virus[J]. Avian Dis, 2008, 52(3): 412-418. DOI:10.1637/8180-112707-Reg (  0) 0) |
| [17] |
SCHAEFER-KLEIN J, GIVOL I, BARSOV E V, et al. The EV-O-derived cell line DF-1 supports the efficient replication of avian leukosis-sarcoma viruses and vectors[J]. Virology, 1998, 248(2): 305-311. DOI:10.1006/viro.1998.9291 (  0) 0) |
 2015, Vol. 36
2015, Vol. 36



