乳腺肿瘤是母犬最常发的肿瘤,且一半以上为恶性肿瘤[1].乳腺是复管泡状腺,其功能的主要承担者是乳腺上皮细胞.乳腺上皮细胞的增殖和分化贯穿整个乳腺发育周期的始终[2].研究表明,大多数乳腺癌的发生都与乳腺上皮细胞关系密切[3-4].成功地对犬乳腺上皮细胞进行体外培养是研究犬乳腺肿瘤发生、转移、癌变的关键[5].因此,建立简单易行的犬乳腺上皮细胞体外培养方法至关重要.早在1957年,Lasfargues[6]就已经利用胶原酶从成年小鼠乳腺组织中成功分离出了乳腺上皮细胞.此后,人们对不同动物,如牛、羊、小鼠、兔等乳腺上皮细胞的离体培养进行了研究,其技术日趋成熟,并获得了成品的乳腺上皮细胞系[7-9].然而,犬的乳腺上皮细胞体外培养在国内外鲜有报道,其分离培养方法仍需要进一步探究.本试验从犬初乳中分离犬乳腺上皮细胞,并对其进行传代培养,观察细胞的生长以及形态,利用细胞免疫组化对所得细胞进行鉴定,成功建立了一种简单易行、经济快速获得大量高纯度犬乳腺上皮细胞的方法.
1 材料与方法 1.1 材料泌乳期健康比格犬,年龄2岁,饲养于广东省兽医临床重大疾病综合防控重点实验室.
主要试剂:D-MEM /F-12(11320-033,Gibico)、胎牛血清(10099-141,Gibico)、胰蛋白酶(25200- 072,Gibico)、青霉素-链霉素(15140-122,Gibico)、氢化考的松(Sigma)、转铁蛋白(Sigma)、表皮生长因子(Sigma)、鼠抗人角蛋白8单克隆抗体(BM0032,BOSTER)等.
主要仪器:超净工作台、CO2培养箱、普通光学显微镜、荧光显微镜、离心机等.
1.2 方法 1.2.1 乳汁的采集及细胞分离与培养用无菌生理盐水清洗乳房,再用酒精棉球擦净乳头.将乳汁挤入15 mL灭菌离心管中.放入37 ℃保温盒备用.将乳汁与含双抗的PBS按适宜比例混匀后,1 000 r·min-1离心5 min.此时可见离心管内混合液分为3层.小心吸出最上层乳脂层和中间层,然后再加入含双抗的PBS继续洗涤.如此重复直至离心后液体澄清透明.将最下层的细胞沉淀转移至适宜的细胞培养瓶中,加入完全培养基于体积分数为5%的CO2培养箱中进行原代培养.3 d后换液,待细胞长出单克隆后原瓶消化,直至细胞铺满培养瓶80%以上,消化传代,并冻存.
1.2.2 CCK-8法绘制细胞生长曲线选择第7代细胞进行复苏,用台盼蓝染色,对细胞进行计数.按103 ~ 104 mL-1的细胞接种于96孔板.置于37 ℃、体积分数为5%的CO2培养箱中进行培养.分别于培养后24、48、72、96 h以及5、6、7 d后,吸出培养液,PBS洗涤细胞2遍,加入培养液及体积分数为10%的CCK-8溶液(KeyGEN),于体积分数为5%的CO2、37 ℃培养箱中孵育1 ~ 4 h.酶标仪450 nm处检测每孔的D 值.每组3个重复并设置阴性对照和空白对照.用下式计算细胞存活率,绘制生长曲线.
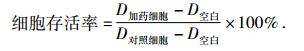
|
复苏冻存的细胞进行爬片,用体积分数为4%多聚甲醛固定,PBS洗涤3次,每次5 min.用体积分数为0.2%的TritonX-100处理细胞5 min,PBS洗涤3次.正常山羊血清封闭30 min后洗涤.加入按体积比1: 100稀释鼠抗人角蛋白8单克隆抗体(BOSTER)作为一抗,4 ℃孵育过夜.洗涤后,加入按体积比1: 100稀释的FITC标记羊抗鼠二抗(Millipore),孵育30 min.PBS洗涤3次,每次5 min.使用DAPI染色液(Sigma)室温染色10 min.在荧光显微镜下观察试验结果.
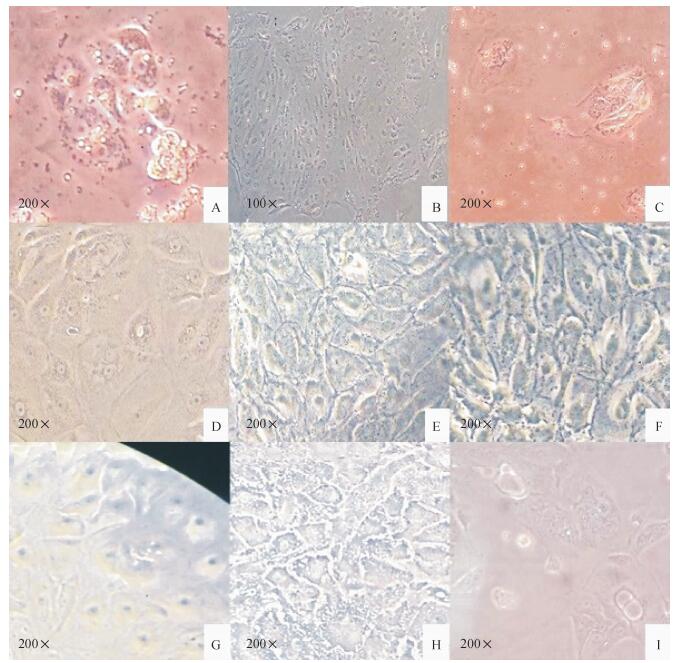
2 结果与分析 2.1 细胞形态学观察从乳汁中分离的细胞接种培养3 d后,此时已可见许多岛屿状的细胞克隆和分散的呈不规则形状的上皮细胞(图 1A).细胞岛屿周围见明显的生长晕.换液后继续培养,可见细胞逐渐增殖、平铺,待长至第9天时即可见形成许多大的单克隆,细胞形态较为单一,单层平铺生长,以多边形和长梭形细胞为主.此时已少见吞噬细胞的存在(图 1B).细胞在分裂增殖的过程中仍可见乳滴的分泌(图 1C).原瓶消化细胞,使单克隆细胞分散,继续培养,出现多核细胞,吞噬细胞完全消失(图 1D).3 d后细胞长满培养瓶80%以上,传代冻存.复苏后的细胞继续传代培养出现多种形态的细胞:多边形的细胞(图 1E)、长形的细胞(图 1F)、蜂窝状细胞(图 1G).细胞开始分泌大量乳滴(图 1H).细胞长满培养瓶底后不传代继续培养的,至铺满瓶底进入生长停滞期,此时细胞增殖不明显,细胞之间出现拉网现象(图 1I),此状态的细胞在换液的情况下,可维持生长3周以上,传代后仍可正常增殖.
|
图 1 犬乳汁中上皮细胞培养不同时间的细胞形态学观察 Figure 1 Morphological observation of the canine mammary epithelial cells cultured in different periods A:培养第3天可见岛屿状的细胞克隆;B:培养至第9天细胞单层平铺生长,形态单一;C:原代细胞增殖过程中可见乳滴分泌;D:多核细胞;E:多边形细胞;F:长形细胞;G:蜂窝状细胞;H:细胞大量分泌乳滴;I:拉网现象. |
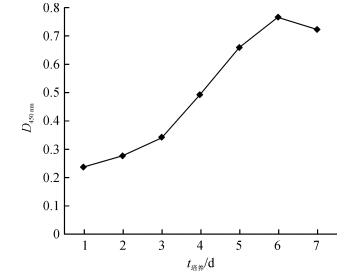
取冻存第7代的细胞进行复苏培养,绘制细胞生长曲线(图 2).细胞在第1至3天时生长较为缓慢.第3天以后进入对数生长期,细胞快速增殖.第6天以后细胞活力逐渐下降.表明所培养的细胞具有正常细胞增殖特性.
|
图 2 犬乳腺上皮细胞生长曲线 Figure 2 A growth curve of the canine mammary epithelial cells |
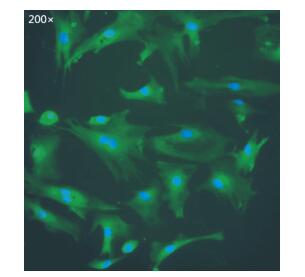
同样取冻存第7代细胞复苏培养,爬片固定后进行细胞免疫荧光鉴定.荧光显微镜下观察可见,细胞核在激发光照射下显示蓝色.一抗孵育呈阳性细胞的细胞质在激发光照射下显示绿色.细胞角蛋白8在分离培养的细胞中表达均成阳性(图 3).表明所分离的乳腺细胞的确为乳腺上皮细胞.
|
图 3 免疫组化鉴定细胞角蛋白8 Figure 3 Cytokeratin 8 identified with the immunohistochemical assay |
分离培养乳腺上皮细胞最常用的方法是酶消化法.本试验在用乳汁分离培养乳腺上皮细胞的同时,也试图用胶原酶消化犬乳腺组织来培养犬乳腺上皮细胞,但是效果并不理想.细胞中有大量的成纤维细胞污染,很难得到纯净的乳腺上皮细胞.且所获得乳腺上皮细胞状态较差,增殖能力较弱,这与郑玉才[10]的研究结果一致.究其原因可能是因为用乳腺组织培养乳腺上皮细胞对所取样品的要求高,必须要求所用动物乳腺健康且所取乳腺组织无其他组织残留;酶消化的时间和程度较难把握,且酶的作用对细胞的损伤较大.因此,采用酶消化法从组织中分离乳腺上皮细胞方法复杂、技巧性高、耗费时间,而且很难纯化[11].
动物在泌乳期时,大量乳腺上皮细胞脱落,随着乳汁排出.许多研究者认为从乳汁中分离乳腺上皮细胞成功率较低[12].本研究发现,乳汁中分离乳腺上皮细胞成功的关键是取材和操作,具体包括:1)要选择哺乳早期的犬进行乳汁采集,一般在1周内为宜;2)采集乳汁的过程中应注意无菌操作,尽量减少污染的可能性;3)收集到的乳汁应立即放在37 ℃保温盒中保存,并尽快进行后续处理.这对于保持细胞的活力至关重要;4)用加双抗的PBS对乳汁进行洗涤,吸出上层乳脂层时一定要缓慢操作,小心不要将下层细胞沉淀吸出,采集足够量的细胞是试验成功的关键;5)在细胞贴壁后长出大面积克隆时,应进行一次原瓶消化,此步骤保证新长出的细胞克隆不会衰老,有助于细胞进一步的增殖;6)细胞传代过程中,传代细胞长至3 ~ 4 d即可长满,如遇细胞密度较低的情况,可能在细胞没有铺满的情况下细胞就会出现衰老,此时应时刻观察细胞生长,在细胞衰老之前及时传代.
相对于酶消化法来说,从乳汁中分离乳腺上皮细胞的方法简便、经济、快捷,不需要复杂的操作方法和试剂.所得的细胞中除了乳腺上皮细胞,仅有吞噬细胞存在.吞噬细胞本身的贴壁增殖能力弱,容易自发死亡,经1次传代后即可得到高纯度的乳腺上皮细胞.所得的乳腺上皮细胞增殖能力强,生长迅速.细胞传至10代以上,未发现细胞老化,其形态、生长速度均未出现明显变化.
角蛋白8是存在于上皮细胞中的结构蛋白,是乳腺上皮细胞的标志性蛋白.本试验用鼠抗人角蛋白单克隆抗体作为一抗,复苏第7代冻存细胞进行爬片固定,进行细胞免疫荧光试验,从犬乳汁中分离出的细胞角蛋白8呈阳性.
CCK-8法绘制的细胞生长曲线表明,从犬乳汁中可分离培养的细胞具有正常的分裂增殖的能力.利用细胞形态学以及细胞免疫荧光的方法鉴定所得细胞为乳腺上皮细胞.表明从犬乳汁中可以分离培养出纯净的犬乳腺上皮细胞,所得细胞生长旺盛,增殖迅速.
本研究从犬乳汁中分离出了犬乳腺上皮细胞.建立了体外培养犬乳腺上皮细胞的方法.该方法操作简单、快捷、经济,且能有效地避免乳腺上皮细胞体外培养过程中面临的成纤维细胞污染以及酶处理造成细胞损伤的问题,在短时间内即可大量获得纯净的犬乳腺上皮细胞,为乳腺上皮细胞体外培养提供了有效的方法,也为研究犬乳腺肿瘤的发生、发展提供了素材.
| [1] |
SLEECKX N, DE ROOSTER H, VELDHUIS K E, et al. Canine mammary tumours, an overview[J]. Reprod Do- mest Anim, 2011, 46(6): 1112-1131. DOI:10.1111/rda.2011.46.issue-6 (  0) 0) |
| [2] |
MACIAS H, HINCK L. Mammary gland development[J]. Wiley Interdiscip Rev Dev Biol, 2012, 1(4): 533-557. DOI:10.1002/wdev.35 (  0) 0) |
| [3] |
AL-HAJJ M, WICHA M S, BENITO-HERNANDEZ A, et al. Prospective identification of tumorigenic breast cancer cells[J]. Proc Natl Acad Sci USA, 2003, 100(7): 3983-3988. DOI:10.1073/pnas.0530291100 (  0) 0) |
| [4] |
刘复生, 刘彤华. 肿瘤病理学[M]. 北京: 北京医科大学、中国协和医科大学联合出版社, 1997, 980-981.
(  0) 0) |
| [5] |
SAPPINO A P, BUSER R, LESNE L, et al. Aluminium chloride promotes anchorage-independent growth in human mammary epithelial cells[J]. J Appl Toxicol, 2012, 32(3): 233-243. DOI:10.1002/jat.v32.3 (  0) 0) |
| [6] |
LASFARGUES E Y. Cultivation and behavior in vitro of the normal mammary epithelium of the adult mouse: Ⅱ: Observations on the secretory activity[J]. Exp Cell Res, 1957, 13(3): 553-562. DOI:10.1016/0014-4827(57)90085-X (  0) 0) |
| [7] |
ANAND V, DOGRA N, SINGH S, et al. Establishment and characterization of a buffalo (Bubalus bubalis) mammary epithelial cell line[J]. PloS One, 2012, 7(7): 1-14. (  0) 0) |
| [8] |
TONG H, LI Q, GAO X, et al. Establishment and characterization of a lactating dairy goat mammary gland epithelial cell line[J]. In Vitro Cell & Dev-An, 2012, 48(3): 149-155. (  0) 0) |
| [9] |
MROUE R, BISSELL M J. Three-dimensional cultures of mouse mammary epithelial cells[M] // SCOTT H. Epithelial cell culture protocols. Berlin: Springer, 2013: 221-250.
(  0) 0) |
| [10] |
郑玉才. 水牛乳腺上皮细胞的体外培养[J]. 西南民族学院学报:自然科学版, 1994, 20(1): 42-44. (  0) 0) |
| [11] |
多曙光, 吴应积, 罗奋华, 等. 牛乳腺上皮细胞的分离培养及其生物学特性[J]. 动物学研究, 2006, 27(3): 299-305. DOI:10.3321/j.issn:0254-5853.2006.03.012 (  0) 0) |
| [12] |
李艳, 徐凯, 赵国琦. 奶牛乳腺上皮细胞的培养与鉴定[J]. 上海畜牧兽医通讯, 2014(1): 8-11. DOI:10.3969/j.issn.1000-7725.2014.01.003 (  0) 0) |
 2015, Vol. 36
2015, Vol. 36


