我国蔗区主要分布在广西、广东、云南、海南等南方黄、红壤地区, 90%以上的种植面积为缺乏灌溉的旱坡地.甘蔗Saccharum officinarum L.为禾本科甘蔗属植物, 属C4作物, 其对温度、水分要求较严格(年积温需5 500 ℃以上、年降水量要求800 mm以上), 从种苗发芽、发根、幼苗生长、分蘖、伸长、糖分积累到成熟, 整个生育过程都要消耗大量水分[1].因此, 季节性干旱已成为限制我国甘蔗生产的首要环境因素, 也成为了制约我国蔗糖生产的关键因素之一.
植物受到干旱、低温、高盐、重金属等胁迫下, 会直接或间接地发生水分胁迫, 为了适应逆境, 植物体内会在短时间内迅速大量地合成和积累如脯氨酸(Pro)、甜菜碱等一系列渗透调节物质[2].其中, 脯氨酸是分布最广、水溶性最大的氨基酸, 具有较强的水合能力.在高等植物中因脯氨酸代谢的初始底物不同其合成的途径也不尽相同, 一般分为谷氨酸(Glu)途径[3]和鸟氨酸(Orn)途径[4], 而每一个途径都受到关键酶的调节, 它们的关键酶分别是△1-毗咯琳5-羧酸合成酶(P5CS)和δ-鸟氨酸转氨酶(δ-OAT) [5-6].脯氨酸合成积累途径在不同植物、不同生理条件以及不同组织器官中各不相同.Roosens等[7]研究不同生育期植物脯氨酸积累途径发现, 幼小植株以Orn途径为主, 成年植株以Glu途径为主, 而在渗透胁迫条件下2条途径发挥同样重要的作用.钱大文等[8]的研究认为, NaCl胁迫下海马齿植株内游离脯氨酸合成积累的2个途径均被启动和发生作用, 并表现出以Glu→Pro途径为主、Orn→Pro途径为辅.黄诚梅等[9]的研究表明, 在PEG处理下甘蔗伸长期叶中脯氨酸生物合成中谷氨酸→脯氨酸途径比精氨酸→鸟氨酸→脯氨酸途径更占优势地位.
磷素(P)在植物体内的作用极为重要, 参与生物膜、原生质和细胞核的构成, 参与ATP等的能量代谢[10].在正常水分条件下, P对作物的生长发育、光合作用等生理过程具有显著作用[11].在旱地施肥增产技术应用中, P肥的效果明显, P能提高原生质胶体的水合度和细胞机构的充水度, 使其维持胶体状态, 并能增加原生质的黏度和弹性, 因而增强了原生质抵抗脱水的能力[12].赵海超等[13]认为增施P肥可以促进根系生长、优化营养分配、提高根系活力、降低丙二醛含量、提高超氧化物歧化酶活性, 从而提高马铃薯的抗旱性, 但施P量过高会降低马铃薯的抗旱性.前人有许多关于不同施肥量对甘蔗产量、生长性状的影响研究[14-16], 也有很多关于甘蔗脯氨酸积累的研究[17-18], 但是, 针对干旱胁迫下, 不同P肥施用量对甘蔗植株体内的脯氨酸合成积累关键基因P5CS、δ-OAT表达和酶活性的变化, 以及脯氨酸合成积累途径的研究鲜见报道.本文以甘蔗品种粤糖55为研究材料, 在正常水分生长和干旱胁迫条件下, 测定4个P肥施用水平的甘蔗植株内P5CS、δ-OAT基因表达和酶活性、以及游离脯氨酸含量等生理生化指标, 以阐明P肥对甘蔗植株脯氨酸合成积累及耐旱性的作用效应, 为甘蔗耐旱高效栽培提供理论参考.
1 材料与方法 1.1 材料甘蔗品种为粤糖55, 粤西蔗区主栽品种之一.
1.2 试验方法试验在广东海洋大学农业生物研究所进行.桶栽试验:塑料桶高50 cm、口径40 cm, 桶下端10 cm处的侧面开4个排水小孔, 每桶装砖红壤土25 kg, 每桶种植1个双芽苗.土壤肥力状况:pH 5.08, 碱解氮152.12 mg·kg-1、速效钾158.56 mg·kg-1、有效磷53.27 mg·kg-1、有机质27.80 g·kg-1.在施用尿素918 kg·hm-2和钾肥(KCl)750 kg·hm-2的水平上(为粤西蔗区通常施N、K肥水平), 设置4个过磷酸钙施用水平:0(CK)、900、1 800、2 700 kg·hm-2; 设置2个生长条件:1)土壤含水量>18%作为正常条件; 2)土壤含水量<8%时(甘蔗出现枯萎)作为干旱胁迫.随机区组试验设计, 3次重复.
2013年6月18日开始种植, 按计划施肥量施用全量的磷肥、半量的氮肥和钾肥, 肥料与土壤充分混匀, 施肥在20 ~ 30 cm土层内, 齐苗后定苗, 每桶选留对称且健壮的2株甘蔗幼苗, 每隔2 d浇1次水, 保持土壤湿润; 于2013年9月10日追肥, 将计划施肥量的另一半氮肥和钾肥全部施入.2013年11月30日, 实测土壤含水量(w)为18.65% ± 0.32%时, 每桶取1株甘蔗苗进行测试分析, 采集其-1叶进行脯氨酸含量、δ-OAT酶活性、P5CS酶活性的测定, 取心叶进行总RNA提取.然后, 将试验桶栽甘蔗移入玻璃温室内, 停水管理6 d进行干旱胁迫处理, 当甘蔗叶片开始出现萎蔫时[2013年12月6日, 实测土壤含水量(w)为7.35% ± 0.27%]按上述方法取样、测试分析.
1.3 试验指标的测定和引物设计脯氨酸含量的测定按Bates等[19]的方法; P5CS提取方法依照Kavi等[20]的方法, 其活性测定参照黄诚梅[21]的方法以每分钟生成1 μmol γ-谷氨酰胺所需要的酶量为一个酶活性单位(U); δ-OAT的抽提按照Delauney等[4]的方法, 其活性测定参照Kim等[22]的方法进行, 以每小时生成1 mmol P5C所需要的酶量为一个酶活性单位(U); 叶片色素含量提取采用乙醇-丙酮混合液浸泡法[23]; 总引物由生工生物工程(上海)股份有限公司合成; 实时荧光定量PCR (RT-qPCR)用TaKaRa宝生物公司的SYBR® Premix Ex TaqTMⅡ (Tli RNaseH Plus)试剂盒, 操作步骤参照说明书; 仪器使用Roche LightCycler® 2.0;基因表达分析采用2-△△CT法[24]进行分析, 以正常水分条件下的基因表达量定义为1.
引物设计:采用引物设计软件Primer Premier 5.0, 按照GenBank中甘蔗P5CS基因的cDNA序列(EU005373.2)、甘蔗δ-OAT基因的cDNA序列(EF517495.1), 并根据RT-qPCR的引物设计原则进行设计, 最终筛选引物特异性好、没有引物二聚体的引物:1) P5CS的引物, F:5′-GTGGGTGTTGAAGGTCTC-3′, R:5′-AGGAAGGTTCTTATGGGT-3′; 2) δ-OAT的引物, F:5′-GAGTTTAGGGACCAGTTACAGAA3′, R:5′-AAGCAGGAGATAGAGCGTCAT-3′.其中, 内参基因引物则引用阙友雄等[25]筛选的25SrRNA引物, F:5′-GCAGCCAAGCGTTCATAGC-3′, R:5′CCTATTGGTGGGTGAACAATCC-3′.
1.4 数据统计方法应用统计分析软件SAS10.3在PC机上进行, 用Duncan’s法测定不同磷肥施用处理间的生理指标的差异显著性.
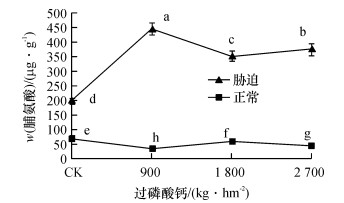
2 结果与分析 2.1 不同磷肥水平甘蔗游离脯氨酸含量如图 1可知, 在正常情况下, 甘蔗体内游离脯氨酸的含量不高, 但不同处理间差异显著, 说明磷肥对脯氨酸含量的影响显著, 不施磷肥(CK)时, 脯氨酸含量最大, 而脯氨酸含量最小为施磷肥900 kg·hm-2的处理.干旱胁迫时, 甘蔗植株体内游离脯氨酸含量大幅增加, 其中CK的脯氨酸含量最小, 且与其他水平差异显著; 施磷肥900 kg·hm-2时脯氨酸的含量最大, 且显著高于1 800和2 700 kg·hm-2处理的脯氨酸含量.
|
图 1 不同磷肥水平脯氨酸含量的变化 Figure 1 The changes of proline contents at different phosphorus levels 图中凡是有一个相同小写字母者, 表示差异不显著(Duncan’s法, P>0.05). |
在正常水平下, CK的脯氨酸含量是施磷肥900 kg·hm-2的1.99倍, 说明磷肥不足会影响甘蔗的正常生长, 出现磷胁迫, 使得脯氨酸的含量增加.干旱胁迫时, 甘蔗体内脯氨酸的合成积累效应显著, 与正常水分时相比, 平均增幅为290.85 μg·g-1; 磷肥水平900 kg·hm-2时, 脯氨酸的含量最高, 效应最明显, 为最佳施磷肥量.
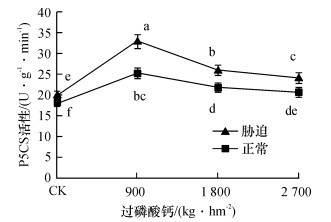
2.2 不同磷肥水平甘蔗P5CS酶活性变化P5CS作为合成脯氨酸中谷氨酸合成途径的关键酶, 其活性变化将直接影响脯氨酸合成积累的效应.从图 2中可看出, 在正常水分或干旱胁迫下, 在4个磷肥处理间P5CS的活性变化趋势类似, 但在干旱胁迫下的P5CS活性明显增大, 尤其是在磷肥水平900 kg·hm-2最为明显, 干旱胁迫时是正常水平时的1.3倍.P5CS活性在不施磷肥时最低, 在磷肥水平900 kg·hm-2时活性最高, 随后急剧下降.
|
图 2 不同磷肥水平P5CS酶活性的变化 Figure 2 The changes of P5CS enzyme activities at different phosphorus levels 图中凡是有一个相同小写字母者, 表示差异不显著(Duncan’s法, P>0.05). |
正常水分情况下, 4个磷肥水平的P5CS活性平均为21.3 U · g-1 · min-1, 干旱胁迫时为25.63 U·g-1·min-1, 平均变化幅度为4.33 U·g-1·min-1.这一结果表明, 干旱胁迫下甘蔗P5CS活性显著地被激活, 尤其是在磷肥水平900 kg·hm-2时.
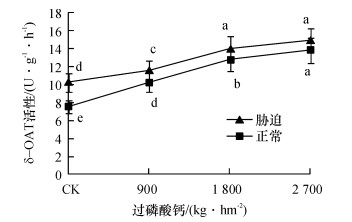
2.3 不同磷肥水平甘蔗δ-OAT酶活性变化从图 3中可知, 无论正常水分或者干旱胁迫下, δ-OAT活性都是随磷肥施用量增加而增强.除2 700 kg·hm-2处理外, 不同磷肥水平下正常水分与干旱胁迫间的δ-OAT活性均有显著性差异.说明干旱胁迫下, 甘蔗植株δ-OAT活性有增强的趋势, 其平均增幅为1.52 U·g-1·h-1.
|
图 3 不同磷肥水平δ-OAT酶活性的变化 Figure 3 The changes of δ-OAT enzyme activities at different phosphorus levels 图中凡是有一个相同小写字母者, 表示差异不显著Duncan’s法, P>0.05). |
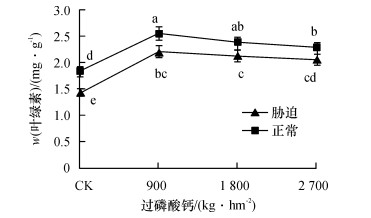
从图 4可知, 在正常水分或干旱胁迫下, 4个磷肥处理间叶绿素(Chl)含量变化趋势类似, 但在干旱胁迫下的叶绿素含量明显降低, 平均下降率为13.3%.表明在较为严重的干旱胁迫下, 甘蔗叶片的叶绿素含量显著降低, 进而影响甘蔗的光合作用能力.但在正常水分或干旱胁迫下, 4个磷肥处理间甘蔗叶片叶绿素含量均以900 kg·hm-2时最大.表明在湛江砖红壤种植甘蔗时, 过磷酸钙的施用量为900kg·hm-2最有利于甘蔗叶片叶绿素的合成, 从而促进甘蔗的光合作用.
|
图 4 不同磷肥水平叶片叶绿素含量的变化 Figure 4 The changes of leaf chlorophyll contents at different phosphorus levels 图中凡是有一个相同小写字母者, 表示差异不显著(Duncan’s法, P>0.05). |
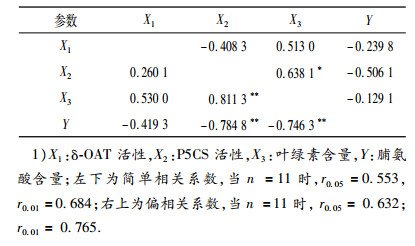
从表 1可知, 正常供水情况下, 脯氨酸含量(Y)与δ-OAT活性(X1)、P5CS活性(X2)、叶绿素含量(X3)之间均表现为负简单相关, 且与X2、X3相关达极显著水平; X2与X3之间呈极显著水平的正简单相关性.偏相关结果表明, X3与X2之间呈显著的正偏相关, 其他指标间偏相关均未达显著水平.
|
|
表 1 正常水分下生理指标间的简单和偏相关分析1) Table 1 Simple and partial correlation analyses of physiological parameters at the normal water level |
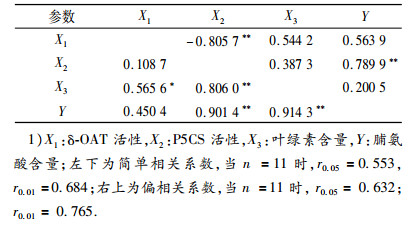
从表 2可看出, 干旱胁迫下, Y与X1、X2、X3之间均表现为正简单相关, 除X1与X2、X1与Y外, 均达到显著或极显著水平.偏相关分析结果表明, X2与Y达极显著正向偏相关, X1与X2达极显著负向偏相关.表明在干旱胁迫下, P5CS的活性与脯氨酸含量间不仅具有极显著水平的简单相关性, 还有极显著水平的偏相关性; 脯氨酸合成积累的2个关键酶P5CS和δ-OAT之间表现为极显著水平的负向偏相关.
|
|
表 2 干旱胁迫下个生理指标间的简单和偏相关性分析 Table 2 Simple and partial correlation analyses of physiological parameters under drought stress |
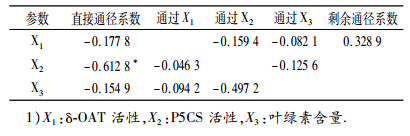
从表 3中可知, 正常水分条件下, X1、X2、X3对Y的直接通径系数均为负数, 且仅有X2对Y的直接通径系数达到显著水平.剩余通径系数较大, 为0.328 9, 说明在正常水分条件下, 植株游离脯氨酸的合成积累受其他随机因素的影响较大.
|
|
表 3 正常水分下X1、X2和X3对Y的通径分析1) Table 3 The path analyses of X1, X2 and X3 to Y at the normal water level |
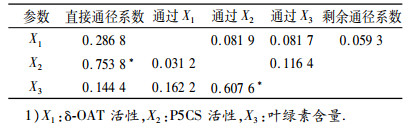
从表 4可以发现, 干旱胁迫下, 在3个直接通径系数中, 只有X2对Y的直接通径系数达到了显著水平; 同时, 叶绿素含量通过P5CS活性对脯氨酸含量的间接通径系数也达到了显著水平; 剩余通径系数仅有0.059 3, 说明在本研究条件下, 随机因子对脯氨酸合成积累量的影响较小.可见, 在δ-OAT活性、P5CS活性和叶绿素含量3个因素中, P5CS活性对脯氨酸含量的直接和间接作用均最大, 即在干旱胁迫下, 甘蔗植株P5CS活性对其脯氨酸合成积累量的影响最为重要.
|
|
表 4 干旱胁迫下X1、X2和X3对Y的通径分析1) Table 4 The path analyses of X1, X2 and X3 to Y under drought stress |
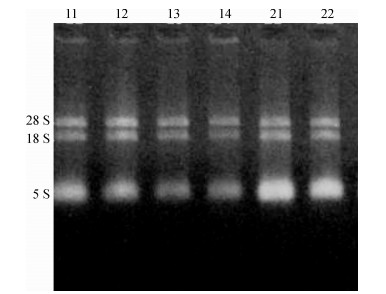
对提取的总RNA经10 g·L-1琼脂糖凝胶电泳检测, 28S和18S这2条带清晰完整, 没有明显的拖尾现象(图 5), 表明总RNA样品比较完整, 没有明显降解.紫外分光光度计法检测RNA浓度表明, D260 nm/D280 nm比值在1.8 ~ 1.9之间, 表明其RNA纯度与浓度达到合成cDNA第1链的要求.
|
图 5 叶片总RNA电泳图 Figure 5 Electrophoresis of total RNA of leaves 泳道11 ~ 14分别为干旱胁迫下过磷酸钙用量分别为0、900、1 800、2 700 kg·hm-2的样品, 21、22分别是11、12的重复样品. |
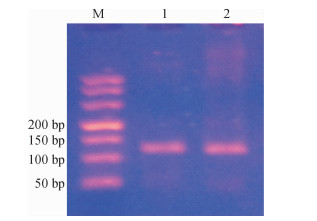
用上述P5CS、δ-OAT的引物进行普通PCR扩增, 并用30 g·L-1的琼脂糖凝胶电泳, 得到的PCR产物条带单一, 没有引物二聚体出现, 片段大小符合荧光定量PCR的要求(图 6).同时, 回收PCR产物并送生工公司测序, 通过Blast比对为目的基因片段.可以做下一步的RT-qPCR.
|
图 6 P5CS和δ-OAT的PCR产物电泳图 Figure 6 Electrophoresis of the PCR products of P5CS and δ-OAT M:DL500 DNA Marker; 1:P5CS; 2:δ-OAT. |
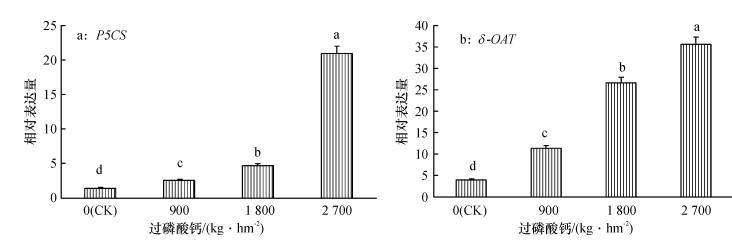
从图 7可知, 随着施磷水平的增加, P5CS和δ-OAT基因相对于正常水分条件下的表达量均呈现递增的趋势.不施磷肥时, 2个基因的相对表达量都最小, 分别为1.48和4.03, 而施磷水平2 700 kg·hm-2时, 两者的基因相对表达量最大, 分别为20.96和35.89.表明磷肥的施用量影响P5CS、δ-OAT基因的表达.
|
图 7 干旱胁迫下甘蔗叶片中P5CS、δ-OAT基因的相对表达量 Figure 7 Relative expressions of P5CS and δ-OAT genes in sugarcane leaves under drought stress 各图中柱子上凡是有一个相同小写字母者, 表示差异不显著(Duncan’s法, P>0.05). |
在固定施用尿素918 kg·hm-2和钾肥(KCl)750 kg·hm-2时, 在水分供应正常的情况下, N、P、K肥之间的配比合理(磷肥水平900 kg·hm-2时)能使甘蔗植株正常生长, 体内各项生理代谢平衡, 细胞内没有产生渗透压, 合成脯氨酸的2个关键酶P5CS和δ-OAT活性较小, 没有被显著激活, 同时脯氨酸含量也处于低水平.随着磷肥施用量的增加, 脯氨酸含量呈现先减少后增加的趋势, P5CS酶活性呈现先增加后减少的趋势, δ-OAT酶活性则呈现一直增加的趋势, 说明脯氨酸合成的2个关键酶P5CS和δ-OAT的活性与脯氨酸含量的变化趋势不一致性.相关研究表明, 除了脯氨酸的合成酶外, 还有其他的一些酶如脯氨酸运输酶[26]、谷氨酰胺合成酶[27]等也参与了脯氨酸的积累过程.但是, 当N、P、K肥之间的配比不合理时, 即使水分供应正常, 也致使甘蔗植株生长代谢异常, 细胞内产生渗透胁迫, 表现为游离脯氨酸含量显著增加, 以抵抗由于N、P、K肥之间的配比不合理所产生的渗透压, 保证甘蔗植株的正常生长.
干旱胁迫不同程度地激活了P5CS和δ-OAT基因的表达以及P5CS和δ-OAT酶活性, 从而使得脯氨酸含量急剧增加, 以缓解干旱胁迫所造成的细胞渗透压力, 维持体内正常的生理代谢平衡, 减少干旱胁迫带来的不利影响.同时磷肥的施用量对P5CS和δ-OAT基因的表达、P5CS和δ-OAT酶活性、脯氨酸含量有显著的影响.本研究中, 当磷肥施用量大于900 kg·hm-2时, 脯氨酸含量和P5CS酶活性都呈现下降趋势, 而δ-OAT酶活性则呈现一直增加的趋势, P5CS、δ-OAT基因的相对表达量也呈增长趋势.由此可推测磷素的增加有利于P5CS、δ-OAT基因的表达, 从而有利于P5CS和δ-OAT的合成, 促使其活性的提高, 特别是δ-OAT基因对磷素的响应较为明显.但是P5CS基因的表达量与其对应酶的活性不一致, 可能是由于基因从表达到成功翻译受到许多因子调控[28], 比如在蛋白质水平上存在钝化蛋白[29]、相关降解酶对酶活性进行调控而产生差异.谭彩霞等[30]认为小麦中GBSS基因的相对表达量与GBSS酶活性间相关不显著是由于GBSS基因属于转录后调控.这些相关的调控机理有待于进一步的探究.
在N、K肥施用量分别为918、750 kg·hm-2水平时, 无论是在正常水分条件下还是在干旱胁迫下, 4个过磷酸钙的施用水平间, 甘蔗植株中P5CS和δ-OAT基因的表达、P5CS和δ-OAT酶活性以及游离脯氨酸的含量均有明显的差异, 表明磷肥的施用量影响植物生理生化过程和植株体内的代谢平衡, 从而影响植株生长发育.当过磷酸钙的施用水平为900 kg·hm-2时, 正常水分条件下, 甘蔗植株脯氨酸含量最低, P5CS与δ-OAT酶活性亦处于较低的水平; 而在干旱胁迫下, 甘蔗植株游离脯氨酸的含量最大, P5CS活性最大, δ-OAT酶活性也处于较高水平, P5CS和δ-OAT基因的相对表达量分别为2.63和11.39.因此, 本研究中的砖红壤基于甘蔗植株游离脯氨酸合成积累的最佳施肥方案是尿素、过磷酸钙、氯化钾的用量分别为918、900、750 kg·hm-2.
3.2 不同磷肥施用水平对甘蔗脯氨酸的合成积累途径的影响高等植物体内脯氨酸的合成积累有谷氨酸(Glu)途径和鸟氨酸(Orn)途径, P5CS和δ-OAT酶分别是这2个途径的关键酶[3-6, 31-33].王丽媛等[34]的研究认为通常在植物受到胁迫或氮素缺乏的情况下, 脯氨酸的主要来源是谷氨酸合成途径; 在氮素供应充足的情况下, 脯氨酸合成的主要途径则是鸟氨酸途径.曹芳等[35]研究发现胁迫条件下硝酸钾可以增加烟草叶片中的脯氨酸含量, PEG胁迫下硝酸钾能增强鸟氨酸代谢途径中δ-OAT酶活性.由此表明, 大量的矿质元素可以影响植物脯氨酸的合成积累途径.
本研究在固定施用尿素918 kg·hm-2和钾肥(KCl)750 kg·hm-2水平时, 过磷酸钙设置4个施入水平, 在干旱胁迫下, 甘蔗植株体内的P5CS、δ-OAT基因表达及其酶活性被不同程度地激活, 从而合成积累大量的脯氨酸, 这显然是谷氨酸途径(Glu → Pro)和鸟氨酸途径(Orn→Pro)共同作用的结果.相关、偏相关分析表明, 在干旱胁迫下, 植株游离脯氨酸含量与P5CS酶活性的简单相关系数及偏相关系数均达到了极显著水平, 而Pro含量与δ-OAT酶活性间均未达到显著水平; 通径分析中P5CS酶活性对Pro含量的直接通径系数达到了显著水平, δ-OAT酶活性对Pro含量的直接通径系数未达显著水平.说明干旱胁迫下甘蔗植株中P5CS酶活性对游离脯氨酸的合成积累贡献最大, 此时甘蔗植株合成积累游离脯氨酸的途径是以谷氨酸途径(Glu→Pro)为主, 鸟氨酸途径(Orn→Pro)为辅.这一结果与姜淑欣等[36]以小麦为材料、Choudhary等[37]以水稻为材料、黄诚梅等[9]以甘蔗为材料的研究结果相似.在正常水分条件下, 植株游离脯氨酸含量与P5CS和δ-OAT酶活性、叶绿素含量的简单相关、偏相关均呈负相关; 通径分析中也均为负向贡献; P5CS酶活性与脯氨酸含量的简单相关系数、直接通径系数达到了显著水平, 偏相关系数的绝对值也较δ-OAT酶活性与脯氨酸含量间的大.由此推测, 在正常供水情况下, P5CS酶活性对植株游离脯氨酸的合成调节作用比较大.此外, 通径分析中剩余通径系数较大, 为0.328 9, 说明正常水分供应下, 甘蔗植株的游离脯氨酸合成积累还受到其他一些因素的调节, 推断应为降解通径的一些相关酶, 如脯氨酸降解酶的调节[9, 26].
| [1] |
轻工业部甘蔗糖业科学研究所, 广东省农业科学院. 中国甘蔗栽培学[M]. 北京: 中国农业出版社, 1985, 225-228.
(  0) 0) |
| [2] |
焦蓉, 刘好宝, 刘贯山, 等. 论脯氨酸积累与植物抗渗透胁迫[J]. 中国农学通报, 2011, 27(7): 216-221. (  0) 0) |
| [3] |
HU C A, DELAUNEY A J, VERMA D P S. A bifunctional enzyme (△1-pyrroline-5-carboxylate synthetase) catalyzes the first two steps in proline biosynthesis in plants[J]. Proc Natl Acad Sci USA, 1992, 89(19): 9354-9358. DOI:10.1073/pnas.89.19.9354 (  0) 0) |
| [4] |
DELAUNEY A J, HU C A, KISHORP B K, et al. Cloning of ornithine-aminotransferase cDNA from Vigna aconitifolia by trans-complementation in Escherichia coli and regulation of proline biosynthesis[J]. J Biol Chem, 1993, 268(25): 18673-18678. (  0) 0) |
| [5] |
SZABADOS L, SAVOUR A. Proline:A multifunctional amino acid[J]. Trends Plant Sci, 2009, 15(2): 89-97. (  0) 0) |
| [6] |
LEHMANN S, FUNK D, SZABADOS L. Proline metabolism and transport in plant development[J]. Amino Acids, 2010, 39(4): 949-962. DOI:10.1007/s00726-010-0525-3 (  0) 0) |
| [7] |
ROOSENS N H C J, THU T T, ISKANDAR H M, et al. Isolation of ornithine-δ- aminotransferase cDNA and effect of salt stress on its expression in Arabidopsis[J]. Plant Physiol, 1998, 117(1): 263-271. DOI:10.1104/pp.117.1.263 (  0) 0) |
| [8] |
钱大文, 周鸿凯, 江大可, 等. NaCl胁迫下海马齿(Sesuvium portulacastrum L.)植株内游离脯氨酸的合成积累途径[J]. 中国野生植物资源, 2013, 32(3): 35-39. DOI:10.3969/j.issn.1006-9690.2013.03.010 (  0) 0) |
| [9] |
黄诚梅, 毕黎明, 杨丽涛, 等. 聚乙二醇胁迫对甘蔗伸长期间叶中脯氨酸积累及其代谢关键酶活性的影响[J]. 植物生理学通讯, 2007, 43(1): 77-80. (  0) 0) |
| [10] |
杨俊兴, 张彤, 吴冬秀. 磷素营养对植物抗旱性的影响[J]. 广东微量元素科学, 2003, 10(12): 13-19. DOI:10.3969/j.issn.1006-446X.2003.12.002 (  0) 0) |
| [11] |
李唯. 植物生理学[M]. 北京: 高等教育出版社, 2012, 46-47.
(  0) 0) |
| [12] |
舒玉. 磷肥对草地早熟禾和黑麦草抗旱性的影响[D]. 哈尔滨: 东北林业大学, 2008.
(  0) 0) |
| [13] |
赵海超, 龚学臣, 抗艳红, 等. 不同施磷量对马铃薯苗期抗旱性的影响[J]. 安徽农业科学, 2012, 40(6): 3314-3316. DOI:10.3969/j.issn.0517-6611.2012.06.038 (  0) 0) |
| [14] |
XU L, HUANG H R, YANG L T. Combined application of NPK on yield quality of sugarcane applied through SSDI[J]. Sugar Tech, 2010, 12(2): 104-107. DOI:10.1007/s12355-010-0021-9 (  0) 0) |
| [15] |
刘永贤, 曾维宾, 熊柳梅, 等. 不同磷肥用量对桂中蔗区甘蔗生长性状与产量的影响[J]. 南方农业学报, 2012, 43(5): 634-636. DOI:10.3969/j:issn.2095-1191.2012.05.634 (  0) 0) |
| [16] |
许树宁, 方锋学, 唐仕云, 等. 不同施肥量对甘蔗产量和蔗糖分的影响[J]. 现代农业科技, 2012(19): 9-10. DOI:10.3969/j.issn.1007-5739.2012.19.001 (  0) 0) |
| [17] |
陈如凯, 张木清, 陆裔波. 干旱胁迫对甘蔗生理影响的研究[J]. 甘蔗, 1995, 2(1): 1-6. (  0) 0) |
| [18] |
杨建波, 诸葛少军, 黎海涛, 等. 干旱胁迫对甘蔗生长生理的影响及品种抗旱性评价[J]. 南方农业学报, 2012, 43(8): 1114-1120. DOI:10.3969/j:issn.2095-1191.2012.08.1114 (  0) 0) |
| [19] |
BATES L S, WALDREN R P, TEARE I D. Rapid determination of free proline for water-stress studies[J]. Plant Soil, 1973, 39(1): 205-207. DOI:10.1007/BF00018060 (  0) 0) |
| [20] |
KAVI KISHOR P B, HONG Z L, MIAO G H, et al. Overexpression of Δ1-pyrroline-5-carboxylate synthetase increases proline production and confers osmotolerance in transgenic plants[J]. Plant Physiol, 1995, 108(4): 1387-1394. DOI:10.1104/pp.108.4.1387 (  0) 0) |
| [21] |
黄诚梅. 甘蔗脯氨酸积累与△1-吡咯啉-5-羧酸合成酶(ScP5CS)基因克隆及转化研究[D]. 南宁: 广西大学, 2007: 17-18.
(  0) 0) |
| [22] |
KIM H R, RHO H W, PARK J W, et al. Assay of ornithine aminotransferase with ninhydrin[J]. Analytical Biochem, 1994, 223(2): 205-207. (  0) 0) |
| [23] |
李合生. 植物生理生化实验原理和技术[M]. 北京: 高等教育出版社, 2000, 164-165.
(  0) 0) |
| [24] |
LIVAK K J, SCHMITTGEN T D. Analysis of relative gene expression data using real-time quantitative PCR and the 2-ΔΔCT method[J]. Methods, 2001, 25(4): 402-408. DOI:10.1006/meth.2001.1262 (  0) 0) |
| [25] |
阙友雄, 许莉萍, 徐景升, 等. 甘蔗基因表达定量PCR分析中内参基因的选择[J]. 热带作物学报, 2009, 30(3): 274-278. DOI:10.3969/j.issn.1000-2561.2009.03.006 (  0) 0) |
| [26] |
IGARASHI Y, YOSHIBA Y, TAKESHITA T. Molecular cloning and characterization of a cDNA encoding proline transporter in rice[J]. Plant Cell Physiol, 2000, 41(6): 750-756. DOI:10.1093/pcp/41.6.750 (  0) 0) |
| [27] |
BRUGIEREA N, DUBOISB F, LIMAMIA A M. Glutamine synthetase in the phloem plays a major role in controlling proline production[J]. Plant Cell, 1999, 11(10): 1995-2012. DOI:10.1105/tpc.11.10.1995 (  0) 0) |
| [28] |
王庭璋, 胡望雄, 徐建红, 等. 植物基因组上游开放阅读框的挖掘方法及其翻译调控[J]. 中国农业科学, 2013, 46(16): 3314-3323. DOI:10.3864/j.issn.0578-1752.2013.16.002 (  0) 0) |
| [29] |
刘丽, 甘志军, 王宪泽. 植物氮代谢硝酸还原酶水平调控机制的研究进展[J]. 西北植物学报, 2004, 24(7): 1355-1361. DOI:10.3321/j.issn:1000-4025.2004.07.038 (  0) 0) |
| [30] |
谭彩霞, 郭静, 陈静, 等. 小麦籽粒淀粉合成酶基因表达与酶活性特征的研究[J]. 麦类作物学报, 2009, 29(1): 24-30. (  0) 0) |
| [31] |
VOCTBERG G S, SHARP R E. Growth of the maize primary root at low water potcntia:3:Role of increased proline deposition in osmotic adjustment[J]. Plant Physiol, 1991, 96(4): 1125-1130. DOI:10.1104/pp.96.4.1125 (  0) 0) |
| [32] |
SCHWACKE R, GRALLATH S, BRCITKREUZ K E, et al. LeProTl, a transproter for proline, glycine betaine and γ-amino butyric acid in tomato pollen[J]. The Plant Cell, 1999, 11(3): 377-391. (  0) 0) |
| [33] |
ROSA P, ROSARIO A, JUAN M R. Evaluation of the role of genes encoding for Δ1-pyrroline-5-carboxylate synthetase (P5CS) during drought stress in arbuscular mycorrhizal Glycine max and Lactuca sativa plants[J]. Physiol Mol Plant P, 2004, 65(4): 211-221. DOI:10.1016/j.pmpp.2005.02.003 (  0) 0) |
| [34] |
王丽媛, 丁国华, 黎莉. 脯氨酸代谢的研究进展[J]. 哈尔滨师范大学自然科学学报, 2010, 26(2): 84-89. DOI:10.3969/j.issn.1000-5617.2010.02.024 (  0) 0) |
| [35] |
曹芳, 魏永胜. 渗透胁迫下硝酸钾对烟草脯氨酸代谢途径的影响[J]. 西北农业学报, 2010, 19(9): 144-148. DOI:10.3969/j.issn.1004-1389.2010.09.029 (  0) 0) |
| [36] |
姜淑欣, 刘党校, 庞红喜, 等. PEG胁迫及复水对不同抗旱性小麦幼苗脯氨酸代谢关键酶活性的影响[J]. 西北植物学报, 2014, 34(8): 1581-1587. (  0) 0) |
| [37] |
CHOUDHARY N L, SAIRAM R K, TYAGI A. Expression of D1-pyrroline-5-carboxylate synthetase gene during drought in rice(Oryza sativa L.)[J]. Indian J Biochem Bio, 2005, 42(6): 366-370. (  0) 0) |
 2015, Vol. 36
2015, Vol. 36