2. 广东省微生物研究所/省部共建华南应用微生物国家重点实验室/广东省菌种保藏与应用重点实验室/广东省微生物应用新技术公共实验室,广东 广州 510070
2. Guangdong Institute of Microbiology/ State Key Laboratory of Applied Microbiology Southern China/Guangdong Provincial Key Laboratory of Microbial Culture Collection and Application/ Guangdong Open Laboratory of Applied Microbiology, Guangzhou 510070, China
耐甲氧西林金黄色葡萄球菌(Methicillin-resistant Staphylococcus aureus,MRSA)因能引起致死性感染,且耐药范围广、耐药性强,已给人类带来了重大危害[1]。MRSA本在医院重症监护室和外科手术室中泛滥,但据最近报道,其已从医院扩散到社区人群和食用动物之中[2-3]。目前,临床治疗MRSA感染的抗生素十分有限,仅有万古霉素和利奈唑胺[4]。但新的抗万古霉素和利奈唑胺的MRSA已经出现[5]。因此,寻找和开发高效抑制MRSA的抗生素刻不容缓。
微生物源天然产物一直以来都是新抗生素最重要的来源之一[6-7]。随着细菌耐药性的日趋严重,MRSA等耐药菌的耐药机制逐步多元化,交叉耐药性也日趋盛行,因此更需要一些结构新颖、作用方式独特的活性产物来有效抑制耐药菌[8]。然而,传统的抗生素产生菌正面临着过度开发的困境,从其中筛选新的化合物已经越来越困难[9]。为摆脱困境,药源微生物的开发逐渐转向特殊生活环境甚至极端生活环境微生物以及新的药源微生物[10-11]。
近50年来,被开发作新的抗生素产生菌的只有蓝细菌和黏细菌。尽管黏细菌生物活性物质研究起步较晚,但目前已从黏细菌中发现了100余种全新结构的次级代谢产物和600多种新的结构衍生物,且具有结构新颖、种类多样、活性良好、作用机制复杂等特点[12-14]。黏细菌已成为仅次于放线菌的第二大抗生素产生细菌,得到了越来越多的关注[15]。
在之前的研究中,我们筛选到1株黏细菌GIM1.813,其次级代谢产物对金黄色葡萄球菌、粪肠球菌等革兰阳性菌有显著的抑制活性,同时对黑曲霉菌也有一定的抑制作用(待发表)。重要的是,该菌能产生高效抑制MRSA的天然活性产物,仅其发酵液的抗MRSA活性就同高质量浓度(100 μg·mL-1)的万古霉素活性相近,或更胜之。另外,该菌产生的抗MRSA活性物质还具有良好的稳定性。高效液相色谱(HPLC)分析发现,该菌株发酵液中至少含有2种高效抑制MRSA的活性天然产物,其中之一对MRSA和甲氧西林敏感金黄色葡萄球菌(Methicillin-sensitive Staphylococcus aureus, MSSA)具有相近的抑制活性,因此该活性天然产物可能具有独特的作用机制,能绕过目前MRSA的抗性产生抑制活性。黏细菌GIM1.813发酵液中分离到的活性物质,极有可能是一种新结构的化合物。总之,黏细菌GIM1.813在开发抗MRSA的抗生素方面具有重要的研究价值,有必要对其开展基础研究。
黏细菌的基础研究和技术开发长期滞后,限制了这一重要的资源微生物的开发利用[16]。例如,目前黏细菌的生理生化特征仍不清晰,液体发酵培养也存在困难。为充分了解这株有重要应用潜力的黏细菌,本文对GIM1.813进行了鉴定,测定了相关生理生化数据;同时开展发酵条件的优化,以提高抗MRSA活性物质的产量,并探讨培养基不同组分对GIM1.813分泌活性物质的影响。本文将为菌株GIM1.813的进一步研究及其大规模发酵和活性化合物的纯化鉴定提供基础信息。
1 材料与方法 1.1 材料 1.1.1 菌株金黄色葡萄球菌S. aureus 11(MRSA)由华南农业大学兽医学院分离并提供。金黄色葡萄球菌ATCC6538(MSSA)由广东省微生物菌种保藏中心提供。黏细菌菌株GIM1.813由广东省微生物研究所分离并提供。
1.1.2 培养基金黄色葡萄球菌使用LB培养基(蛋白胨10.0 g·L-1,NaCl 10.0 g·L-1,酵母提取物5.0 g·L-1,pH 7.0)培养。黏细菌GIM1.813培养和发酵所用的培养基见表 1[17-20]。对应的固态培养基是在上述配方基础上添加15 g·L-1的琼脂。
|
|
表 1 黏细菌培养基组分 Table 1 Ingredients of myxobacterial mediums |
使用体视显微镜、扫描电镜对黏细菌GIM1.813的菌落、子实体、营养细胞和黏孢子的形态、大小进行观察。而后根据文献[21]中黏细菌的形态描述和分类标准对黏细菌GIM1.813进行分类鉴定。
1.2.2 16S rRNA基因的分子生物学鉴定提取黏细菌GIM1.813的总DNA,使用16S rRNA基因引物27F和1492R进行PCR扩增[22]。PCR产物送往英骏测序公司(上海)进行测序。将有效序列在NCBI数据库中进行比对。收集相似性较高的序列,使用MEGA5.5,运用邻接法构建系统发育树。
1.2.3 生理生化鉴定按照文献[23]对黏细菌GIM1.813进行刚果红、脲酶、纤维素分解、淀粉水解、蔗糖利用、降解酪素、脂酶(吐温80)、明胶液化、七叶苷利用、硝酸盐还原、氧化酶、过氧化氢酶、耐盐以及生长pH、生长温度和抗生素耐受性等各项生理生化指标测定。
1.2.4 基因组DNA G+C含量及醌型的测定采用Mesbah等[24]描述的熔点法(Tm值法)测定黏细菌GIM1.813的基因组DNA G+C含量。参照Collins等[25]的方法,使用HPLC分析黏细菌GIM1.813的醌型。
1.3 打孔法测定抑菌活性使用优化过的打孔法测定发酵液等产物对金黄色葡萄球菌的抑制活性[26]。将菌株金黄色葡萄球菌11(MRSA)、金黄色葡萄球菌ATCC6538(MSSA)接种到LB液体培养基中,37 ℃、200 r·min-1条件下培养至对数期,按1:100的比例接种到LB琼脂培养基(50 ℃,液体状态)中,然后每20 mL添加到1个无菌平皿中,晾干备用。需测活性的发酵液均经0.22 μm滤膜过滤除菌。用9 mm打孔器在制备好的平皿中打孔,然后将100 μL发酵液注入到孔中。阳性对照平板的孔中加入100 μL氨苄西林(Ampicillin,100 μg·mL-1),阴性对照平板的孔中加入100 μL VY/2培养基。将平皿置于37 ℃恒温培养箱内培养18~24 h,观察记录抑菌圈直径(Inhibitory zone diameter,IZD)。每组试验重复3次。
1.4 发酵条件的优化 1.4.1 发酵培养基的选择将黏细菌GIM1.813在VY/2固体培养基上活化,培养5 d后接入VY/2液体培养基中,28 ℃、150 r·min-1条件下培养制成种子液。将种龄3 d的种子液按照体积分数10%的接种量分别接种至VY/2、Improved-VY/2(IVY/2)、CY、MD1、SSG、BAI和SMG 7种发酵液中(瓶装体积:250 mL锥形瓶装100 mL培养基),150 r·min-1、28 ℃条件下发酵7 d。然后用打孔法测定各种发酵液的抗菌活性。
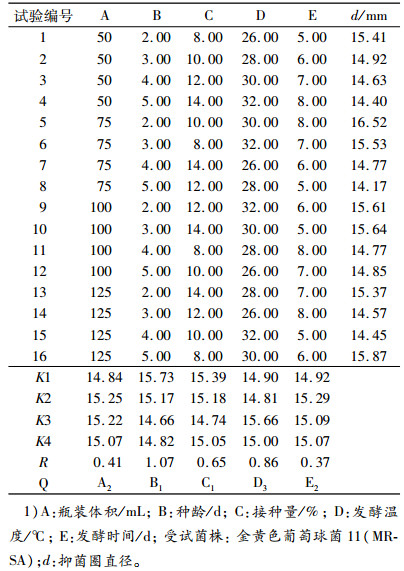
1.4.2 发酵培养基优化选用正交法,对上一步筛选出的最佳发酵培养基IVY/2的5个因素:鲜酵母、CaCl2·2H2O、MgSO4·7H2O、维生素B12(VB12)和pH,选用5因素5水平L25(55)正交表,开展发酵培养基优化试验(250 mL锥形瓶装100 mL发酵液)。试验设计见表 2。发酵完成后,用打孔法测定各配方组合下发酵液的抗菌活性。最后使用软件MINITAB 16对数据进行分析。
|
|
表 2 发酵培养基主要因素的正交试验因素及水平1) Table 2 Factors and levels of orthogonal test for main culture medium components |
以IVY/2培养基为发酵培养基,选用正交法,根据发酵培养条件(瓶装体积、种龄、接种量、发酵温度、发酵时间),选用5因素4水平L16(45)正交表,开展发酵培养条件的优化试验。试验设计见表 3。发酵完成后,用打孔法测定各条件组合下发酵液的抗菌活性。最后使用软件MINITAB 16对数据进行分析。
|
|
表 3 发酵培养条件主要因素的正交试验因素及水平1) Table 3 Factors and levels of orthogonal test for main conditions of fermentation medium |
分别使用优化前和优化后的培养基及发酵条件,对黏细菌GIM1.813进行小规模发酵。发酵完成后,4 000 r·min-1离心收集发酵液,用打孔法测定2种条件下产生的发酵液的抑菌活性。对优化前后得到的发酵液用等体积的乙酸乙酯萃取并浓缩,然后进行HPLC分析,并对比分析结果。
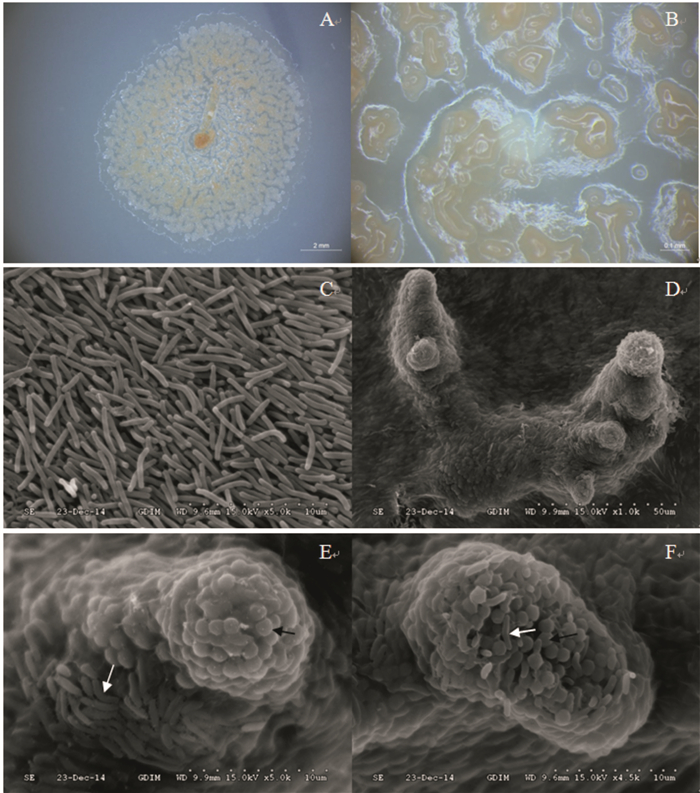
2 结果与分析 2.1 黏细菌菌株GIM1.813的鉴定 2.1.1 形态学鉴定在体视显微镜下,GIM1.813的菌落呈薄膜状扩散,有明显的辐射线,菌落边缘有火焰状突出,子实体均匀分布(图 1A);其子实体微呈褐色,致密,具有光泽,表面光滑,无明显珊瑚状分枝(图 1B)。在扫描电镜下,营养细胞呈细长杆状,末端变尖,雪茄状,宽0.4 ~0.7 μm,长3~7 μm(图 1C);子实体有柄,头部团聚成球形,黏孢子呈规则球形,直径1.5~2.0 μm(图 1D、1E、1F)。根据文献[21]中对黏细菌形态鉴定的描述,笔者推测菌株GIM1.813为弱小珊瑚球菌Corallococcus exiguus。
|
图 1 黏细菌GIM1.813的形态结构 Figure 1 Morphological structure of myxobacteria strain GIM1.813 A:菌落,B、D、E和F:子实体,C:营养细胞;A和B在体式显微镜下拍摄,C、D、E和F在扫描电镜下拍摄;黑色箭头所指为黏孢子,白色箭头所指为还未转化为黏孢子的营养细胞。 |
黏细菌GIM1.813的16S rRNA基因核苷酸序列大小为1 414 bp(Accession No. KP747688)。BLAST结果显示,GIM1.813的16S rRNA基因与模式菌株弱小珊瑚球菌DSM 14696T(NR 115864.1)的相似性最高(99.93%)。从系统发育树(图 2)中可以看出,菌株GIM1.813与菌株DSM 14696 T在同一进化分支上。因此,菌株GIM1.813被鉴定为弱小珊瑚球菌。

|
图 2 基于16S rRNA基因序列的系统发育树 Figure 2 Phylogentic tree based on 16S rRNA genes 脱硫脱硫弧菌 Desulfovibrio desulfuricans ATCC 27774T和大肠埃希菌Escherichia coli ATCC 11775T为外参菌株。 |
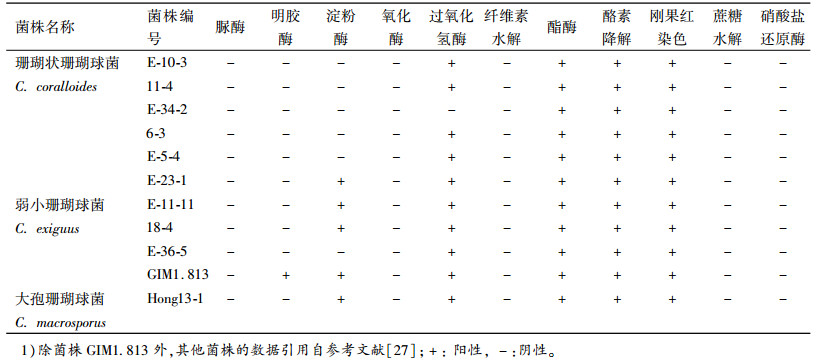
目前黏细菌菌种鉴定主要依据为文献[21],但其中并未列举珊瑚球菌属的理化特征。各参考文献中,也没有给出珊瑚球菌属的3个模式种的理化数据。除菌株GIM1.813之外,广东省微生物研究所之前还测定了6株珊瑚状珊瑚球菌、3株弱小珊瑚球菌和1株大孢珊瑚球菌的理化数据[27](表 4)。菌株GIM1.813能产生酯酶、降解酪素、吸附刚果红、利用明胶和淀粉、产生过氧化氢酶,不能利用尿素、纤维素和蔗糖,不产生氧化酶和不能还原硝酸盐。除了能液化明胶外,与其他3株弱小珊瑚球菌有较好的相似性,与其他2个属的7株珊瑚球菌也比较接近。
|
|
表 4 11株黏球菌的生理生化特征1) Table 4 Metabolism-related enzymes of 11 Corallococcus strains |
笔者还检测了菌株GIM1.813在不同条件下的生长情况(表 5)。该菌株在NaCl质量浓度大于10 g·L-1的VY/2培养基中不生长;在pH5~10以及10~37 ℃环境中均能生长;最适pH为7.0,最适温度为30 ℃;在抗生素耐受性试验中,GIM1.813能够耐受25 μg·mL-1的氯霉素,10 μg·mL-1的庆大霉素,40 μg·mL-1的氨苄西林和10 μg·mL-1的卡那霉素,但不耐受10 μg·mL-1的四环素。
|
|
表 5 菌株GIM1.813在不同条件下的生长情况 Table 5 Growth situation of GIM1.813 under different conditions |
黏细菌GIM1.813的基因组DNA G+C含量为72.14%。其醌型主要有2种类型,含量最多的是MK-7(占81.26%),其次为MK-9(占15.97%)。根据文献[21],珊瑚状珊瑚球菌模式菌株DSM2259T的基因组DNA G+C含量为68%,而弱小珊瑚球菌DSM14696T和大孢珊瑚球菌DSM14697T的基因组DNA G+C含量均尚未测定。这3个菌种的参考醌型数据目前也未知。
一般认为,基因组DNA G+C含量的差异在同种内菌株应不超过5%,而超过10%可考虑是不同属。而菌株GIM1.813基因组DNA G+C含量为72.14%,与模式菌株珊瑚状珊瑚球菌DSM2259T的68%差异在5%以内,同鉴定结果相一致。
2.2 发酵条件的优化 2.2.1 发酵培养基的选择黏细菌GIM1.813在7种发酵培养基中均生长良好,但是其发酵液的抗金黄色葡萄球菌活性差别明显(图 3)。除CY培养基外,菌株GIM1.813在其他6种培养基中培养时,其发酵液均有一定的抗菌活性;在VY/2、IYV/2、SMG、SSG培养基中培养的发酵液均有显著的抗MRSA活性。菌株GIM1.813在IVY/2培养基中培养的发酵液抗MSSA和抗MRSA活性均最强。

|
图 3 在不同培养基中黏细菌GIM1.813发酵液对金黄色葡萄球菌的抑菌圈直径(d抑菌圈) Figure 3 Inhibition zone diameter against Staphylococcus aureus in different fermentation mediums produced by myxobacteria GIM1.813 打孔直径为9 mm,d抑菌圈=9 mm表示无抑菌活性。 |
根据结果中极差(R)的大小(表 6),各因子对发酵结果影响顺序为:pH>MgSO4·7H2O>CaCl2·2H2O>VB12>鲜酵母。由K值可以得到发酵培养基各组分最佳组合为A5B4C4D4E2,即:鲜酵母7 g·L-1,CaCl2·2H2O 1.2 g·L-1,MgSO4·7H2O 1.2 g·L-1,VB120.6 mg·L-1,pH 6.7。
|
|
表 6 发酵培养基正交优化结果1) Table 6 Orthogonal experiments of culture medium |
根据结果中极差(R)的大小(表 7),各因子对发酵结果影响顺序为:种龄>发酵温度>接种量>瓶装体积>发酵时间。由K值可以得到发酵各培养条件最佳组合为A2B1C1D3E2,即:瓶装体积75 mL,种龄2 d,接种量8%,发酵温度30 ℃,发酵时间6 d。
|
|
表 7 发酵培养条件正交优化结果1) Table 7 Orthogonal experiments of culture conditions |
发酵条件优化前后摇瓶中菌株形态对比:发酵条件优化前,菌体生长速度较慢,容易聚集成大的球状团聚体,且有菌体悬浮在发酵液中,导致发酵液较浑浊,需要离心才能将菌体和发酵液分离;发酵条件优化后,菌体聚集程度大大减轻,大都呈较小的絮状,发酵液较澄清,只需短时间静置沉淀、过滤即可将菌体和发酵液分离。总之,优化后菌株生长情况明显改善。
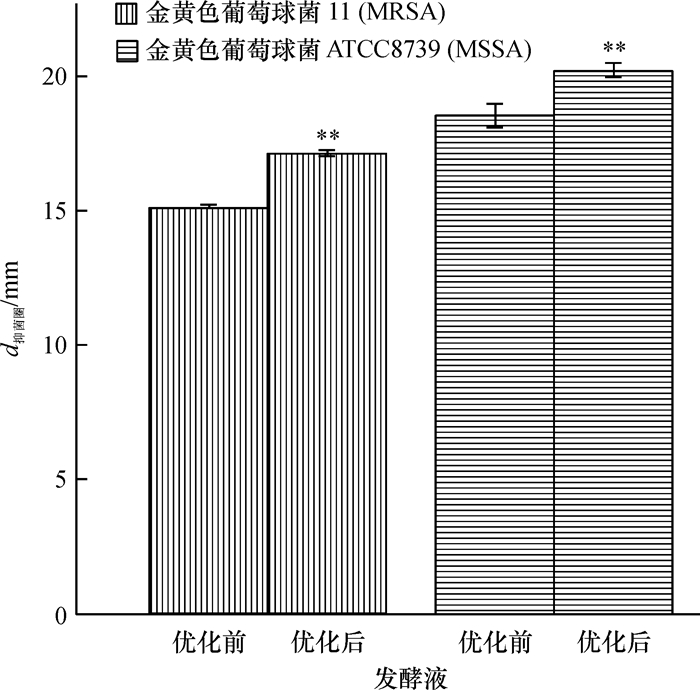
发酵条件优化前后代谢产物对比:优化后,发酵液抗MRSA的活性较优化前提升了49.12%(t检验,P<0.01),抗MSSA的活性较优化前提升了27.73%(t检验,P<0.01)(图 4),提升均非常显著。HPLC分析表明(图 5),优化前后发酵液中分离峰数量从82个减少到64个(杂峰数量减少了21.95%);而活性试验表明,抗金黄色葡萄球菌活性物质分布在图 5中的A、B、C、D 4段,优化后,这4段组分占代谢产物总量的比例分别提高了395.65%、118.87%、426.67%和202.88%。上述结果表明,本文发酵条件优化试验对提高黏细菌GIM1.813抗金黄色葡萄球菌活性成分的浓度和纯度都有明显效果。
|
图 4 优化前后发酵液抗金黄色葡萄球菌的活性对比 Figure 4 Anti- Staphylococcus aureus activities of fermentation broths before and after optimization 打孔直径为9 mm,d抑菌圈=9 mm表明无抑菌活性;**表示同一图例中两组数据差异极显著(P<0.01,t检验)。 |
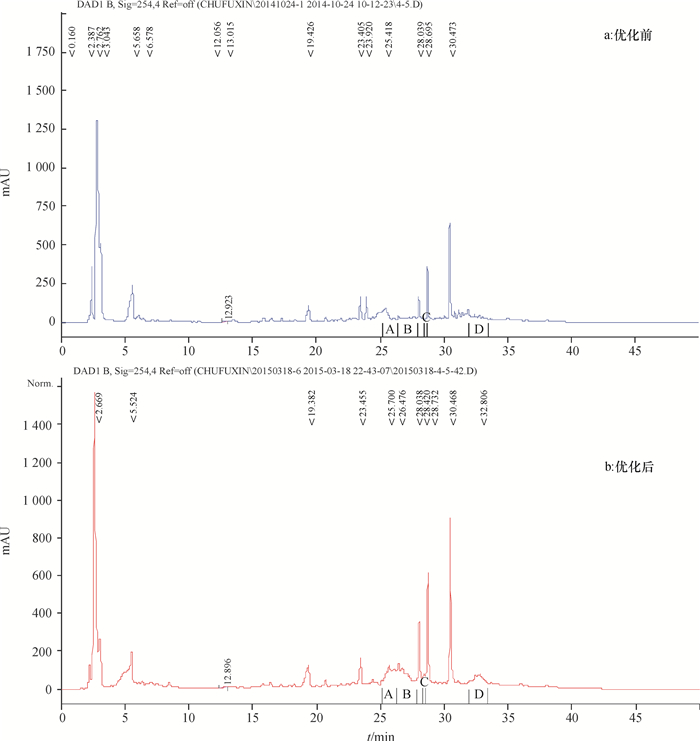
|
图 5 优化前后发酵液粗提物HPLC结果对比 Figure 5 HPLC analysis of crude extracts from fermentation broths before and after optimization |
近50年来,仅蓝细菌和黏细菌这2类微生物被确认为新的抗生素产生菌。一般说来,拓展一种新的抗生素产生菌至少需要10年以上的研究[28]。然而黏细菌的基础研究、分离纯化、发酵培养等相对滞后,限制了这一重要资源微生物的开发利用。例如,目前对于黏细菌仍未建立起一套完整、标准的生理生化分类指标。黏细菌的分类仍主要依靠形态学特征[29]。本文经形态学和16S rRNA基因系统发育分析,将黏细菌GIM1.813鉴定为弱小珊瑚球菌。本文所测定理化数据,对菌株GIM1.813的后期发酵条件优化和开发利用有重要价值。目前在菌种鉴定方面,珊瑚球菌属的3个模式种都没有生理生化性质数据和醌型数据,弱小珊瑚球菌和大孢珊瑚球菌还缺乏基因组DNA G+C含量数据[21]。因此本文菌种鉴定部分的结果为将来珊瑚球菌属的基础研究、分类鉴定等提供一定参考。
目前,黏细菌的发酵培养尚存在诸多困难,例如生长速度慢、菌体密度低、易聚集成团、易发生污染及产生的活性物质浓度很低等[16]。本文通过发酵条件的优化,对存在的问题做出了明显的改善,使GIM1.813液体发酵培养时,菌体密度提高,聚集成团现象减少,且显著地提高了GIM1.813分泌抗菌活性物质的能力。一方面对后续大规模发酵生产和纯化鉴定该活性物质打下了基础;另一方面也加深了对黏细菌发酵的认识:(1)VY/2培养基中含有鲜酵母,其营养成分复杂、浓度低且释放缓慢,几乎适合于各种黏细菌的生长和短期保存[30]。本文中黏细菌GIM1.813能利用VY/2培养基,生长良好且能分泌高效抗菌活性物质。(2)Shimkets等[30]曾报道高浓度的Mg2+对黏细菌的生长至关重要。本文发现,添加了Mg2+的VY/2培养基(即IVY/2培养基)能够显著提高该菌发酵液的抗菌活性,特别是抗MRSA活性;其他5种不含鲜酵母的培养基中,只有CY培养基不含Mg2+,结果也只有CY的发酵液没有抗金黄色葡萄球菌活性;在发酵培养基正交优化试验中,MgSO4·7H2O对发酵活性的影响也排在其他组分前。总之,本文将Mg2+与黏细菌产生天然活性物质的能力联系了起来。(3)VB12对黏细菌的生长发育同样十分重要[31],这或许就是黏细菌GIM1.183在添加了VB12的VY/2和IVY/2培养基中分泌更多活性物质的原因。(4)对比除了VY/2和IVY/2之外的5种不含鲜酵母的发酵液,我们发现GIM1.813在唯一没有淀粉的CY培养基中不能分泌活性物质;在含有水溶性淀粉的培养基中,主要分泌抗MSSA活性物质;而在含有马铃薯淀粉及EDTA-Na-Fe组分的培养基中,才明显分泌抗MRSA活性物质。在理化试验中,我们已经发现黏细菌GIM1.813可以以淀粉为碳源,本文揭示了淀粉及其类型可能影响黏细菌产生活性物质的能力。
上述讨论揭示了GIM1.813在发酵过程中基于不同的营养成分产生不同的活性物质,即GIM1.813可以产生2种以上的抗菌活性物质:一种只对MSSA有活性,一种有突出的抗MRSA活性,这也进一步验证了HPLC分析的结果。培养基中营养成分如鲜酵母、Mg2+和淀粉与GIM1.813在液体培养时产生活性物质具体关系需要进一步的研究,这可能成为开发针对GIM1.813乃至其他黏细菌的高效发酵培养基的重要依据。
目前,黏细菌的次级代谢产物研究主要集中在堆囊菌属Sorangium、黏球菌属Myxococcus和立杆黏细菌属Chondromyces这3个属[32]。珊瑚球菌属Corallococcus占目前所有分离得到的黏细菌菌株比例的23.1%,但从中分离到的次生代谢产物却仅占1.7%[33]。近来,随着对珊瑚球菌研究力度的增强,从中分离出一些新的具有活性的化合物[34-36]。这表明,珊瑚球菌属在天然产物开发方面仍有很大的研究空间。本文对GIM1.813进行了鉴定,为珊瑚球菌属的基础研究提供了新的数据;同时对其发酵培养进行了优化,为下一步纯化鉴定和大规模发酵生产该抗MRSA活性物质奠定了基础,也为珊瑚球菌属菌株的发酵,提供帮助和启发。
| [1] |
KLEVENS R M, MORRISON M A, NADLE J, et al. Invasive methicillin-resistant Staphylococcus aureus infections in the United States[J]. JAMA, 2007, 298(15): 1763-1771. DOI:10.1001/jama.298.15.1763 (  0) 0) |
| [2] |
FRAZEE B W, LYNN J, CHARLEBOIS E D, et al. High prevalence of methicillin-resistant Staphylococcus aureus in emergency department skin and soft tissue infections[J]. Ann Emerg Med, 2005, 45(3): 311-320. DOI:10.1016/j.annemergmed.2004.10.011 (  0) 0) |
| [3] |
VANDERHAEGHEN W, HERMANS K, HAESEBROUCK F, et al. Methicillin-resistant Staphylococcus aureus (MRSA) in food production animals[J]. Epidemiol Infect, 2010, 138(5): 606-625. DOI:10.1017/S0950268809991567 (  0) 0) |
| [4] |
FUSCO N M, TOUSSAINT K A, PRESCOTT W A. Antibiotic management of methicillin-resistant Staphylococcus aureus-associated acute pulmonary exacerbations in cystic fibrosis[J]. Ann Pharmacother, 2015, 49(4): 458-468. DOI:10.1177/1060028014567526 (  0) 0) |
| [5] |
GEORGE S, ROBERT C M. Increasing antibiotic resistance among methicillin-resistant Staphylococcus aureusstrains[J]. Clin Infect Dis, 2008, 46(5): S360-S367. (  0) 0) |
| [6] |
NEWMAN D J, CRAGG G M. Natural products as sources of new drugs over the 30 years from 1981 to 2010[J]. J Nat Prod, 2012, 75(3): 311-335. DOI:10.1021/np200906s (  0) 0) |
| [7] |
SINGH S B, BARRETT J F. Empirical antibacterial drug discovery:foundation in natural products[J]. Biochem Pharmacol, 2006, 71(7): 1006-1015. DOI:10.1016/j.bcp.2005.12.016 (  0) 0) |
| [8] |
张哲峰. 多重耐药菌的监控与新抗生素研发[J]. 中国药学杂志, 2014, 49(14): 1268-1273. (  0) 0) |
| [9] |
BERDY J. Bioactive microbial metabolites[J]. J Antibiot, 2005, 58(1): 1-26. DOI:10.1038/ja.2005.1 (  0) 0) |
| [10] |
刘少伟, 韩晓艳, 刘佳萌, 等. 塔克拉玛干沙漠来源抗MRSA新抗生素—和田霉素A-D[C]//中国药学会抗生素专业委员会. 第十二届全国抗生素学术会议论文集. 成都. 出版地不详: 出版者不详, 2013: 76-86.
(  0) 0) |
| [11] |
武英, 王辂. 开发微生物来源天然产物的新技术[J]. 国外医药(抗生素分册), 2010, 31(1): 1-6. (  0) 0) |
| [12] |
WEISSMAN KJ, MVLLER R. Myxobacterial secondary metabolites: Bioactivities and modes-of-action[J]. Nat Prod Rep, 2010, 27(9): 1276-1295. DOI:10.1039/c001260m (  0) 0) |
| [13] |
李艳利, 张荫雷, 刘迎, 等. 一株新粘细菌生物学性质的研究[J]. 微生物学通报, 2008, 35(23): 1888-1891. (  0) 0) |
| [14] |
王海英, 张利平. 粘细菌:一类重要的微生物资源[J]. 微生物学通报, 2003, 30(2): 115-116. DOI:10.3969/j.issn.0253-2654.2003.02.029 (  0) 0) |
| [15] |
SCH BERLE T F, LOHR F, SCHMITZ A, et al. Antibiotics from myxobacteria[J]. Nat Prod Rep, 2014, 31: 953-972. DOI:10.1039/c4np00011k (  0) 0) |
| [16] |
GERTH K, PRADELLA S, PERLOVA O, et al. Myxobacteria: Proficient producers of novel natural products with various biological activities:past and future biotechnological aspects with the focus on the genus Sorangium[J]. J Biotechnol, 2003, 106(2): 233-253. (  0) 0) |
| [17] |
GASPARI F, PAITAN Y, MAININI M, et al. Myxobacteria isolated in Israel as potential source of new anti-infectives[J]. J Appl Microbiol, 2005, 98(2): 429-439. DOI:10.1111/jam.2005.98.issue-2 (  0) 0) |
| [18] |
WANG D, YUAN J, TAO W. Identification of a novel antibiotic from myxobacterium Stigmatella eracta WXNXJ-B and evaluation of its antitumor effects in-vitro[J]. Iran J Pharmaceut Res, 2014, 13(1): 171. (  0) 0) |
| [19] |
GUO W J, TAO W Y, XU Z H, et al. Directed-screening of myxobacteria producing high bioactive antitumor metabolites[J]. Nat Pro Res Dev, 2007, 19(6): 1032-1036. (  0) 0) |
| [20] |
施晓琼, 许强芝, 刘小宇, 等. 六种粘细菌095b06次生代谢产物的分离、鉴定及初步生物学活性研究[J]. 第二军医大学学报, 2007, 28(3): 266-271. DOI:10.3321/j.issn:0258-879X.2007.03.008 (  0) 0) |
| [21] |
GARRITY G M. Bergey's manual of systematic bacteriology[M]. Berlin: Springer, 2006, 1079-1082.
(  0) 0) |
| [22] |
BRUNEL B, GIVAUDAN A, LANOIS A, et al. Fast and accurate identification of Xenorhabdus and Photorhabdus species by restriction analysis of PCR-amplified 16S rRNA genes[J]. Appl Environ Microb, 1997, 63(2): 574-580. (  0) 0) |
| [23] |
东秀珠, 蔡妙英. 常见细菌系统鉴定手册[M]. 北京: 科学出版社, 2001, 370-398.
(  0) 0) |
| [24] |
MESBAH M, PREMACHANDRAN U, WHITMAN W B. Precise measurement of the G+C content of deoxyribonucleic acid by high-performance liquid chromatography[J]. Int J Syst Bacteriol, 1989, 39(2): 159-167. DOI:10.1099/00207713-39-2-159 (  0) 0) |
| [25] |
COLLINS M, PIROUZ T, GOODFELLOW M, et al. Distribution of menaquinones in actinomycetes and corynebacteria[J]. J Gen Microbiol, 1977, 100(2): 221-230. DOI:10.1099/00221287-100-2-221 (  0) 0) |
| [26] |
FYHRQUIST P, MWASUMBI L, HAGGSTRÖM C A, et al. Ethnobotanical and antimicrobial investigation on some species of Terminalia and Combretum(Combretaceae) growing in Tanzania[J]. J Ethnopharmacol, 2002, 79(2): 169-177. DOI:10.1016/S0378-8741(01)00375-0 (  0) 0) |
| [27] |
原红娟. 热带亚热带原始森林粘细菌的多样性研究[D]. 广州: 华南农业大学, 2014.
(  0) 0) |
| [28] |
REICHENBACH H. Myxobacteria, producers of novel bioactive substances[J]. J Ind Microbiol Biotechnol, 2001, 27(3): 149-156. DOI:10.1038/sj.jim.7000025 (  0) 0) |
| [29] |
李越中, 李健, 周璐, 等. 我国粘细菌(Myxobacteria)资源的分离与鉴定[J]. 微生物学报, 2000, 40(6): 652-656. DOI:10.3321/j.issn:0001-6209.2000.06.015 (  0) 0) |
| [30] |
SHIMKETS L J, DWORKIN M, REICHENBACH H. The prokaryotes[M]. Berlin: Springer, 2006, 31-115.
(  0) 0) |
| [31] |
BRETSCHER A P, KAISER D. Nutrition of Myxococcus xanthus, a fruiting myxobacterium[J]. J Bacteriol, 1978, 133(2): 763-768. (  0) 0) |
| [32] |
王大红. 粘细菌Stigmatella WXNXJ-B产生新型抗肿瘤抗生素的研究[D]. 无锡: 江南大学, 2010.
(  0) 0) |
| [33] |
GERTH K, IRSCHIK H, JANSEN R, et al. Myxobacteria-the word is spreading [J]. [EB/OL]. [2015-04-21]. http://www.naturstoff-forschung.info/nafo_media/13+myxobacteria.pdf.
(  0) 0) |
| [34] |
胡玮, 李越中, 李曦, 等. 珊瑚状珊瑚球菌Cc9736抗肿瘤活性组分的分离纯化[J]. 中国抗生素杂志, 2000, 25(4): 309-311. DOI:10.3969/j.issn.1001-8689.2000.04.021 (  0) 0) |
| [35] |
鞠培殿. Corallococcus coralloides 085B04次级代谢产物的分离与结构表征[D]. 济南: 山东轻工业学院, 2010.
(  0) 0) |
| [36] |
李健, 郭新征, 李越中, 等. 具有抑瘤活性的粘细菌珊瑚状珊瑚球菌Cc9736发酵产物的初步研究[J]. 中国抗生素杂志, 1999, 24(4): 308-309. (  0) 0) |
 2016, Vol. 37
2016, Vol. 37