氟虫腈是法国罗纳–普朗克公司1987年开发研制的一种高效、广谱的芳基吡唑类杀虫剂,该药结构新颖、作用机理独特、活性高,开发应用前景十分广阔[1-2]。氟虫腈对害虫以胃毒作用为主,兼有触杀和一定的内吸作用,作用于γ–氨基丁酸(GABA)受体,阻断氯离子通道,进而破坏中枢神经系统内信号传导的第2代杀虫剂,与已有其他类杀虫剂无交互抗性,主要用于防治鳞翅目和直翅目的害虫以及土壤中的鞘翅目幼虫[3-4]。
在我国氟虫腈大面积用于水稻害虫的防治,但环境毒理学研究发现,其应用具有潜在风险:它具有慢性神经毒性,对甲壳类水生生物和蜜蜂高毒,并且在环境中代谢缓慢,易在生物体内富集[5-6]。鉴于以上风险,从2009年起,除部分旱田种子包衣剂及卫生用途外,氟虫腈在我国其他领域均不可使用。因而,对以氟虫腈为代表的芳基吡唑类杀虫剂进行结构改造,在维持或提高其防效的同时改善其不足之处,显得尤为重要。近年来,世界各大农药公司对氟虫腈结构的优化改造,进行了不断地开发研究,如原万安特(现拜耳)公司研发了Vaniliprole、乙硫虫腈和乙酰虫腈等一系列新型芳基吡唑类杀虫剂。同时,日本农药公司和我国大连瑞泽农药股份有限公司在此基础上开发了Pyriprole、Pyrafluprole和丁烯氟虫腈,其对水稻、蔬菜等作物上的害虫显现出与氟虫腈同等效力,是很有前景的杀虫杀螨剂[7-11]。基于农用化学品创制中常用的中间体衍生化策略[12],我们开展了对以氟虫腈为代表的芳基吡唑类化合物的衍生改造,以寻找作用于昆虫中枢神经系统的新型活性化合物。本研究以氟虫腈【5–氨基–3–氰基–1–(2, 6–二氯–4–三氟甲基苯基)–4–三氟甲基亚磺酰基吡唑】为原料,分2步进行酰胺脲化衍生,合成了6个新型芳基吡唑脲类化合物,并通过MS、1H NMR和13C NMR等方法,对所合成的新型化合物进行了结构表征。
昆虫电生理技术是进行深入药剂毒理学研究,特别是分子水平作用机制研究主要的试验技术,尤其是与计算机联用后,不仅可以很好地模拟神经的各种兴奋和传导特性,而且能定量描述杀虫剂的作用机理,从而把杀虫剂毒理学研究提高到细胞水平和分子水平。电生理技术具有快速灵敏、用虫量少、所需化合物微量等特点,是对活性物质进行定性检测的有效手段[13-14]。本研究利用电生理技术筛选出具有良好生物活性并对昆虫中枢神经系统毒性作用方式不同的新型衍生物,以期为新杀虫剂的开发提供实践经验与理论指导。
1 材料与方法 1.1 试验仪器和试剂Bruker–600核磁共振仪(瑞士Bruker公司);Bruker maXis 4G ESI–Q–TOF质谱仪(德国Bruker Daltonics公司);1702–MPS型万分之一电子天平(德国Srrtorius Gmbh Gottingen公司);X–6型显微熔点测定仪(北京中仪博腾公司);GF–254高效薄层层析板(青岛海洋化工厂);BX51WI正置固定载物台显微镜(Olympus, Lehigh Valley, PA);Multiclamp700B放大器(Molecular Devices, Foster City, CA);Digital 1440A D–A转换器(Molecular Devices, Foster City, CA)。
本试验所用试剂及溶剂均为市售分析纯,必要时按常规方法干燥。
1.2 供试昆虫小菜蛾Plutella xylostella 3龄幼虫,华南农业大学天然农药与化学生物学教育部重点实验室养虫室提供。
1.3 方法 1.3.1 目标化合物的合成与结构表征目标化合物的合成路线如图1所示。以氟虫腈为原料,先后经过酰胺化、氨化两步反应合成目标化合物。
将氟虫腈 (4.37 g, 10 mmol) 置入100 mL烧瓶中,加入50 mL丙酮充分溶解,冰浴条件下加入氢氧化钾 (1.68 g,30 mmol),然后逐滴加入氯甲酸苯酯 (1.88 g,12 mmol),0℃条件下反应1 h,室温下反应过夜。将反应后的溶液加硅藻土后抽滤、蒸干。溶于经金属钠除水干燥的四氢呋喃(THF)中,加入DBU (1.5 g,1 mmol)、烃基胺 (12 mmol),65℃反应过夜。
反应完毕后,将反应液减压浓缩,然后加入50 mL冰水,再用50 mL乙酸乙酯萃取3次,有机相用饱和食盐水水洗,无水硫酸钠干燥,过滤、减压浓缩,硅胶色谱柱层析纯化所得固体即为目标产物。目标产物结构经1H NMR和13C NMR鉴定,并经MS确认。

|
图 1 目标化合物合成路线 Figure 1 Synthetic routes of target compounds |
采用浸叶法检测化合物的杀虫活性[15]。将测试样品用二甲基亚砜(DMSO)配制成10 000 mg·L–1的母液,然后取此母液加入到含有0.1%(φ)吐温–80的脱氯自来水中,配制成所需浓度梯度的药液。将面积大小一致的洁净新鲜甘蓝Brassica oleracea叶片浸入100 mg·L–1的药液中5 s,取出自然晾干后放入垫有保湿滤纸的培养皿中,选取3龄小菜蛾10只放于培养皿中,重复3组,置于养虫室内观察;另设含有1%(φ)DMSO和0.1%(φ)吐温–80的脱氯自来水作为对照,氟虫腈为药剂对照。处理一定时间后检查结果,计算死亡率。
死亡率和校正死亡率计算公式为:
| ${\text{死亡率}} = \frac{\text{死虫数}}{\text{供试活虫数}} \times 100 \text{%} \text{,}$ |
| ${\text{校正死亡率}} = \frac{{\text{对照组生存率}{\rm{-}}\text{处理组生存率}}}{\text{对照组生存率}} \times 100 \text{%} \text{。}$ |
选取小菜蛾羽化前2 d的蛹作为记录对象。
小菜蛾离体全脑制备简要过程:在含有木瓜蛋白酶(20 U·mL–1)的记录外液中,利用1 mL注射器针头或显微镊将小菜蛾脑从颈部摘除,孵育1 min(软化脑部组织周围的结缔组织鞘)后将脑组织分离出来并去除表面的气囊和神经鞘膜;然后将脑组织尽快转移至浴槽,浴槽中含有氧饱和(氧气和二氧化碳体积分数分别为95%和5%)的外液,其成分为145 mol·L–1 NaCl、2 mmol·L–1 CaCl2、2 mmol·L–1MgCl2、5 mmol·L–1 KCl、10 mmol·L–1 葡萄糖、1.25 mmol·L–1 NaH2PO4、20 mmol·L–1 NaHCO3;pH=7.2,360 mOsmol·Kg–1,并用铂框架固定;记录时用含氧生理盐水灌流贯穿整个记录阶段。选取触角叶的神经元作为记录目标。
记录电极灌注电极内液(150 mmol·L–1 葡萄糖酸钾,1 mmol·L–1 CaCl2,2 mmol·L–1 MgCl2,10 mmol·L–1 EGTA,10 mmol·L–1HEPES,pH=7.2,330 mOsmol·Kg–1)后电阻为8~12 MΩ。全细胞状态形成后,在电流钳模式下记录细胞的静息膜电位和自发膜电位活动。待细胞稳定5 min后通过滴加给药的方式将化合物加入浴槽内,并同步记录细胞的电活动至给药后20 min。所有记录在室温下进行。
1.4 数据处理数据处理方法参照文献[16],并分别求出各药剂的毒力回归方程、致死中浓度(LC50)、相关系数(r)以及LC50的95%置信区间。
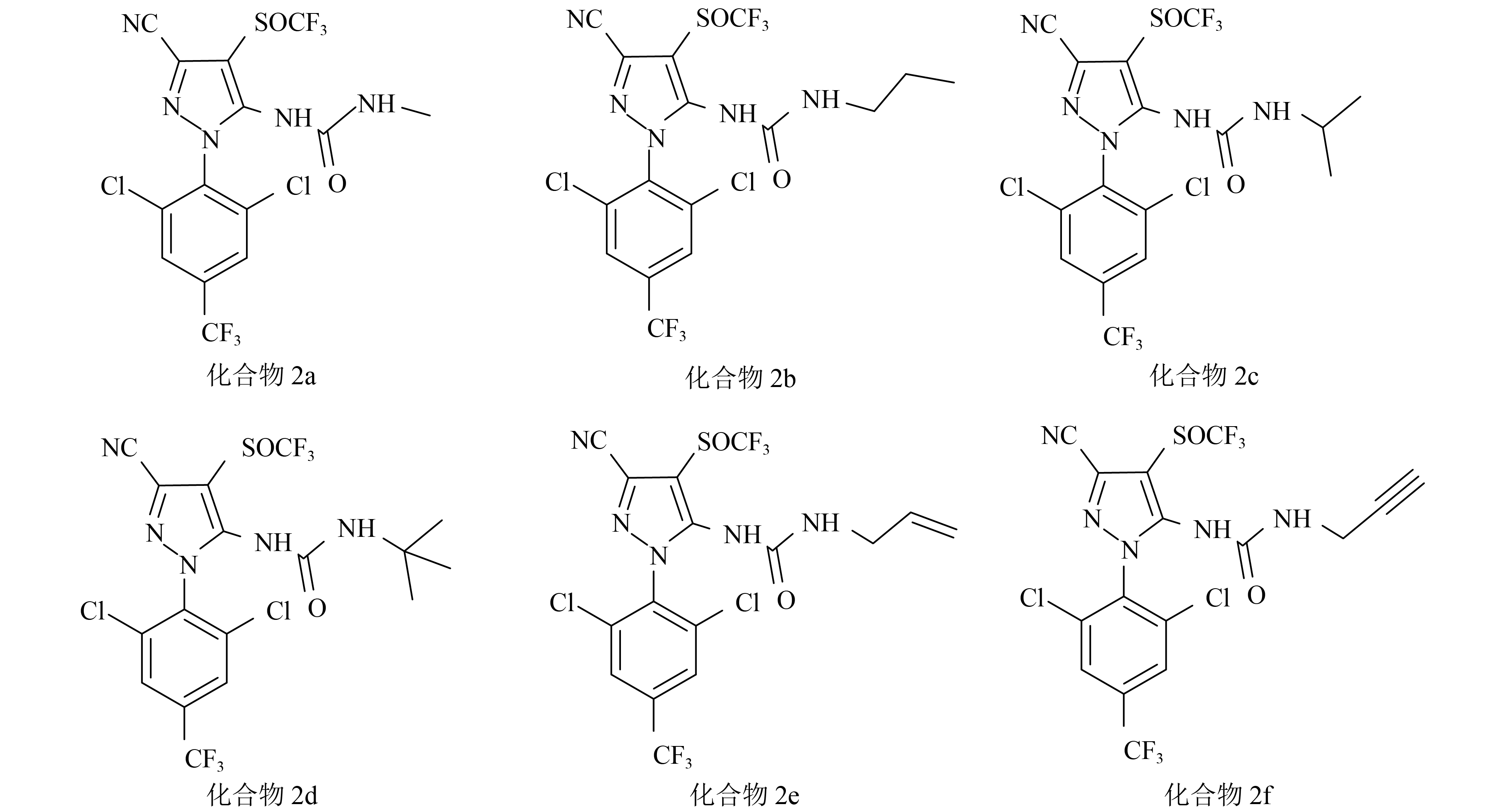
2 结果与分析 2.1 目标化合物的鉴定目标产物结构经1H NMR和13C NMR鉴定,并经MS确认为化合物2a~2f,其结构式见图2。
|
图 2 目标化合物的结构式 Figure 2 Structures of target compounds |
化合物结构的表征数据如下:
化合物2a,白色固体(产率87%),熔点(Melting point,mp):156.6~158.7 ℃。1H NMR (600 MHz,DMSO-d6) δ 10.32 (s,1H),8.35 (d,J=1.8 Hz,1H),8.31 (d,J=1.8 Hz,1H),6.63 (s,1H),3.70 (s,3H)。13C NMR (150 MHz,DMSO-d6):δ 154.59,142.31,135.78,135.39,133.85,133.63,127.11,125.64,125.00,123.53,121.72,119.90,111.39,31.56。C14H6Cl2F6N5O2S [M-H]– 的ESI-MS理论值:492.2;测量值:492.3。
化合物 2b,白色固体(产率81%),mp:219.3~220.6 ℃。1H NMR (600 MHz,DMSO-d6):δ 9.59 (s,1H),8.46 (d,J=1.8 Hz,1H),8.41 (d,J=1.8 Hz,1H),6.61 (t,J=5.8 Hz,1H),2.98~3.07 (m,2H),1.36~1.42 (m,2H),0.81 (t,J=7.4 Hz,3H)。13C NMR (150 MHz,DMSO-d6):δ 152.44,141.83,136.08,135.76,134.64,134.21,127.46,126.42,125.24,123.50,121.68,111.68,106.04,41.74,22.83,11.51。C16H10Cl2F6N5O2S [M-H]– 的ESI-MS理论值:520.0;测量值:520.3。
化合物 2c,白色固体(产率82%),mp:217.9~219.5℃。1H NMR (600 MHz,DMSO-d6):δ 9.44 (s,1H),8.46(d,J=1.9 Hz,1H),8.42 (d,J=1.9 Hz,1H),6.53 (d,J=7.5 Hz,1H),3.68~3.72 (m,1H),1.07 (d,J=6.6 Hz,3H),1.04 (d,J=6.5 Hz,3H)。13C NMR (150 MHz,DMSO-d6):δ 151.58,141.65,136.09,135.85,134.57,134.28,127.44,126.53,125.24,123.47,121.65,111.69,105.73,42.55,22.58(2C)。C16H10Cl2F6N5O2S [M-H]– 的ESI-MS理论值:520.0;测量值:520.3。
化合物 2d,白色固体(产率92%),mp:208.5~210.8℃。1H NMR (600 MHz,DMSO-d6):δ 9.26 (s,1H),8.47 (d,J=1.8 Hz,1H),8.45 (d,J=1.8 Hz,1H),6.52 (s,1H),1.23 (s,9H)。13C NMR (150 MHz,DMSO-d6):δ 151.21,141.37,135.99,135.93,134.55,134.33,127.52,126.60,125.25,123.47,121.65,111.72,105.34,51.10,28.71(3C)。C17H12Cl2F6N5O2S[M-H]– 的ESI-MS理论值:534.2;测量值:534.4。
化合物 2e,白色固体(产率78%),mp:201.9~202.5℃。1H NMR (600 MHz,DMSO-d6):δ 8.86 (s,1H),7.63 (d,J= 1.8 Hz,1H),7.59 (d,J=1.8 Hz,1H),5.92 (t,J=5.8 Hz,1H),4.93~4.99 (m,1H),4.22~4.28 (m,2H),2.84~2.91 (m,2H)。13C NMR (150 MHz,DMSO-d6):δ 152.02,141.48,135.75,135.39,134.86,134.28,133.89,127.15,126.04,124.89,123.17,121.35,115.53,113.31,106.03,41.91。C16H8Cl2F6N5O2S[M-H]– 的ESI-MS理论值:518.0;测量值:518.3。
化合物 2f,白色固体(产率75%),mp:212.9~214.5℃。1H NMR (600 MHz,DMSO-d6):δ 9.80 (s,1H),8.45 (d,J=1.8 Hz,1H),8.40 (d,J=1.8 Hz,1H),6.97 (t,J=5.8 Hz,1H),3.84~3.92 (m,2H),3.15 (s,1H)。13C NMR (150 MHz,DMSO-d6):δ 152.25,141.66,136.07,135.68,134.58,134.22,127.42,126.37,125.19,123.48,121.67,111.59,106.64,80.93,74.05,29.77。C16H6Cl2F6N5O2S [M-H]– 的ESI-MS理论值:516.0;测量值:516.3。
2.2 目标化合物对小菜蛾的毒杀活性以氟虫腈作对照,测定了目标化合物2a~2f对小菜蛾的毒力,测试结果见表1。从表1中可以看出,化合物2a~2f均具有一定的杀虫活性,其中化合物2a毒力最大,12 h LC50值为6.17 μg·mL–1,95%的置信区间为4.76~7.99 μg·mL–1。其次是化合物2e,12 h LC50值为11.42 μg·mL–1,95%置信区间为9.42~13.85 μg·mL–1。初步构效关系表明,脲基侧链的长度、体积、不饱和度等均对杀虫活性有较大影响,引入最短的饱和直链甲基(化合物2a)活性最佳。虽然化合物2b、2d、2f间的毒力大小没有显著差异,其杀虫活性弱于对照组,但上述目标化合物对3龄小菜蛾均表现出一定的拒食活性,其生长较对照组延缓。因而,我们认为所设计合成的新型芳基吡唑脲类化合物对小菜蛾幼虫可能有一定的生长抑制作用。
|
|
表 1 目标化合物2a~2f对小菜蛾的毒力测定1) Table 1 Toxicity of target compounds (2a–2f) against Plutella xylostella |
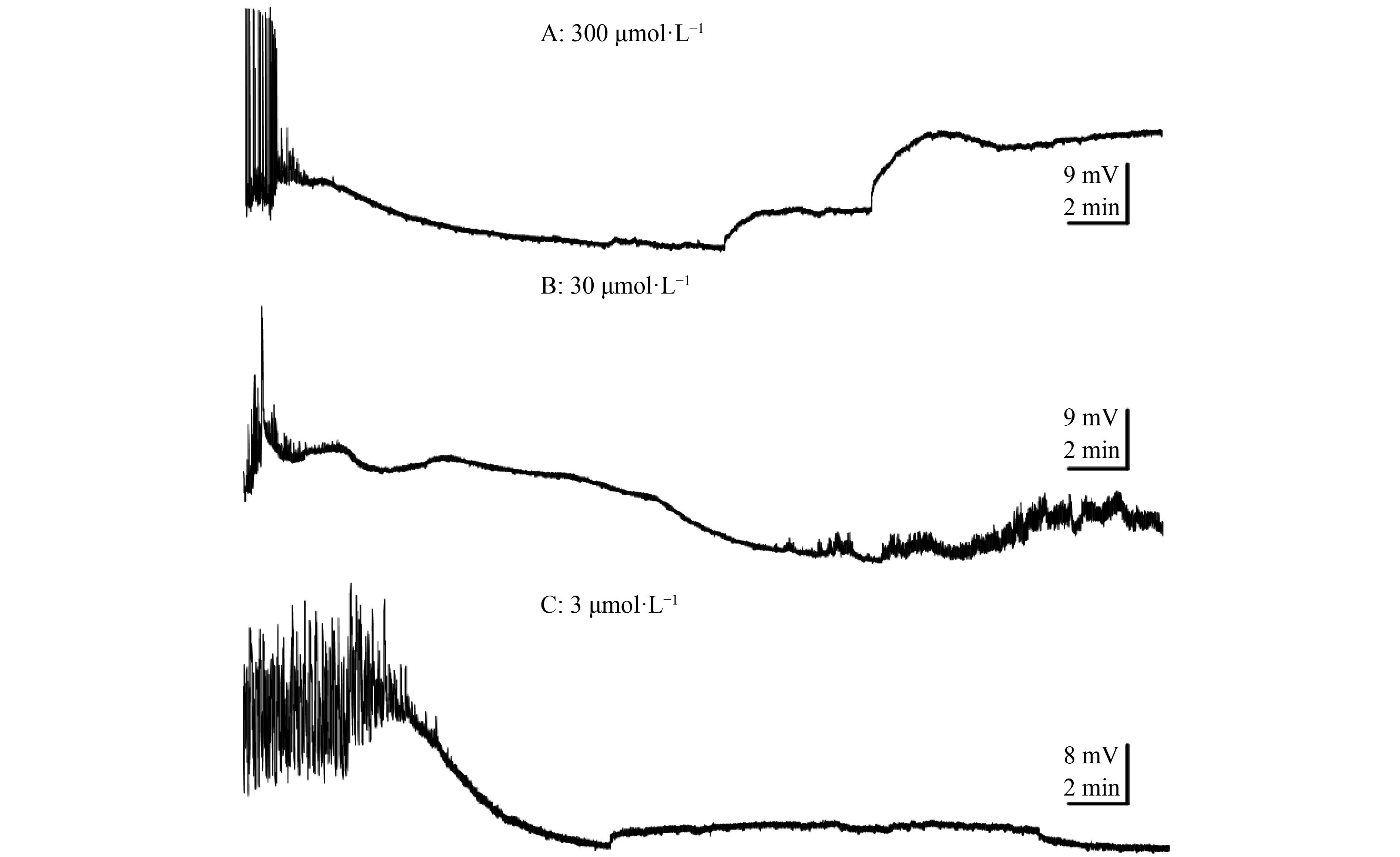
通过滴加给药的方式检测化合物对神经元静息膜电位和自发电活动的影响。图3结果显示(以化合物2e为例),化合物对神经元静息膜电位的作用和自发电活动具有浓度和时间依赖性,随化合物浓度的增加,膜电位去极化的程度和自发电活动被抑制的程度逐渐增加,并随作用时间的延长逐步加强并达到峰值。
|
图 3 不同浓度的化合物2e对嗅神经元静息膜电位和自发电活动的影响 Figure 3 Effects of different concentrations of compound 2e on resting membrane potential and self-generation activities in olfactory neurons |
比较了6个化合物及氟虫腈对神经元兴奋性的影响及其作用方式,图4A~4H分别为化合物2a、化合物2b、化合物2c、氟虫腈、化合物2d、化合物2e、化合物2f及DMSO对神经元膜电位和自发电活动的影响。化合物总体作用趋势呈现2种作用模式,一种(如化合物2a、化合物2c)作用趋势类似于氟虫腈,早期神经元兴奋性增加,静息膜电位去极化及自发电活动增加,随作用时间延长膜电位去极化至最大值并伴随自发电活动完全被抑制,提示神经传导功能被阻断。另一种(如化合物2b、化合物2d、化合物2e、化合物2f)作用趋势明显区别于氟虫腈,呈现出神经元膜电位短暂去极化,继而膜电位逐渐超级化(红色箭头指示膜电位的超级化),并伴随自发电活动被抑制。

|
图 4 目标化合物2a~2f对神经元兴奋性影响的比较 Figure 4 Comparison of the effects of compounds 2a-2f on neuronal excitability A~H: 分别为化合物2a、化合物2b、化合物2c、氟虫腈、化合物2d、化合物2e、化合物2f及DMSO作用前后神经元静息膜电位和自发电活动的展示图;其中1:给药前神经元的神经元静息膜电位和自发电活动,3:给予30 μmol·L-1 不同化合物及φ为0.1%的DMSO后神经元静息膜电位和自发电活动的时间变化趋势;2:3中灰色区域的放大图,其时程与1相同 |
为了寻找作用于昆虫中枢神经系统的新型活性化合物,基于中间体衍生化策略,我们以氟虫腈为母体结构,设计合成了6个芳基吡唑类化合物。以氟虫腈为原料,经过酰胺化和胺化两步反应合成目标化合物,产率达75%以上。中间体的获得及其重要。以丙酮作溶剂,强碱氢氧化钾(以3倍量较为适宜)作缚酸剂,与氯甲酸苯酯反应得中间体(不稳定),不进行进一步的过柱处理,采用一锅法继续进行下一步处理。用硅藻土抽滤,蒸干,换用CH2Cl2作溶剂,DBU作催化剂,在50~80 ℃下反应即得产率较为理想的目标产物。
新化合物结构均由表征数据所验证。目标化合物在1H NMR谱图上有3种最主要的氢:芳环上的氢、酰胺键上的氢和烃基上的氢。芳环上的氢的吸收位于低场,表现为单峰,2个酰胺键上的氢分别位于高场和中低场,也较易归属。此类化合物的ESI-MS谱中均有较强的分子离子峰,主要碎片峰都能得到很好的归属。
酰胺脲键结构的引入对化合物的结构和性质都有一定的影响。酰胺脲键在动植物体内是普遍存在的,引入酰胺键,目的是使其经过植物或昆虫代谢后能够降解产生更为有效的偶合物。目标化合物的毒力测定表明,化合物2a~2f仍具有一定的杀虫活性,其中化合物2a毒力最大,12h LC50值为6.17 μg·mL-1。初步构效关系表明,脲基侧链的长度、体积、不饱和度等均对杀虫活性有较大影响,引入最短的饱和直链甲基(化合物2a)活性最佳。虽然化合物2b、2d、2f的毒力大小没有显著差异,其杀虫活性弱于对照组,但上述目标化合物对3龄小菜蛾均表现出一定的拒食活性,其生长较对照组延缓。因而,我们推测所设计合成的新型芳基吡唑脲类化合物对小菜蛾幼虫可能有一定的生长抑制作用。
在对神经元膜电位和自发电活动的影响方面,化合物2b、2d、2e及2f呈现出不同于氟虫腈的作用模式。这表明,虽然化合物类别相同,但其毒性作用方式与母体结构相比可能存在差异,具有进一步的研究价值。因此,笔者认为在具有生物活性分子上引入酰胺脲键,是改变农药对昆虫中枢神经系统毒性作用方式的潜在策略,在新农药创制中具有一定指导意义。
| [1] |
HAINZL D, CASIDA J E. Fipronil insecticide: Novel photochemical desulfinylation with retention of neurotoxicity[J]. Proc Natl Acad Sci, 1996, 93(23): 12764-12767. DOI:10.1073/pnas.93.23.12764 (  0) 0) |
| [2] |
SIMON D N, AMARAL R V, BELZUNCES L P, et al. Systemic insecticides (neonicotinoids and fipronil): Trends, uses, mode of action and metabolites[J]. Environ Sci Pollut R, 2015, 22(1): 5-34. DOI:10.1007/s11356-014-3470-y (  0) 0) |
| [3] |
张元, 张博, 任天瑞. 氟虫腈与昆虫γ-氨基丁酸受体相互作用研究[J]. 农药学学报, 2016, 18(1): 49-56. (  0) 0) |
| [4] |
ZHAO X L, YEH J Z, SALGADO V L, et al. Fipronil is a potent open channel blocker of glutamate-activated chloride channels in cockroach neurons[J]. J Pharmacol Exp Ther, 2004, 310(1): 192-201. DOI:10.1124/jpet.104.065516 (  0) 0) |
| [5] |
GUNASEKARA A S, TRUONG T, GOH K S, et al. Environmental fate and toxicology of fipronil[J]. J Pestic Sci, 2007, 32(3): 189-199. DOI:10.1584/jpestics.R07-02 (  0) 0) |
| [6] |
孙竹君. 氟虫腈的禁用促使我国水稻杀虫剂重新洗牌[J]. 中国农药, 2009, 5(10): 21-24. (  0) 0) |
| [7] |
CABONI P, SAMMELSON R E, CASIDA J E. Phenylpyrazole insecticide photochemistry, metabolism, and GABAergic action: Ethiprole compared with fipronil[J]. J Agric Food Chem, 2003, 51(24): 7055-7061. DOI:10.1021/jf030439l (  0) 0) |
| [8] |
SCHUELE G, BARNETT S, LUEMPERT L G, et al. The efficacy of pyriprole topical solution against infestations of adult ticks (Ixodes scapularis, Amblyomma americanum and Dermacentor variabilis) on dogs
[J]. Int J Appl Res Vet M, 2009, 7(1): 50-56. (  0) 0) |
| [9] |
BOUHSIRA E, FYSIKOPOULOS A, FRANC M. Efficacy of fipronil-(S)-methoprene, metaflumizone combined with amitraz, and pyriprole commercial spot-on products in preventing Culex pipiens pipiens from feeding on dogs
[J]. Vet Rec, 2009, 165(5): 135-137. DOI:10.1136/vr.165.5.135 (  0) 0) |
| [10] |
LEES K, MUSGAARD M, SUWANMANEE S, et al. Actions of agonists, fipronil and ivermectin on the predominant in vivo splice and edit variant (RDLbd, I/V) of the Drosophila GABA receptor expressed in Xenopus laevis oocytes
[J]. Plos One, 2014, 9(5): e97468. DOI:10.1371/journal.pone.0097468 (  0) 0) |
| [11] |
大连瑞泽农药股份有限公司. 新型杀虫剂—丁烯氟虫腈[J]. 世界农药, 2005, 27(5): 48. (  0) 0) |
| [12] |
GUAN A, LIU C L, YANG X P, et al. Application of the intermediate derivatization approach in agrochemical discovery[J]. Chem Rev, 2014, 114(14): 7079-7107. DOI:10.1021/cr4005605 (  0) 0) |
| [13] |
李佳, 李贺年, 赵斌涛, 等. 电生理技术在昆虫学研究中的研究进展[J]. 河北农业大学学报, 2003, 26(Z1): 208-211. DOI:10.3969/j.issn.1000-1573.2003.z1.063 (  0) 0) |
| [14] |
程东美, 张志祥, 胡美英. 电生理技术在昆虫毒理学上的应用[J]. 仲恺农业技术学院学报, 2001, 14(3): 64-70. (  0) 0) |
| [15] |
XIA Q, WEN Y J, WANG H, et al. β-glucosidase involvement in the bioactivation of glycosyl conjugates in plants: Synthesis and metabolism of four glycosidic bond conjugates in vitro and in vivo
[J]. J Agric Food Chem, 2014, 62(46): 11037-11046. DOI:10.1021/jf5034575 (  0) 0) |
| [16] |
张志祥, 徐汉虹, 程东美. Excel在毒力回归计算中的应用[J]. 昆虫知识, 2002, 39(1): 67-70. DOI:10.7679/j.issn.2095-1353.2002.020 (  0) 0) |
 2018, Vol. 39
2018, Vol. 39


