苯丙氨酸解氨酶(Phenylalanine ammonia-lyase,PAL)是苯丙氨酸代谢途径的关键酶和限速酶[1],只存在于微生物与植物中。在PAL作用下,苯丙烷类代谢完成第1步反应,生成香豆酸、阿魏酸和芥子酸等中间产物,这些中间产物进一步转化为香豆素和绿原酸,也可形成苯丙烷酸CoA酯,再进一步代谢转化为一系列苯丙素类化合物,如类黄酮、木质素和生物碱[2]。因此,PAL基因在植物的代谢过程中起着重要作用。
20世纪70年代以来,越来越多的研究显示PAL基因与细胞分化存在一定相关性,愈伤组织分化过程中PAL活性增强,分化组织中有管状分子形成[3]。章金明[4]发现,当植物叶片受到机械损伤时,叶片PAL含量大幅增加,而且活性快速升高。苯丙烷类代谢产物经类黄酮途径产生黄酮类化合物,间接参与呼吸代谢,可作为植物体特殊贮能,帮助植物体清除自由基等。黄酮类化合物对根瘤菌有趋化作用[5],有些还可作为根瘤菌结瘤基因的诱导物质[6]。此外,PAL基因在植物抗逆过程中也起着重要作用,研究发现多种植物受病原菌侵染后,PAL活性明显升高,并表现出规律性变化[7-8]。欧芹Petroselinum crispum在受伤害或紫外线照射时PAL基因的转录水平提高[9],胡萝卜Daucus carota细胞受到UV-B照射时PAL基因对应的mRNA表达量会增加[10]。
桉树Eucalyptus是原产于澳大利亚的树种,为当地重要的工业用材,具有速生和丰产的特点,相继被100多个国家引种。目前,尾叶桉E. urophylla是我国华南地区重要的纸浆材造林树种 [11],也是一种比较理想的水土保持树种,具有美化和绿化环境的功能。此外,黄瑶等[12]研究表明尾叶桉叶精油对某些常见菌有抑制效果。因此,研究尾叶桉抗逆性具有重要的经济、生态和社会效益。虽然目前已从多种植物中克隆出PAL基因,但在尾叶桉中鲜见有关PAL基因的相关报道。本研究以尾叶桉叶片为材料,开展尾叶桉PAL基因的克隆与表达分析,并进行DNA序列变异和系统进化等生物信息学方面的研究,解析PAL基因在尾叶桉抗逆过程中的作用。
1 材料与方法 1.1 试验材料2009年,广东省林业科学研究院从尾叶桉自然分布区如澳洲大陆、新几内亚岛、印度尼西亚以及菲律宾等24个国家和地区收集了500个基因型的尾叶桉个体,种植于广东省肇庆市国有林场总场大南山林场,建立了尾叶桉种质资源库。本研究用于提取DNA的材料取自该基因库中24个种源的35个基因型个体。
用于提取RNA的材料来自广东省林业科学研究院内经水肥处理的16个月生尾叶桉无性系个体ZQUA44。水肥处理分为2部分:水分梯度处理和养分梯度处理。水分梯度处理分别为:梯度1,20%~40%田间持水量;梯度2,40%~60%田间持水量;梯度3,60%~80%田间持水量。养分梯度处理分别为:梯度1,基肥(钙镁磷肥250 g);梯度2,基肥(钙镁磷肥250 g),8月份施1次复合肥150 g,第2年春天施复合肥100 g;梯度3,基肥(钙镁磷肥250 g+复合肥150 g),种植2个月后施尿素100 g,8月份施1次复合肥150 g,第2年春天施复合肥100 g。具体见表1。
|
|
表 1 尾叶桉无性系9种不同水肥处理 Table 1 Nine different water-fertilizer treatments of Eucalyptus urophylla clone |
总DNA的提取按照Plant Genomic DNA Kit进行,试剂盒购自天根生化科技(北京)有限公司。
1.2.2 RNA的提取和cDNA的合成总RNA的提取按照RNAsimple Total RNA Kit进行,cDNA的合成按照Tiangen FastKing RT Kit进行,2种试剂盒均购自天根生化科技(北京)有限公司。
1.2.3 同源基因的获得尾叶桉PAL同源基因从Phytozome网站(https://phytozome.jgi.doe.gov/pz/ portal.html)巨桉E. grandis基因序列数据库下载。与尾叶桉PAL基因同源的cDNA从NCBI数据库(https://www. ncbi.nlm.nih.gov/)下载。
1.2.4 引物设计及cDNA全长和基因全长扩增利用NCBI Primer-BLAST(https://www.ncbi.nlm.nih.gov/tools/primer-blast/index.cgi?LINK_ LOC=BlastHome)网站,根据巨桉cDNA序列在其可能的开放阅读框两端设计引物:
PAL cDNA F:5′-GTTCTCCCTCGCCATTCTCC-3′;
PAL cDNA R:5′-TCAAAGCAAATACCACTCACGG-3′。
该基因较长,将其分成3段扩增。根据巨桉同源基因序列,在其开放阅读框两端分别设计引物:
PAL 1F:5′-CTTCGGTACGTTACCCACCC-3′;
PAL 1R:5′-ATCCGTGACGTGATTCCCTG-3′;
PAL 2F:5′-TGCGTCTTGTCAGGGAATCA-3′;
PAL 2R:5′-GCCGCCTTGACGTAAGAACT-3′;
PAL 3F:5′-TGCAGCTATCATGGAGCACA-3′;
PAL 3R:5′-TCGGAATGCTTTGTGCGGTA-3′。
本研究采用25 μL聚合酶链式反应(PCR)体系, 以尾叶桉叶片基因组DNA为模板,加入Taq PCR Master Mix (2×,blue dye) 12.5 μL,1 μL基因组DNA(5 μg·L–1),0.4 μmol·L–1的正反向引物各2 μL,加适量蒸馏水至25 μL。于94 ℃条件下4 min;35个循环(94 ℃,30 s;60 ℃,30 s;72 ℃,90 s);72 ℃,10 min。在此热循环条件下扩增出1 500 bp的DNA片段,然后通过拼接获得DNA全长。
1.2.5 逆转录定量聚合酶链式反应(RT-qPCR)检测PAL基因在尾叶桉无性系不同处理中的表达模式采用NCBI Primer-BLAST (https://www.ncbi.nlm.nih.gov/tools/ primer-blast/index.cgi?LINK_LOC=BlastHome) 网站设计扩增长度约200 bp的RT-qPCR引物,检测PAL基因在不同处理中的表达模式:
PAL RT-qPCR F:5′-ATCAGATTCTTGAACGCCGGT-3′;
PAL RT-qPCR R:5′-AAGTCACCAGAGGCGGAGAT-3′。
以肌动蛋白基因Actin作为内参,引物序列为:
Act F:5′-CTCCATCATGAAATGCGATG-3′;
Act R:5′-TTGGGGCTAGTGCTGAGATT-3′。
RT-qPCR反应按照FastKing RT Kit进行,试剂盒购自天根生化科技(北京)有限公司。每个反应设置4个样品重复,4个内参对照重复。依次加入2×Talent RT-qPCR PreMix 10 μL, 10 μmol·L–1的正反向引物各0.6 μL,cDNA 2 μL,添加RNase-Free dd H2O至终体积为20 μL。RT-qPCR反应程序为:94 ℃,5 min;40个循环(94 ℃,30 s;60℃,30 s;72 ℃,30 s)。扩增结束后,通过溶解曲线检查引物的扩增特异性,然后应用7500Fast软件分析结果。
1.2.6 PAL基因的单核苷酸多态性(SNP)分析以选取的35株个体的总DNA为模板进行PCR扩增,对PCR扩增产物进行测序,然后将每一个基因片段的核苷酸序列拼接成完整的基因序列。利用MEGA6.0软件对PAL基因的35个序列进行比对分析,检测该基因的SNP。利用Dnasp4.90.1软件对该基因进行多态性分析,并进一步分析编码区和非编码区的SNP频率及编码区的同义突变和非同义突变情况,其中非同义突变又包括错义突变和无义突变等。
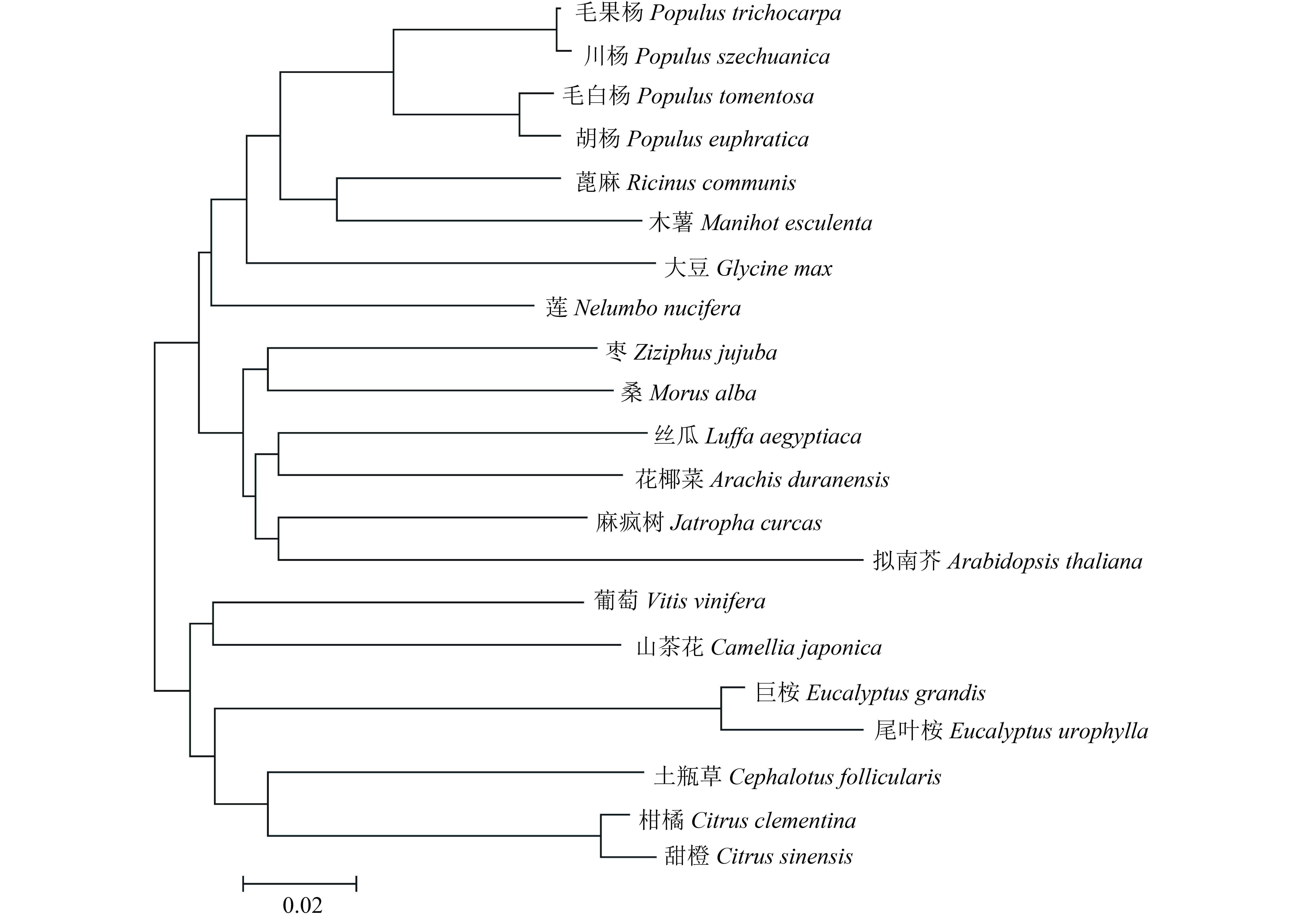
2 结果与分析 2.1 尾叶桉PAL同源cDNA的克隆及其结构特征为了分离尾叶桉PAL基因的cDNA序列,本研究从巨桉全基因组上获得同源PAL基因序列。以此为基准设计引物,从尾叶桉叶片cDNA中扩增出PAL基因的氨基酸编码序列。对该序列测序后发现该序列与巨桉PAL基因序列相似度达96%,因此该序列即为尾叶桉EuuPAL基因序列。该序列共2 748 bp,包括166 bp的5′非编码区,411 bp的3′非编码区,以及2 172 bp的氨基酸编码序列。将获得的PAL基因氨基酸序列在NCBI上进行比对,并下载其他不同物种的氨基酸序列。对拟南芥Arabidopsis thaliana、大豆Clycine max、巨桉、葡萄Vitis vinifera和柑橘Citrus clementina等21个物种的氨基酸序列进行进化分析,发现尾叶桉与巨桉PAL基因亲缘关系最近,是同源基因(图1)。
|
图 1 尾叶桉及其他物种PAL基因的进化分析 Figure 1 The phylogenetic tree of PAL gene in Eucalyptus urophylla and other plant species |
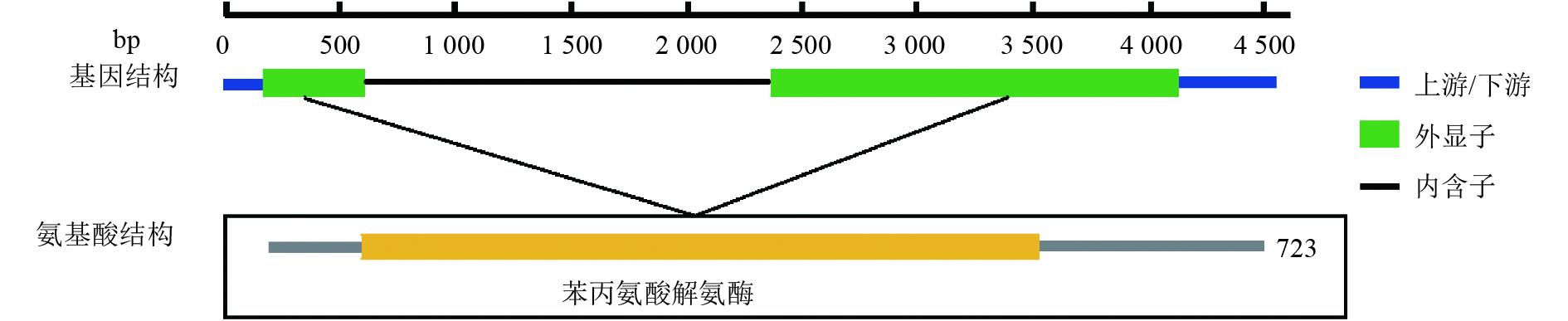
根据cDNA序列信息设计引物,本研究从尾叶桉基因组DNA中克隆出PAL基因组序列全长,并对其进行分析。PAL基因组全长4 507 bp,包括166 bp的5′非编码区、411 bp的3′非编码区、2 172 bp的氨基酸编码序列(由2个外显子组成,分别为422 bp和1 750 bp)以及1 759 bp的内含子区域(图2)。
|
图 2 尾叶桉PAL基因结构序列 Figure 2 The structure of PAL gene in Eucalyptus urophylla |
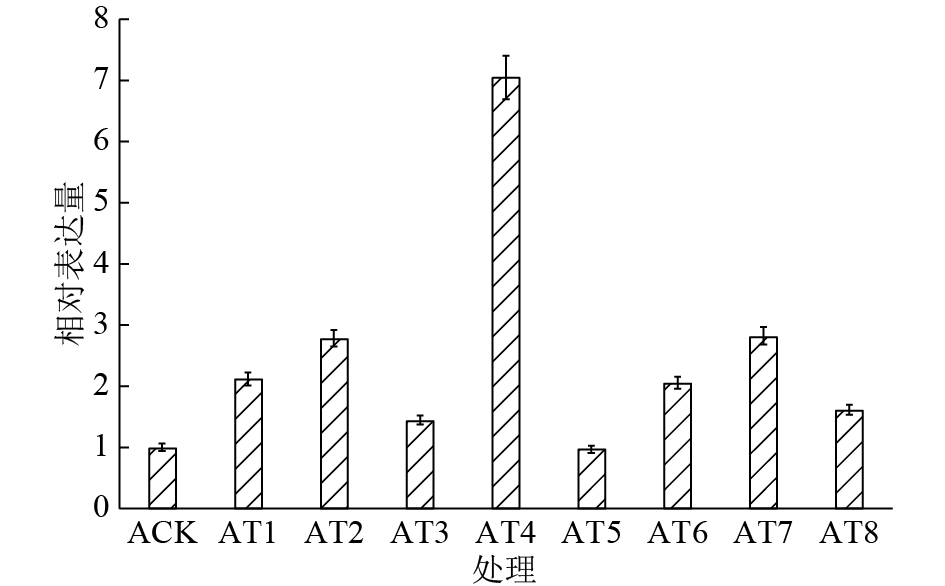
为了确定尾叶桉PAL基因在不同水肥处理中是否有差异性表达,我们提取尾叶桉9个处理的叶片RNA并反转录为cDNA进行RT-qPCR反应。结果表明PAL基因在AT4处理中表达量最高,AT2以及AT7处理次之,AT5处理表达量最低(图3)。
|
图 3 尾叶桉PAL基因在9种不同水肥处理中的相对表达量 Figure 3 Relative expression of PAL gene of Eucalyptus urophylla in nine different water-fertilizer treatments |
根据已知序列设计引物,对35株尾叶桉个体进行PCR扩增和序列分析。将比对的结果整理分析后发现,PAL基因全长4 507 bp,共有SNP位点307个,每15个碱基便出现1个多态性位点。在这些SNP位点中,频率最高的(7 bp–1)出现在内含子区域,频率最低的(194 bp–1)出现在外显子区域(表2)。这和预期的生物在选择压下编码区会高度保守一致。在外显子区域共24个SNP位点,其中21个为同义突变,3个为非同义突变(表3)。总体来说,PAL基因具有较大多态性,SNP系数πT和θw分别为0.036 46和0.049 2。基因不同结构区域多态性系数差异很大,在第1个外显子区域多态性比较小,多态性系数πT和θw分别为0.064 85和0.082 3;在内含子区域多态性比较大,多态性系数πT和θw分别为0.071 36和0.099 1(表2)。
|
|
表 2 尾叶桉PAL基因SNP分析 Table 2 SNP analysis of PAL gene in Eucalyptus urophylla |
|
|
表 3 尾叶桉PAL基因编码区内SNP突变类型分析 Table 3 Mutation types of SNPs located in the coding region of PAL gene of Eucalyptus urophylla |
碱基之间存在2种突变类型:转换和颠换。转换是嘌呤与嘌呤之间或者嘧啶与嘧啶之间的突变;颠换是嘌呤与嘧啶之间的突变。PAL基因中的307个SNP位点包括202个转换突变(89个A/G转换、113个T/C转换)和105个颠换突变(31个A/C颠换、21个T/G颠换、28个A/T颠换、25个G/C颠换)。
3 讨论与结论 3.1 尾叶桉PAL基因的进化分析与SNP分析将克隆出来的尾叶桉PAL基因的氨基酸序列在NCBI中进行比对,发现尾叶桉PAL基因与巨桉相似性最高,印证了尾叶桉与巨桉的亲缘关系。对该基因进行SNP分析发现共有307个多态性位点,多态性程度较高。但多数多态性位点都出现在内含子区域(即非编码区域),该区域的SNP变异一般不会直接影响PAL基因的正常表达与PAL正常催化功能。外显子区域24个多态性位点中21个是同义突变,仅3个是错义突变,并且均属于罕见突变位点。因此总体来说尾叶桉PAL基因在长期进化过程中保持着比较稳定的遗传,这一结果与前人研究一致[13]。
在自然界中,约有一半以上的SNP突变是T/C转换或者反义的A/G转换。人类每3个SNP突变中就有2个是T/C或者A/G转换,小麦和玉米大约有45%和55%的SNP突变是T/C或A/G转换。发生这一现象的原因在于甲基化的核苷酸C在去氨基化后,容易被DNA聚合酶误读为T[14],因此可以根据T/C或者A/G转换的比例来判断测序结果是否可信。通过对PAL基因 2种碱基变换形式的分析发现,A/G和T/C转换的突变频率(28.99%和36.81%)远大于A/C、T/G、A/T和G/C颠换的突变频率(10.10%、6.84%、9.12%和8.14%)。T/C和A/G转换的比例大概占65.80%,与人类T/C和A/G转换的比例相近。
3.2 PAL基因在尾叶桉抗逆性方面的作用大量研究表明,PAL基因参与植物的多种抗逆活动,如抗病[15-19]和抗虫[20-21]等。为了研究尾叶桉PAL基因与其抗逆性是否相关,此次试验运用了2个变量来研究尾叶桉PAL基因表达与抗逆性的关系。结果表明,PAL基因在AT5处理的表达量与对照一致,且AT5处理表型数据也与对照一致,说明AT5处理已能满足尾叶桉生长对水分和养分的需求。AT4处理中PAL基因表达量最高,说明在水分相同情况下,养分的短缺成为影响尾叶桉幼苗生长的重要因素。因此PAL基因可能参与了尾叶桉对逆境的响应过程。AT2与AT7处理中PAL基因表达量基本一致,均高于对照2倍,说明在这2种处理下植物受到一定程度的胁迫,但胁迫程度低于AT4处理。因此植物的生长受到水分和养分的联合作用。
| [1] |
NAKAZAWA A, NOZUE M, YASUDA H, et al. Expression pattern and gene structure of phenylalanine ammonia-lyase in Pharbitis nil
[J]. J Plant Res, 2001, 114(3): 323-328. DOI:10.1007/PL00013994 (  0) 0) |
| [2] |
BOVÉ C, CONN E E. Metabolism of aromatic compounds in higher plants: II: Purification and properties of the oxynitrilase of Sorghum vulgare
[J]. J Biol Chem, 1961, 236(1): 207-210. (  0) 0) |
| [3] |
余沛涛, 薛应龙. 植物苯丙氨酸解氨酶(PAL)在细胞分化中的作用[J]. 植物生理学报, 1987, 13(1): 14-19. (  0) 0) |
| [4] |
章金明. MeSA、叶蝉为害和机械刺伤对茶芽挥发物及PAL、PPO酶活性影响[D]. 杭州: 中国农业科学院茶叶研究所, 2006.
(  0) 0) |
| [5] |
CAETANO-ANOLLÉS G, CRIST-ESTES D K, BAUER W D. Chemotaxis of Rhizobium meliloti to the plant flavone luteolin requires functional nodulation genes
[J]. J Bacteriol, 1988, 170(7): 3164-3169. DOI:10.1128/jb.170.7.3164-3169.1988 (  0) 0) |
| [6] |
HARTWIG U A, PHILLIPS D A. Release and modification of nod-gene-inducing flavonoids from alfalfa seeds
[J]. Plant Physiol, 1991, 95(3): 804-807. DOI:10.1104/pp.95.3.804 (  0) 0) |
| [7] |
江昌俊, 余有本. 苯丙氨酸解氨酶的研究进展[J]. 安徽农业大学学报, 2001, 28(4): 425-430. (  0) 0) |
| [8] |
曾永三, 王振中. 苯丙氨酸解氨酶在植物抗病反应中的作用[J]. 仲恺农业技术学院学报, 1999, 12(3): 56-65. (  0) 0) |
| [9] |
LOIS R, DIETRICH A, HAHLBROCK K, et al. A phenylalanine ammonia-lyase gene from parsley: Structure, regulation and identification of elicitor and light responsive cis-acting elements
[J]. EMBO J, 1989, 8(6): 1641-1648. (  0) 0) |
| [10] |
TAKEDA J, OBI I, YOSHIDA K. Action spectra of phenylalanine ammonia-lyase and chalcone synthase expression in carrot cells in suspension[J]. Physiol Plant, 1994, 91(3): 517-521. DOI:10.1111/ppl.1994.91.issue-3 (  0) 0) |
| [11] |
徐建民. 尾叶桉纸浆材育种综合选择及改良研究[D]. 北京: 中国林业科学研究院, 2003.
(  0) 0) |
| [12] |
黄瑶, 田玉红, 刘雄民, 等. 尾叶桉叶精油的成分分析及抑菌效果初探[J]. 北方园艺, 2010(6): 26-28. (  0) 0) |
| [13] |
杜何为, 蔡荣, 徐树德, 等. 克隆植物苯丙氨酸解氨酶基因通用引物的发掘与应用[J]. 河北农业科学, 2010, 14(7): 45-47. (  0) 0) |
| [14] |
SUH Y, VIJG J. SNP discovery in associating genetic variation with human disease phenotypes[J]. Mutat Res, 2005, 573(1): 41-53. (  0) 0) |
| [15] |
张淑珍, 徐鹏飞, 吴俊江, 等. 大豆疫霉根腐病菌毒素处理抗感不同大豆品种后苯丙氨酸解氨酶活性的变化[J]. 作物杂志, 2008, 1: 47-49. (  0) 0) |
| [16] |
MOESTA P, GRISEBACH H. L-2-Aminooxy-3-phenylpropionic acid inhibits phytoalexin accumulation in soybean with concomitant loss of resistance against Phytophthora megasperma f. sp. glycinea
[J]. Physiol Plant Pathol, 1982, 21(1): 65-70. DOI:10.1016/0048-4059(82)90008-X (  0) 0) |
| [17] |
冯洁, 陈其煐. 棉株体内几种生化物质与抗枯萎病之间关系的初步研究[J]. 植物病理学报, 1991, 21(4): 291-297. (  0) 0) |
| [18] |
郭文硕. 杉木对炭疽病的抗性与苯丙氨酸解氨酶的关系[J]. 应用与环境生物学报, 2002, 8(6): 592-595. (  0) 0) |
| [19] |
尚庆茂, 张志刚. 亚精胺对黄瓜幼苗灰霉病的诱抗作用[J]. 应用生态学报, 2008, 19(4): 825-830. (  0) 0) |
| [20] |
吴龙火, 李庆, 杨群芳, 等. 禾谷缢管蚜取食5种山羊草的诱导抗性[J]. 中国农业科学, 2008, 41(1): 102-107. (  0) 0) |
| [21] |
HARTLEY S E, FIRN R D. Phenolic biosynthesis, leaf damage, and insect herbivory in birch (Betula pendula)
[J]. J Chem Ecol, 1989, 15(1): 275-283. DOI:10.1007/BF02027789 (  0) 0) |
 2018, Vol. 39
2018, Vol. 39


