农业病原微生物导致重大的农作物病害及动物疾病,成为保障国家粮食安全和农产品有效供给的关键限制因素。当前,我国主要粮食作物和经济作物每年因病害造成的减产和经济损失巨大,每年因病害损失的粮食达10%以上[1];水产养殖鱼类和甲壳类主要病害的发病率为20%~30%,每年因病害造成的损失在100亿元以上[2-3]。同时,在病害防控中由于大量使用农药、抗生素和兽药等,造成了农(兽)药在粮食和副食品上的高残留以及对土壤、水体和空气的污染,严重威胁了人们的健康[4]。微生物群体感应是近年来微生物学领域的重大发现之一,其核心内容是:以单细胞形式存在的微生物个体通过产生和感应小分子化学信号进行广泛的信息交流,从而以群体形式对寄主和外部环境做出协同反应,包括建立侵染和产生抗生素等[5-7]。该系统的发现为明确病原菌致病调控机理和发展新的病害防控策略提供了一个全新的切入点。群体感应这种细胞间的化学通讯系统首先在细菌中发现,它在细菌致病基因表达、生物膜形成以及抗生素(抗菌活性物质)合成等方面起关键调控作用。病原真菌尤其是以单细胞形态存在的真菌,可以产生和利用小分子化学信号调控群体成员基因的表达,从而控制各类生物功能。在病原菌−寄主互作过程中,病原菌和寄主各自依靠释放小分子信号分子干预对方,因而对病害的发生发展常常起着关键的作用。这种病原−寄主间的化学信号识别现象通常称之为“跨界通讯”,是群体感应研究的衍生和发展,也是当前国际上的研究热点之一。
为避免或减少因病害造成的农产品产量损失,必须对病原菌致病机制以及病原−寄主的互作机制进行深入研究。微生物群体感应通讯系统对病原菌的致病基因表达、生物膜形成以及生防菌抗生素(抗菌活性物质)合成等有益性状具有非常重要的调控作用,因此,加强微生物群体感应通讯系统研究,解析群体感应通讯系统在病原菌致病及其与寄主互作过程中的功能和作用机制,对保障国家粮食安全和农产品的有效供给具有重要意义。化学药物和抗生素是当前农作物病害及动物疾病防控不得已的选择和主要的防治方式,化学污染引起的食品质量安全已成为全人类共同关注的重大课题,化学药物过度和不当使用造成农产品化学污染物超标,削弱了我国农产品的国际竞争力,也影响了国家的整体形象。Zhang等[6]和Dong等[8-10]在国际上证明干扰或阻断群体感应系统可以发展新的病害防控策略和措施以及淬灭群体感应(Quorum quenching,群体淬灭)可以控制病害的发生发展。群体淬灭的核心内容是阻断微生物的信号交流,掌握了微生物的“语言”,就可以对其进行干扰,从而阻断微生物的信号交流,使微生物成为“聋哑”个体。研究病原菌之间的信息交流及病原菌与宿主间的信息通讯,不仅能加深人们对病原菌致病机理的了解,也为发展新型病害防控策略并从源头上消除农产品质量安全隐患提供了关键的理论和技术支撑。
对微生物病害的防治在农业上主要通过培育抗病品种和化学防治,人和动物则依靠抗生素。农药不当使用造成严重的生态环境污染,据估算高达80%的农药漂移或流失至非靶标生物、土壤和水域中。这种使微生物面临“生”与“死”的选择的药物作用方式,迫使微生物病原产生突变,一方面导致能抵抗多种抗生素的超级病原菌(Superbugs)愈来愈多,抗药性和耐药性问题变得日益严峻;另一方面导致需投放更多的化学药物,从而加剧了对环境的污染。阻断群体感应信号交流可以显著降低致病基因和抗药性基因的表达,但不影响微生物和其他生物的生长。因此,发现新的群体感应系统,探索新型安全的病害防治策略,减少化学药物的使用,对解决日趋严重的环境污染与病原菌耐药性等问题具有重大意义。本文将追溯与此有关的群体感应研究的一些重要发现、并探讨群体感应研究的未来发展前景,旨在为从事微生物学和植物病理学等研究的科研工作者提供一些思路与参考。
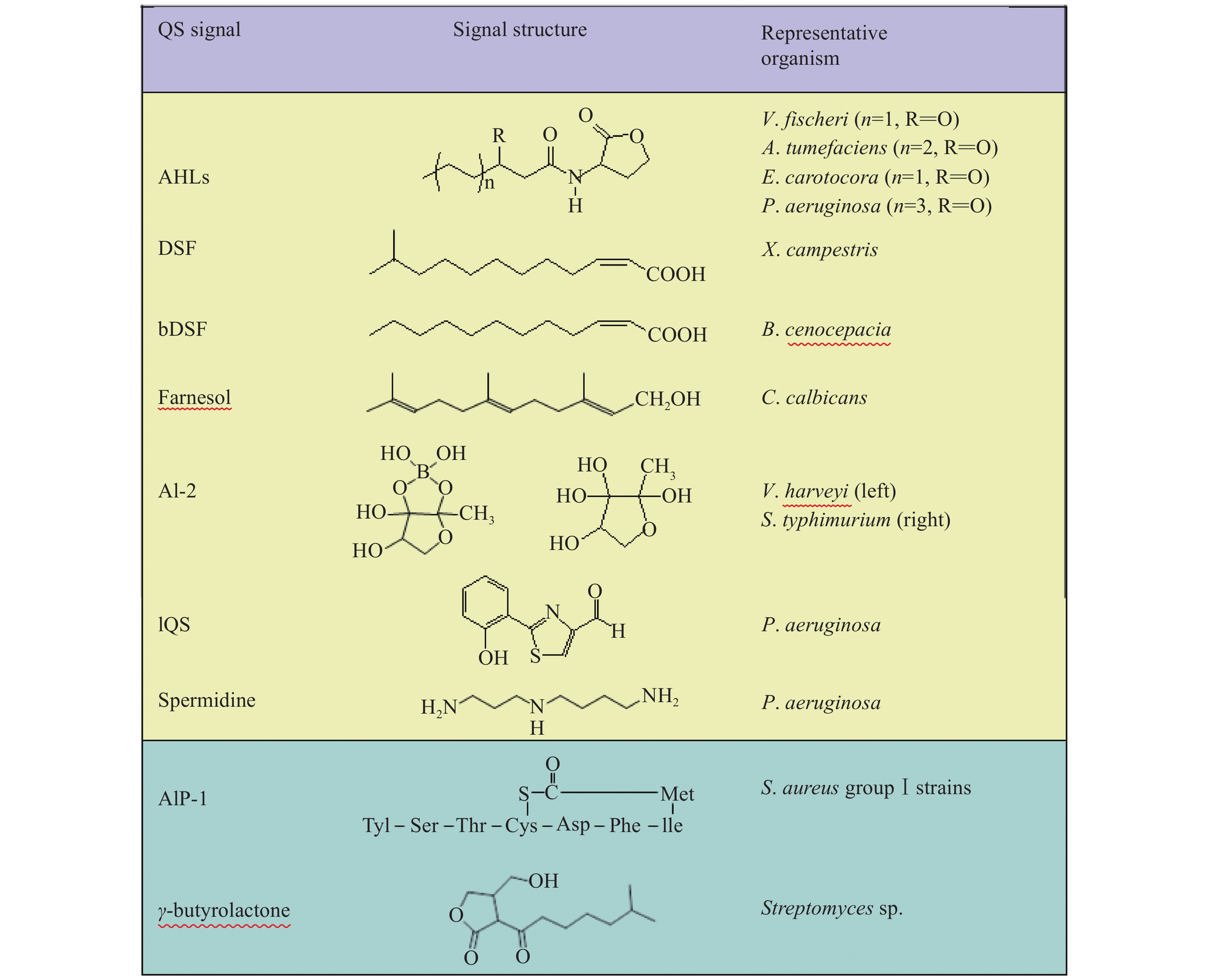
1 从自体诱导到群体感应 1.1 群体感应前期研究群体感应研究的起源至少可以追溯至20世纪中叶,当时美国洛克菲勒研究所和哈佛大学的研究者先后发现肺炎链球菌Stretococcus pneumonia吸收外源DNA分子的能力和费氏弧菌Vibrio fisher生物荧光的产生与细菌的群体密度有关[11-12],称之为细胞密度依赖现象(Cell density dependent phenomenon)。以费氏弧菌为例,在低群体密度时细菌不产生荧光,但当群体密度达到一定阈值时,细菌迅速产生荧光[12]。荧光的产生是由于费氏弧菌产生和感受一种称之为自诱导分子(Autoinducer,AI)的胞外信号,并分离鉴定该信号为含6碳脂肪酸侧链的酰基高丝氨酸内酯(Acyl homoserine lactone,AHL)(图1)[13]。随后的研究克隆鉴定了自诱导分子的合成酶基因luxI,依赖于自诱导分子的调控因子基因luxR以及产生荧光酶有关的基因luxCDABEG[14],luxI和luxCDABEG位于同一个基因簇,表达均受LuxR-AI复合体的正向调控。
|
图 1 代表性群体感应信号及化学结构[13] Fig. 1 Representative quorum sensing signals and chemical structures |
1990年以后,群体感应研究迅速发展。根癌农杆菌Agrobacterium tumefaciens的致病基因大部分位于肿瘤诱导质粒(Tumor inducing plasmid),而肿瘤诱导质粒可以从有致病力的根癌农杆菌菌株转移到无致病力的农杆菌菌株,从而保障和维持了农杆菌群体的整体致病能力,这个过程称之为配合转移(Conjugal transfer)。Zhang和Kerr[15]发现,不同农杆菌菌株的肿瘤诱导质粒的转移效率不同,转移效率高的菌株分泌一个可以在培养基中扩散的配合转移因子(Conjugation factor),诱导转移效率低的菌株进行肿瘤诱导质粒的有效转移。1993年,Zhang等[16]分离提纯了配合转移因子,并通过质谱、核磁共振等分析鉴定,证明配合转移因子是一个含8个碳侧链的AHL家族信号(图1),并在著名国际刊物《Nature》发表论文首次提出AHL类衍生物可能是广泛存在于微生物界调控不同生物功能的小分子信号。在同一期《Nature》中,Piper等[17]也报道了根癌农杆菌致病质粒的水平转移受LuxR同源物TraR的调控,从AHL信号受体这个层面预示了AHL通讯调控系统在微生物界的普遍性。随后,英美科学家分别报道6碳和12碳的AHL信号调控欧文氏软腐病菌Erwinia carotovora和绿脓杆菌Pseudomonas aeruginosa致病基因的表达[18-19],进一步验证了关于AHL信号广泛存在并调控不同生物功能的假说。
1.2 群体感应概念的提出自诱导分子AHL信号调控费氏弧菌生物荧光的产生过程与微生物群体密度有关,也称之为自体诱导(Autoinduction),但“自体诱导”无法直接反映微生物群体密度变化对调控的重要性。1994年,Fuqua等[5]在综述费氏弧菌、哈维氏弧菌Vibrio harveyi、农杆菌和绿脓杆菌产生的AHL家族信号及其生物功能时提出了群体感应(Quorum sensing)这一术语。群体感应从此为微生物学研究工作者广泛采用,用于描述可以监测微生物自身群体密度以协调微生物群体行为的环境传感系统。群体感应调控系统的特点:微生物产生一种可以扩散的自诱导分子或群体感应信号,在生长过程中自诱导分子在周围环境中积累;微生物群体密度低时,群体感应信号保持在低浓度;随着微生物生长,群体感应信号积累到临界浓度,从而诱导目标基因的转录表达。Lee等[20]的研究表明,一种微生物拥有多套群体感应系统、产生多种群体感应信号分子,协调或调控微生物的生物功能。
1.3 AHL 群体感应系统的保守性与调控机制AHL是广泛存在于微生物界的群体感应信号,也是目前研究最多的一种群体感应通讯信号分子,目前已知有超过200种细菌产生AHL家族信号。Dong等[21]报道AHL信号分子均有一个保守的高丝氨酸内酯,但脂肪酸侧链长度和取代基则变化不一。目前已报道的依赖于AHL群体感应通讯系统的生物功能包括:生物荧光的产生、质粒DNA转移、致病因子的产生、生物膜的形成和抗生素的产生等[21]。基因芯片分析表明,在绿脓杆菌中AHL信号可调控数百个基因的表达,包含致病基因、生物膜形成基因和抗生素抗性基因等[22-23]。AHL系统在致病过程中的重要性由此可见一斑。
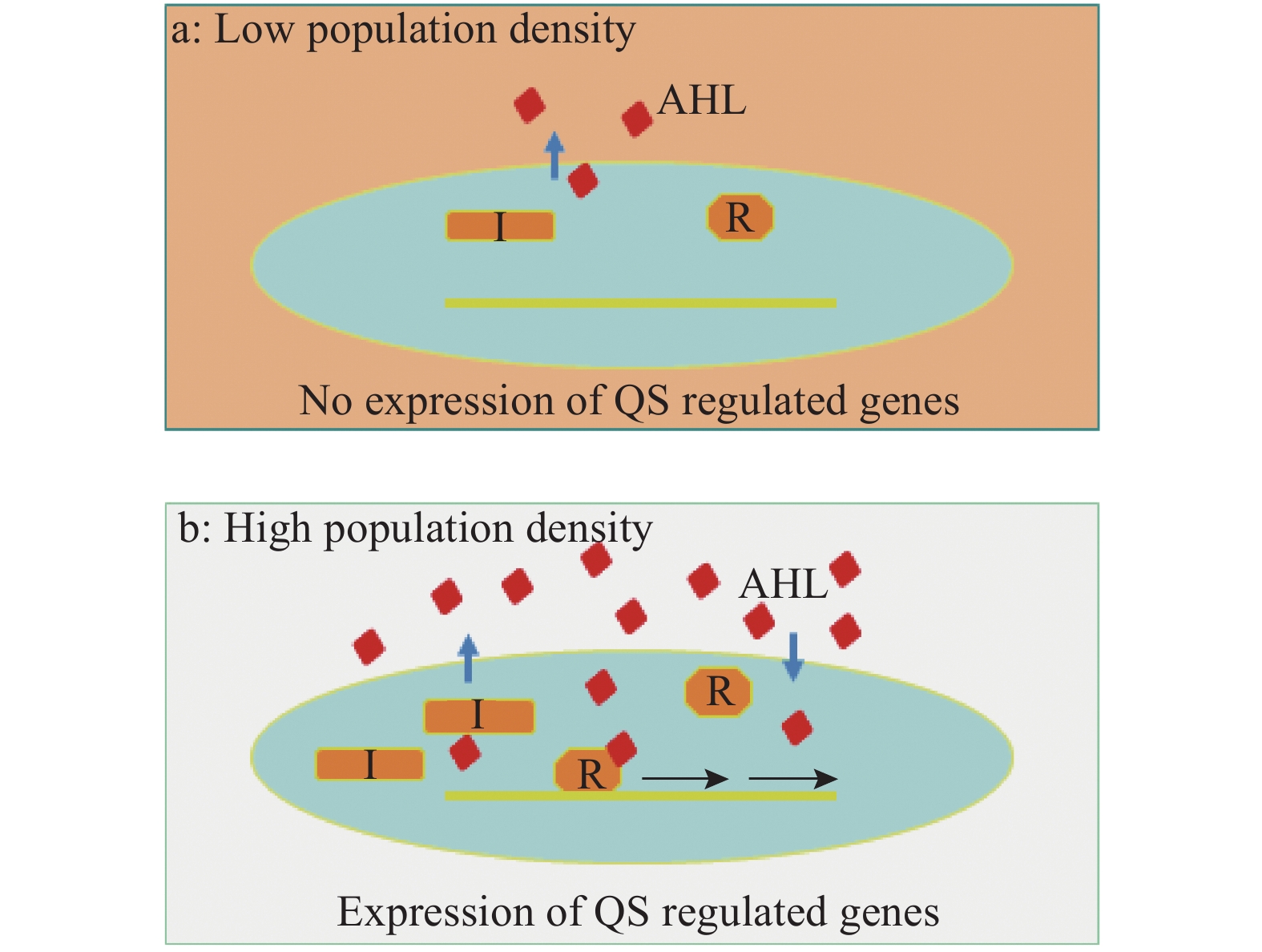
AHL群体感应通讯系统的核心部分由AHL合成酶(I蛋白)和AHL受体(R蛋白)组成。在低细菌群体密度时,I蛋白只合成少量AHL信号分子;随着细菌生长,积累的AHL信号与R蛋白结合形成R蛋白二聚体,进而诱导靶基因的转录表达(图2)。这种群体感应调控机理在细菌中基本保守留用,但是在不同细菌中可能有一定程度的修饰进化[21]。比如在农杆菌中R蛋白基因的表达受植物根瘤特异性代谢产物Opine的诱导控制;绿脓杆菌则有2套AHL系统(las和rhl),其中,LasI产生12碳AHL信号,通过IQS和PQS系统进而调控RhlI产生4碳AHL信号;而在玉米枯萎欧氏杆菌Erwinia stewartii中,AHL信号受体EsaR则是一个负调控转录因子。这些研究表明,AHL群体感应通讯系统在不同细菌中的调控机理可能有所不同,深入研究其调控网络及与其他通讯调控系统的互作将有可能取得原创性的重要发现,有助于阐明病原的致病机理和设计新型特异的病害防控体系。
|
图 2 AHL信号介导的群体感应调控模型[21] Fig. 2 The regulatory model of AHL signal mediated quorum sensing system QS:群体感应;红色方块代表群体感应信号AHL,I蛋白是AHL信号合成酶,R蛋白是信号受体;蓝色箭头指示信号转运方向;黑色箭头显示基因表达 QS: Quorum sensing; Red block represents QS signal AHL, I protein is the AHL synthetase, R protein is the signal receptor; Blue arrow indicates the direction of signal transportation; Black arrow indicates gene expression |
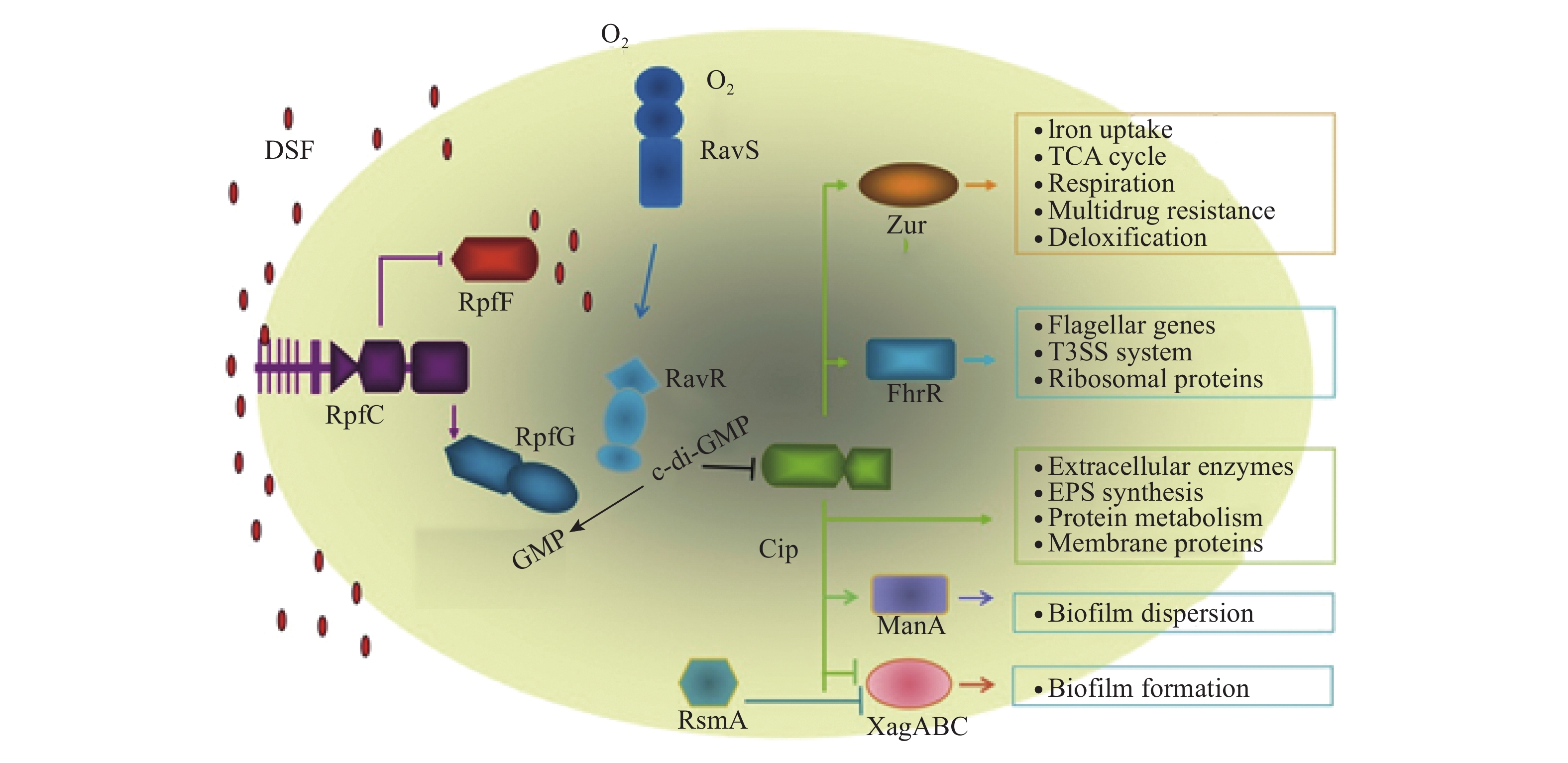
DSF代表了另一类广泛存在于革兰阴性菌中的群体感应通讯系统。英国Daniels实验室发现,野油菜黄单胞杆菌(Xanthomonas campestris pv. campestris,Xcc)可以产生一个扩散信号因子(Diffusible signaling factor,DSF)并调控若干致病因子,包括蛋白酶、纤维素酶和胞外多糖[24-25]。Slater等[25]研究表明,有3个基因与DSF群体感应系统有关,其中,rpfF基因可能编码DSF合成酶,rpfC和rpfG基因则与DSF信号传导有关。Wang等[26]分离鉴定了DSF为顺式−11−甲基−2−十二碳烯酸。到目前为止,已从6个属的革兰阴性细菌中分离鉴定了超过10种结构相似的DSF家族信号[7, 27],推测超过100种细菌可利用DSF调控各种生物功能。DSF系统的生物功能和信号通路在黄单胞杆菌中已进行较深入的研究。He等[28]研究表明,DSF信号通过一个多级分层通讯网络调控包括胞外酶和胞外多糖等致病相关基因在内的300多个基因的表达(图3)。在其他多种微生物中,DSF已知参与致病和生物膜形成的调控[7]。黄单胞杆菌中DSF信号传导通路和分子机理已基本确定:蛋白激酶RpfC感应外源DSF信号后进行自我磷酸化,激活RpfG的磷酸二酯酶活性,从而降解全局调控因子Clp的抑制因子c-di-GMP,激活释放Clp。Clp可以直接调控一系列致病基因的转录,同时通过下游转录因子FhrR和Zur间接调控其他致病基因的表达(图3)[28]。
|
图 3 黄单胞杆菌的群体感应通讯网络[28] Fig. 3 The quorum sensing signaling network of Xanthomonas campestris pv. campestris 红色圆点代表DSF群体感应信号;箭头代表正调控;T型线代表负调控 Red dot represents quorum sensing signal DSF; Arrow represents positive regulation; T bar indicates negative regulation |
新洋葱伯克霍尔德杆菌Burkholderia cenocepacia存在一个保守的RpfF同源蛋白,负责合成DSF家族信号顺式−2−十二碳烯酸(Cis-2-dodecenoic acid,BDSF),但缺少RpfC和RpfG的同源蛋白[29],预示伯克霍尔德杆菌BDSF介导的群体感应系统存在与黄单胞杆菌不一样的信号传导机理和不同的进化起源[7]。Deng等[30]研究表明,在伯克霍尔德杆菌中,BDSF信号的新型受体蛋白RpfR承担了RpfC和RpfG的双重功能——信号感知和信号转导,RpfR这个新型受体蛋白包含PAS、GGDEF和EAL这3个功能域,GGDEF和EAL功能域分别催化c-di-GMP的合成和降解,而PAS功能域则负责感知结合BDSF信号,其结果引起RpfR构象变化、激发EAL功能域的酶活降解c-di-GMP,进而调控下游致病基因的表达。
2.2 依赖于AI-2/LuxS的群体感应系统AI-2(或者更准确地说是其合成酶LuxS)代表了另一类可能相对广泛存在的群体感应系统。哈维氏弧菌不产生AHL群体感应信号的突变体,但可以产生生物荧光,因而推测存在另外一种群体感应信号,并命名为“AI-2”。Surette等[31]的研究发现了AI-2的合成酶基因luxS。 AI-2被认为是一种广泛存在的种间通讯信号,基于luxS 同源基因可以在数百种微生物中找到,并且若干具有luxS 同源基因的其他种类细菌可以诱导哈维氏弧菌产生荧光[32]。
依赖于AI-2的群体感应系统主要参与调控生物膜的合成、细胞运动和致病基因表达。AI-2化学结构不稳定,这给常规化学提取分离带来很大的挑战。2002年Bassler实验室的Chen等[33]利用受体蛋白LuxP对AI-2的高亲和力进行蛋白−配体结晶分析,将哈维氏弧菌的AI-2鉴定为带一个硼酸分子的S−2−甲基−2,3,3,4−四羟基四氢呋喃环型化合物。但是,用同样的方法鉴定发现,沙门氏菌Salmonella enterica ssp. enterica serovar trphimurium的AI-2却是无硼酸分子的R−2−甲基−2,3,3,4−四羟基四氢呋喃[34]。说明在微生物体内AI-2衍生物之间也许可以进行快速的结构变换。
2.3 革兰阳性细菌群体感应系统革兰阴性细菌中群体感应现象的发现,推动了革兰阳性细菌群体感应系统的研究。与革兰阴性细菌群体感应信号基本都是小分子化合物不同,一部分革兰阳性细菌的群体感应信号是翻译后加工的(有时是修饰的)分泌肽;另一部分阳性细菌则是小分子化合物。目前,研究得比较清楚的是γ−丁内酯(AHL结构同系物)(图1),这个小分子化合物是链霉菌属Streptomyces物种中调控抗生素产生的关键调节信号[35-36]。
金黄色葡萄球菌Staphylococcus aureus是医院内主要的病原体之一,对其群体感应系统的研究详细说明了病原菌是如何利用小分子短肽信号调控致病基因的表达。JI等[37]研究发现,金黄色葡萄球菌致病基因的表达受细菌细胞密度的影响。Mayville等[38]证明,由agrD基因编码的前肽通过膜蛋白AgrB加工和分泌产生成熟自诱导肽(AIP),后者与agrC编码的跨膜受体AgrC结合,AIP-AgrC的结合触发标准的双组分磷酸化信号转导过程,激活其响应调控蛋白AgrA,进而通过RNAIII诱导大多数毒力基因的表达。AIP经高压液相色谱分离、质谱鉴定和化学合成验证,被证明是一个由8个氨基酸组成的环状短肽[37-38]。Magnuson等[39]研究发现,金黄色葡萄球菌这种依赖于自诱导肽的群体感应系统与枯草芽孢杆菌调控遗传感受态(Genetic competence)的群体感应系统极为相似。说明这类以短肽作为信号的群体感应系统在细菌进化的早期就已经存在了。
2.4 真菌群体感应系统群体感应是微生物群落中分子通讯的一种形式,在细菌种类中相对研究得比较透彻,但在真菌中却知之甚少。金合欢醇(Farnesol)是由机会性人类致病真菌白色念珠菌Candida albicans分泌的群体感应分子,是真核生物中描述的第一个群体感应分子。白色念珠菌通常以酵母和菌丝2种形式存在,并且互相转换。白色念珠菌的细胞形态取决于初始细胞密度,在其他条件相同的情况下,以细胞密度≥106 mL−1的白色念珠菌接种后产生出酵母状真菌细胞,用细胞密度<106 mL−1的白色念珠菌接种则产生出胚芽管和菌丝体,这种现象被称为接种剂量效应。高密度的白色念珠菌培养液中存在一种群体感应分子(QSM),QSM的产生不依赖于碳源的类型,也不依赖于氮源或培养基的化学性质,且可在生长期间(23~43 ℃)连续产生。Hornby等[40]通过色谱分离和质谱鉴定证明金合欢醇是调控白色念珠菌形态转换的关键信号分子。但至今,白色念珠菌通过金合欢醇调控酵母−菌丝二态性生长的分子机理尚有待阐明.
2.5 集成型群体感应系统集成型群体感应系统IQS的发现表明了群体感应系统的复杂性和可塑性[41],扩展了群体感应和逆境响应机制的范围。集成型群体感应系统首先在绿脓杆菌中发现。绿脓杆菌是一种机会致病菌,对于患有囊性纤维化的个体和免疫系统受损的患者具有极强的侵染力、甚至引起死亡。绿脓杆菌进化形成了一个复杂的群体感应网络来调节细菌的毒力,该网络由3个群体感应系统组成:las、rhl和pqs。las和rhl系统涉及2种酰基高丝氨酸内酯合酶——LasI和RhlI,它们产生QS信号N−3−氧代十二烷酰基高丝氨酸内酯(3OC12HSL)和N−丁酰基高丝氨酸内酯(C4HSL)。这2个信号随着细菌群体生长被释放到细胞间的环境中,当积累达到阈值浓度时,分别结合并活化其细胞内同源受体LasR和RhlR,从而调节相应靶基因的表达。而pqs系统则使用烷基喹诺酮信号2−庚基−3−羟基−4(1H)−喹诺酮(PQS)和2−庚基−4−羟基喹啉顶部,控制rhl和pqs系统的表达。临床中经常分离检测到绿脓杆菌lasI和lasR的突变体[42-43],这促使我们寻找一种可能在功能上取代las系统的机制。Lee等[20]研究证实,绿脓杆菌确实存在这种细胞通讯系统,其信号被命名为“IQS”,化学结构鉴定为2−(2−羟基苯基)−噻唑−4−甲醛,属于一类新的群体感应信号分子。IQS生物合成的破坏使pqs和rhl QS系统瘫痪、细菌毒力显著减弱。在正常培养条件下,IQS的产生受las严格控制,但也被磷酸耗竭逆境所激活,磷酸耗竭是细菌在感染期间常常遇到的逆境信号。表明IQS系统能将中央las系统和磷酸逆境响应机制连接到下游的pqs和rhl调节系统。
3 群体感应的作用机理 3.1 群体感应对微生物生物膜生长发育的调控自然界中的细菌通常作为固定不动的群落存在,称为生物膜,这些群落在形态和生理上形成与自由浮游生活细菌不同的结构。生物膜的形成显著地增强微生物对逆境包括抗生素和其他杀生物剂的抵抗能力。在很长一段时间,是否存在一个特定的调控系统调控生物膜的形成存在争议。微生物群体感应现象的揭示,为阐明影响微生物生物膜生长发育的调控系统提供了新的途径。1998年,Davies等[44]首次证明AHL群体感应信号参与绿脓杆菌生物膜的发育;AHL信号合成酶基因lasI突变体形成扁平未分化的生物膜,与野生型结构分明的生物膜不同,但与野生型相比,它对杀生物剂十二烷基硫酸钠显著敏感;当合成的AHL信号分子存在时,突变体恢复形成正常的生物膜结构。
与AHL群体感应信号正向调控微生物生物膜的形成不同,以DSF为代表的另一类广泛存在的群体感应信号则参与调控生物膜的降解。在植物病原细菌黄单胞杆菌中,DSF合成酶基因rpfF的突变体形成生物膜多聚体,加入DSF后,rpfF突变体的生物膜多聚体消失,突变体以单细胞形态自由浮游生长[45-46]。这是因为DSF诱导产生β−1,4−甘露聚糖酶(ManA),降解了生物膜。He等[46]发现,在培养基中补充DSF后,DSF合成酶RpfF与ManA的双重缺失突变体ΔrpfFΔmanA同样可以以单细胞浮游形式生长,表明除了调节manA表达外,DSF还控制与生物膜生长发育有关的其他机制。Tao等[47]的研究证明了上述推测,受DSF负调控的xagABC编码的糖基转移酶负责黄单胞杆菌生物膜的合成,删除xag基因导致细胞外产生的多糖减少,破坏了黄单胞杆菌生物膜形成并减弱了细菌对氧化应激的抵抗力。可见,黄单胞杆菌可以通过群体感应信号,负调控与生物膜形成有关的糖基转移酶XagABC的表达,正向诱导与生物膜降解有关的糖基水解酶ManA的产生,从而有效地调控生物膜的形成与降解,这对于保障病原菌侵入寄主植物体内并随后进行系统扩散侵染可能有非常重要的意义。
3.2 群体淬灭理论提出与证实基于群体感应信号在产生抗生素和致病过程中的重要作用,推测微生物在互作竞争进化的过程中可能会形成有效对抗群体感应的机制。Dong等[10]和Lin等[48]从不同的土壤、植物样本中分离各种微生物菌株,建立了可靠的AHL降解反应培养条件,利用AHL的报告菌株检测AHL信号的降解情况,并发现了能高效降解AHL信号分子的AHL内酯酶AiiA和AHL酰基转移酶AiiD。这些群体感应信号降解酶被称为“群体淬灭酶”[8, 49]。Dong等[8]利用转基因植物证明,表达群体淬灭酶可以有效地防控欧文氏软腐病菌引起的作物软腐病。随后,又进一步证明群体淬灭是一种有效的病害生防机制[9]。目前已报道的具有淬灭群体感应通讯功能的物质还有各种小分子化学抑制剂[21, 50-51]。这些小分子抑制剂大部分是群体感应通讯信号的结构衍生物,主要针对AHL群体感应通讯系统,作用机理包括阻断信号产生和识别、干扰信号交流和信号陷阱等。
通过阻断群体感应通讯以实现病害防控的策略,同样适用于寄主−病原跨界通讯系统。在证明了人和动物体内的多胺分子是诱导绿脓杆菌关键致病因子III型分泌系统表达所必须的信号[52]之后,Wu等[53]分别利用信号和信号受体作为靶标,设计病原防控制剂,完成了亚精胺受体的蛋白结构分析;Wang等[54]根据其结构特点合成了一系列多胺衍生物,明确了结构−活性关系,筛选得到一个高效专一的亚精胺跨界通讯抑制剂。2018年,Wang等[55]针对多胺信号制作了专一性强、效价高的单克隆抗体,证明用单克隆抗体同样可以有效地阻断亚精胺跨界通讯,显著地降低了绿脓杆菌侵染引起的试验动物的死亡率。
4 结论与展望微生物群体感应系统是微生物学研究的重大发现之一,但目前仅在少数模式细菌中有较为系统的研究,这些研究极大地增进了人们对微生物致病调控机理的了解,也说明了研究微生物群体感应系统的重要性和复杂性。对绿脓杆菌研究结果表明,约90%的致病毒力表达受las群体感应系统、spd寄主−病原跨界通讯系统和iqs集成型群体感应系统的综合诱导调控。很多微生物病原尤其是真菌病原的群体感应系统和寄主−病原跨界通讯系统的信号分子尚未鉴定,信号通路及调控机理也尚未查明。可以预见,在小分子分离鉴定和蛋白结构分析技术日益成熟、在各种组学技术飞速发展的后基因组时代,微生物通讯系统的研究将继续是微生物学研究的重中之重,交叉学科协同攻关将有利于阐明微生物基因表达的调控网络和调控机理、有利于揭示微生物彼此之间互作竞争的作用机制、有利于明确寄主和环境因素影响相关基因表达的分子机理。这些研究成果也将有效地扩展和丰富我们设计绿色安全病害防控措施的思维与视野。
综上所述,微生物群体感应通讯系统研究的生命力在于其能够揭示影响微生物重要生命过程的调控网络、在于其能够为设计绿色安全病害防控制剂提供关键的理论基础和新型靶标。值得关注的是,群体感应通讯系统不仅参与微生物致病基因的表达调控,而且也直接影响微生物的抗药性[56-57]。因此,深入开展微生物之间的信息交流以及病原菌与寄主间的信息通讯系统研究可望取得原创性的重大突破,具有重大的科学意义和应用价值:
1)以细菌和真菌群体感应通讯系统以及病原−寄主跨界通讯系统的重大科学问题为核心进行研究,有助于全方位建立微生物群体感应通讯系统创新研究的科学体系,有助于创建微生物群体感应通讯系统调控的新理论、新思路与新方法,有助于丰富和发展微生物学科的相关基础理论和技术。
2)以微生物群体感应通讯系统领域的科学前沿为突破口,将可加深人们对病原微生物和生防微生物目标性状与基因调控机理的认识,揭示群体感应通讯系统在病原−寄主互作过程中的功能与生物学基础,促进微生物学与植物保护学、遗传学等其他学科的交叉渗透和共同发展。
3)群体感应、跨界通讯和群体淬灭的知识创新,将为病害防控提出新思路和新措施,为减少农(兽)药的使用、发展新型绿色安全环保农(兽)药和实现微生物制剂的更新换代提供关键的理论基础和技术支撑,为防控人类微生物病害、克服微生物抗药性问题提供有益的借鉴。
| [1] |
杲修杰, 王正华, 曹孟良. 植物抗病基因研究进展[J]. 长江大学学报(自然科学版), 2006, 3(4): 205-210. DOI:10.3969/j.issn.1673-1409.2006.04.022 (  0) 0) |
| [2] |
陈爱平, 刘福林, 吴凡修. 2010年水产养殖病害发生情况与2011年流行趋势分析[J]. 中国水产, 2011(3): 56-59. DOI:10.3969/j.issn.1002-6681.2011.03.025 (  0) 0) |
| [3] |
崔向阳, 樊景凤, 林凤翱, 等. 海水养殖鱼类病害的研究进展[EB/OL]. 北京: 中国科技论文在线[2008-03-11]. http://www.paper.edu.cn/releasepaper/content/200803-222.
(  0) 0) |
| [4] |
赵超英. 食品中农药和兽药残留对人体的危害[J]. 中国全科医学, 2006(13): 1086-1087. DOI:10.3969/j.issn.1007-9572.2006.13.020 (  0) 0) |
| [5] |
FUQUA W C, WINANS S C, GREENBERG E P. Quorum sensing in bacteria: The LuxR-LuxI family of cell density-responsive transcriptional regulators[J]. J Bacteriol, 1994, 176: 269-275. DOI:10.1128/jb.176.2.269-275.1994 (  0) 0) |
| [6] |
ZHANG L H. Quorum quenching and proactive host defense[J]. Trends Plant Sci, 2003, 8: 238-244. DOI:10.1016/S1360-1385(03)00063-3 (  0) 0) |
| [7] |
DENG Y, WU J, TAO F, et al. Listening to a new language: DSF-based quorum sensing in Gram-negative bacteria[J]. Chem Rev, 2011, 111: 160-173. DOI:10.1021/cr100354f (  0) 0) |
| [8] |
DONG Y H, WANG L H, XU J L, et al. Quenching quorum sensing-dependent bacterial infection by an N-acyl homoserine lactonase
[J]. Nature, 2001, 411: 813-817. DOI:10.1038/35081101 (  0) 0) |
| [9] |
DONG Y H, ZHANG X F, XU J L, et al. Insecticidal Bacillus thuringiensis silences Erwinia carotovora virulence by a new form of microbial antagonism-signal interference
[J]. Appl Environ Microbiol, 2004, 70: 954-960. DOI:10.1128/AEM.70.2.954-960.2004 (  0) 0) |
| [10] |
DONG Y H, XU J L, LI X Z, et al. AiiA, an enzyme inactivates acyl homoserine-lactone quorum-sensing signal and attenuates the virulence of Erwinia carotovora
[J]. Proc Natl Acad Sci USA, 2000, 97: 3526-3531. DOI:10.1073/pnas.97.7.3526 (  0) 0) |
| [11] |
TOMASZ A, HOTCHKISS R D. Regulation of the transformability of Pseumococcal cultures by macromolecular cell products
[J]. Proc Natl Acad Sci USA, 1964, 51: 480-487. DOI:10.1073/pnas.51.3.480 (  0) 0) |
| [12] |
NEALSON K H, PLATT T, HASTINGS J W. Cellular control of the synthesis and activity of the bacterial luminescent system[J]. J Bacteriol, 1970, 104: 313-322. (  0) 0) |
| [13] |
EBERHARD A, BURLINGAME A L, EBERHARD C, et al. Structural identification of autoinducer of Photobacterium fischeri luciferase
[J]. Biochem, 1981, 20: 2444-2449. DOI:10.1021/bi00512a013 (  0) 0) |
| [14] |
ENGEBRECHT J, NEALSON K, SILERMAN M. Bacterial bioluminescence: isolation and genetic analysis of functions from Vibrio fisheri
[J]. Cell, 1983, 32: 773-781. DOI:10.1016/0092-8674(83)90063-6 (  0) 0) |
| [15] |
ZHANG L H, KERR A. A diffusible compound can enhance conjugal transfer of Ti plasmid in Agrobacterium tumefaciens
[J]. J Bacteriol, 1991, 173: 1867-1872. DOI:10.1128/jb.173.6.1867-1872.1991 (  0) 0) |
| [16] |
ZHANG L H, MURPHY P, KERR A, et al. Agrobacterium conjugation and gene regulation by N-acyl-L-homoserine lactones
[J]. Nature, 1993, 362: 446-447. DOI:10.1038/362446a0 (  0) 0) |
| [17] |
PIPER K R, VON BODMAN S B, FARRAND SK. Conjugation factor of Agrobacterium tumefaciens regulates Ti plasmid transfer by autoinduction
[J]. Nature, 1993, 362: 448-450. DOI:10.1038/362448a0 (  0) 0) |
| [18] |
JONES S, YU B, BAINTON N J, et al. The lux autoinducer regulates the production of exoenzyme virulence determinants in Erwinia carotovora and Pseudomonas aeruginosa
[J]. EMBO J, 1993, 12: 2477-2482. DOI:10.1002/embj.1993.12.issue-6 (  0) 0) |
| [19] |
PEARSON J P, GARY K M, Passador L, et al. Structure of the autoinducer required for expression of Pseudomonas aeruginosa virulence genes
[J]. Proc Natl Acad Sci USA, 1994, 91: 197-201. DOI:10.1073/pnas.91.1.197 (  0) 0) |
| [20] |
LEE J, WU J, DENG Y, et al. A cell-cell communication signal integrates quorum sensing and stress response[J]. Nature Chem Biol, 2013, 9: 339-343. DOI:10.1038/nchembio.1225 (  0) 0) |
| [21] |
DONG Y H, WANG L H, ZHANG L H. Quorum quenching microbial infections mechanisms and implications[J]. Phil Trans R Soc B, 2007, 362: 1201-1211. DOI:10.1098/rstb.2007.2045 (  0) 0) |
| [22] |
SCHUSTER M, LOSTROH C P, OGI T, et al. Identification, timing, and signal specificity of Pseudomonas aeruginosa quorum-controlled genes: A transcriptome analysis
[J]. J Bacteriol, 2003, 185: 2066-2079. DOI:10.1128/JB.185.7.2066-2079.2003 (  0) 0) |
| [23] |
WAGNER V E, BUSHNELL D, PASSADOR L, et al. Microarray analysis of Pseudomonas aeruginosa quorum-sensing regulons: Effects of growth phase and environment
[J]. J Bacteriol, 2003, 185: 2080-2095. DOI:10.1128/JB.185.7.2080-2095.2003 (  0) 0) |
| [24] |
BARBER C E, TANG J L, FENG J X, et al. A novel regulatory system required for pathogenicity of Xanthomonas campestris is mediated by a small diffusible signal molecule
[J]. Mol Microbiol, 1997, 24: 556-566. (  0) 0) |
| [25] |
SLATER H, ALVAREZ-MORALES A, BARBER C E, et al. A two-component system involving an HD-GYP domain protein links cell-cell signaling to pathogenicity gene expression in Xanthomonas campestris
[J]. Mol Microbiol, 2000, 38: 986-1003. (  0) 0) |
| [26] |
WANG L H, HE Y W, GAO Y F, et al. A bacterial cell-cell communication signal with cross-kingdom structural analogs[J]. Mol Microbiol, 2004, 51: 903-912. (  0) 0) |
| [27] |
ZHOU L, ZHANG L H, CÁMARA M, et al. The DSF family of quorum sensing signals: Diversity, biosynthesis, and turnover[J]. Trends Microbiol, 2017, 25: 293-303. DOI:10.1016/j.tim.2016.11.013 (  0) 0) |
| [28] |
HE Y W, ZHANG L H. Quorum sensing and virulence regulation in Xanthomonas campestris
[J]. FEMS Microbiol Rev, 2008, 32: 842-857. DOI:10.1111/j.1574-6976.2008.00120.x (  0) 0) |
| [29] |
BOON C, DENG Y Y, WANG L H, et al. A novel DSF-like signal from Burkholderia cenocepacia interferes with Candida albicans morphological transition
[J]. ISME J, 2008, 2: 27-36. DOI:10.1038/ismej.2007.76 (  0) 0) |
| [30] |
DENG Y, SCHMID N, WANG C, et al. Cis-2-dodecenoic acid receptor RpfR links quorum-sensing signal perception with regulation of virulence through cyclic dimeric quanosine monophosphate turnover[J]. Proc Natl Acad Sci USA, 2012, 109: 15479-15484. DOI:10.1073/pnas.1205037109 (  0) 0) |
| [31] |
SURETTE M G, MILLER M B, BASSLER B L. Quorum sensing in Escherichia coli, Salmonella typhimurium, and Vibrio harveyi: A new family of genes responsible for autoinducer production
[J]. Proc Natl Acad Sci USA, 1999, 96: 1639-1644. DOI:10.1073/pnas.96.4.1639 (  0) 0) |
| [32] |
BASSLER B L. How bacteria talk to each other: Regulation of gene expression by quorum sensing[J]. Curr Opin Microbiol, 1999, 2: 582-587. DOI:10.1016/S1369-5274(99)00025-9 (  0) 0) |
| [33] |
CHEN X, SCHAUDER S, POTIER N, et al. Structural identification of a bacterial quorum sensing signal containing boron[J]. Nature, 2002, 415(6871): 545-549. DOI:10.1038/415545a (  0) 0) |
| [34] |
MILLER S T, XAVIER K B, CAMPAGNA S R, et al. Salmonella typhimurium recognizes a chemically distinct form of the bacterial quorum-sensing signal AI-2
[J]. Mol Cell, 2004, 15(5): 677-687. DOI:10.1016/j.molcel.2004.07.020 (  0) 0) |
| [35] |
KATO J Y, FUNA N, WATANABE H, et al. Biosynthesis of gamma-butyrolactone autoregulators that switch on secondary metabolism and morphological development in Streptomyces
[J]. Proc Natl Acad Sci USA, 2007, 104: 2378-2383. DOI:10.1073/pnas.0607472104 (  0) 0) |
| [36] |
WANG J, WANG W, WANG L, et al. A novel role of pseudo γ-butyrolactone receptors in controlling γ-butyrolactone biosynthesis in Streptomyces
[J]. Mol Microbiol, 2011, 82: 238-250. (  0) 0) |
| [37] |
JI G, BEAVIS R C, NOVICK R P. Cell-density control of staphylococcal virulence mediated by an octapeptide pheromone[J]. Proc Natl Acad Sci USA, 1995, 92: 12055-12059. DOI:10.1073/pnas.92.26.12055 (  0) 0) |
| [38] |
MAYVILLE P, JI G, BEAVIS R, et al. Structure-activity analysis of synthetic autoinducing thiolactone peptide from Staphylococcus aureus responsible for virulence
[J]. Proc Natl Acad Sci USA, 1999, 96: 1218-1223. DOI:10.1073/pnas.96.4.1218 (  0) 0) |
| [39] |
MAGNUSON R, SOLOMON J, GROSSMAN A D. Biochemical and genetic characterization of a competence pheromone from B. subtilis
[J]. Cell, 1994, 77: 207-216. DOI:10.1016/0092-8674(94)90313-1 (  0) 0) |
| [40] |
HORNBY J M, JENSEN E C, LISEC A D, et al. Quorum sensing in the dimorphic fungus Candida albicans is mediated by farnesol
[J]. Appl Environ Microbiol, 2001, 67: 2982-2992. DOI:10.1128/AEM.67.7.2982-2992.2001 (  0) 0) |
| [41] |
LEE J, ZHANG L H. The hierarchy quorum sensing network in Pseudomonas aeruginosa
[J]. Protein Cell, 2015, 6: 26-41. (  0) 0) |
| [42] |
HOFFMAN L R, KULASEKARA H D, EMERSON J, et al. Pseudomonas aeruginosa lasR mutants are associated with cystic fibrosis lung disease progression
[J]. J Cyst Fibros, 2009, 8: 66-70. DOI:10.1016/j.jcf.2008.09.006 (  0) 0) |
| [43] |
SMITH E E, BUCKLEY D G, WU Z, et al. Genetic adaptation by Pseudomonas aeruginosa to the airways of cystic fibrosis patients
[J]. Proc Natl Acad Sci USA, 2006, 103: 8487-8492. DOI:10.1073/pnas.0602138103 (  0) 0) |
| [44] |
DAVIES D G, PARSEK M R, PEARSON J P, et al. The involvement of cell-to-cell signals in the development of a bacterial biofilm[J]. Science, 1998, 280: 295-298. DOI:10.1126/science.280.5361.295 (  0) 0) |
| [45] |
DOW J M, CROSSMAN L, FINDLAY K, et al. Biofilm dispersal in Xanthomonas campestris is controlled by cell-cell signaling and is required for full virulence to plants
[J]. Proc Natl Acad Sci USA, 2003, 100: 10995-11000. DOI:10.1073/pnas.1833360100 (  0) 0) |
| [46] |
HE Y W, XU M, LIN K,et al. Genome scale analysis of DSF regulon in Xanthomonas campestris pv. campestris: Identification of novel cell-cell communication-dependent genes and functions
[J]. Mol Microbiol, 2006, 59: 610-622. DOI:10.1111/j.1365-2958.2005.04961.x (  0) 0) |
| [47] |
TAO F, SWARUP S, ZHANG L H. Quorum sensing modulation of a putative glycosyltransferase gene cluster essential for Xanthomonas campestris biofilm formation
[J]. Environ Microbiol, 2010, 12: 3159-3170. DOI:10.1111/emi.2010.12.issue-12 (  0) 0) |
| [48] |
LIN Y H, XU J L, HU J, et al. Acyl-homoserine lactone acylase from Ralstonia strain XJ12B represents a novel and potent class of quorum quenching enzymes
[J]. Mol Microbiol, 2003, 47: 849-860. DOI:10.1046/j.1365-2958.2003.03351.x (  0) 0) |
| [49] |
DONG Y H, ZHANG L H. Quorum sensing and quorum-quenching enzymes[J]. J Microbiol, 2005, 43: 101-109. (  0) 0) |
| [50] |
ZHANG L H, DONG Y H. Quorum sensing and signal interference: Diverse implications[J]. Mol Microbiol, 2004, 53: 1563-1571. DOI:10.1111/j.1365-2958.2004.04234.x (  0) 0) |
| [51] |
GRANDCLÉMENT C, TANNIÈRES M, MORÉRA S, et al. Quorum quenching: Roles in nature and applied developments[J]. FEMS Microbiol Rev, 2016, 40: 86-116. DOI:10.1093/femsre/fuv038 (  0) 0) |
| [52] |
ZHOU L, WANG J, ZHANG L H. Modulation of bacterial type III secretion system by a spermidine transporter dependent signaling pathway[J]. PLoS One, 2007, 2: e1291. DOI:10.1371/journal.pone.0001291 (  0) 0) |
| [53] |
WU D, LIM S C, DONG Y, et al. Structural basis of substrate binding specificity revealed by the crystal structures of polyamine receptors SpuD and SpuE from Pseudomonas aeruginosa
[J]. J Mol Biol, 2012, 416: 697-712. DOI:10.1016/j.jmb.2012.01.010 (  0) 0) |
| [54] |
WANG C, LIU X, WANG J, et al. Design and characterization of a polyamine derivative inhibiting the expression of type II secretion system in Pseudomonas aeruginosa
[J]. Sci Rep-UK, 2016, 6: 30949. DOI:10.1038/srep30949 (  0) 0) |
| [55] |
WANG J H, WANG J, ZHANG L H. Immunological blocking of spermidine-mediated host-pathogen communication provides effective control against Pseudomonas aeruginosa infection[J/OL]. Microbiol Biotech, 2018, https://doi.org/10.1111/1751-7915.13279.
(  0) 0) |
| [56] |
陈昱帆, 刘诗胤, 梁志彬, 等. 群体感应与微生物耐药性[J]. 遗传, 2016, 38(10): 881-893. (  0) 0) |
| [57] |
梁志彬, 陈豫梅, 陈昱帆, 等. RND家族外排泵及其与微生物群体感应的关系[J]. 遗传, 2016, 38(10): 894-901. (  0) 0) |
 2019, Vol. 40
2019, Vol. 40

