2. 彭阳县畜牧技术推广服务中心,宁夏 彭阳 756599;
3. 宁夏大学 生命科学学院/宁夏饲料工程技术研究中心,宁夏 银川 750021
2. Animal Husbandry and Technology Promotion Service Center of Pengyang County, Pengyang 756599, China;
3. School of Life Science, Ningxia University/ Ningxia Feed Engineering Technology Research Center, Yinchuan 750021, China
静原鸡主要分布于宁夏彭阳县和甘肃静宁县,2006年被农业部认定为地方优良品种,已被列入国家级畜禽遗传资源保护名录[1],根据羽色的不同,分为白羽、麻羽和黑羽3个群体。由于长期处于气候高寒湿润、地形起伏、牧草及昆虫众多的生活环境和优越的地理位置,静原鸡具有耐粗饲、抗逆性强、氨基酸含量丰富、肉质细嫩、营养和滋补价值高等特点,尤其多不饱和脂肪酸(二十碳五烯酸、二十二碳六烯酸)含量较高[2],符合现今人们对高品质鸡肉的要求,属鸡肉中优选的绿色食品[3]。
腺苷酸激酶(Adenylate kinase, AK)是一种普遍存在于动植物体内的单体酶,对生物的生长和维持至关重要[4],主要调节腺嘌呤核苷酸代谢,催化反应:ATP+AMP↔2ADP,在维持细胞能量平衡中起着不可或缺的作用[5]。在哺乳动物中,有几种AK亚型具有组织特异性分布和独特的亚细胞定位[6],其中AK1蛋白被认为是骨骼肌细胞质中的主要AK亚型[7]。猪心脏中胞质酶AK1蛋白的三维结构已经被Schulz等[8]和Sachsenheimer等[9]准确测定。有研究表明,AK1基因缺失的小鼠尽管肌肉形成正常,但由于ADP的异常积累会导致骨骼肌松弛延迟[10]。此外,还有研究发现AK1蛋白磷酸化可能是质膜线粒体和KATP通道之间传递信号所必需的[11]。目前关于AK1基因的研究集中在与溶血性贫血相关的罕见遗传疾病中,国内外将AK1作为肌苷酸影响基因及有关AK1基因结构及功能预测的研究鲜有报道。
本研究通过对宁夏优良地方品种静原鸡AK1基因CDS区序列进行扩增、克隆、构建其真核表达载体,运用生物信息学分析方法预测其理化性质、亲水性/疏水性、跨膜结构域、磷酸化位点、亚细胞定位、磷酸化位点、B细胞抗原表位、基因共表达、CpG岛、蛋白的空间结构等,为后续深入研究AK1基因蛋白水平、代谢水平和细胞功能研究等的调控机理和表达模式提供科学依据,并为我国地方品种鸡的分子育种技术平台奠定基础。
1 材料与方法 1.1 试验材料与试剂随机屠宰宁夏彭阳县朝那鸡繁育中心180日龄静原鸡公、母各15只(饲养管理条件相同),采集腿肌、胸肌于液氮罐中,带回实验室于−80 ℃保存备用。试剂:Trizo,Hifair®Ⅱ1st Strand cDNA Synthesis SuperMix for qPCR(gDNA digester plus)试剂盒(上海翊圣生物公司),DNA loading buffer(百泰克),核酸染料(索莱宝),pMD18-T、DH5α、质粒小提中量试剂盒、普通琼脂糖凝胶DNA回收试剂盒(天根),T4连接酶(NEB),EcoRⅠ、BamHⅠ(宝生物有限公司)。
1.2 试验方法 1.2.1 总RNA的提取及反转录通过传统Trizo(Invitrogen, USA)法提取静原鸡腿肌、胸肌的总RNA,并对其RNA的纯度、完整性、浓度进行检测。采用Hifair®Ⅱ1st Strand cDNA Synthesis SuperMix for qPCR(gDNA digester plus)试剂盒合成cDNA后,于−20 ℃保存备用。
1.2.2 AK1基因的引物设计根据GenBank上已公布的原鸡AK1基因序列,利用Primer 5.0软件设计特异性引物(表1),并送至生工生物工程(上海)股份有限公司合成。
|
|
表 1 静原鸡AK1基因CDS区引物序列 Table 1 Primer sequence for CDS region in AK1 gene of Jingyuan chicken |
PCR扩增总体系为20 μL:cDNA样品1 μL,上、下游引物各0.5 μL,Taq PCR Master Mix 11 μL,ddH2O 7 μL。AK1基因CDS区PCR扩增程序为:94 ℃预变性5 min;94 ℃变性45 s,退火40 s,72 ℃延伸45 s,共31个循环;72 ℃延伸10 min,4 ℃保存。PCR产物通过10 g/L的琼脂糖凝胶电泳检测后,使用普通琼脂糖凝胶DNA回收试剂盒对目的片段进行回收。
将回收纯化好的目的片段与pMD18-T载体4 ℃下连接并过夜。将连接好的带有pMD18-T载体的目的片段转化到DH5α感受态细胞中,冰浴30 min,42 ℃热激90 s,冰浴3 min,加入无抗液体LB培养基,混匀后置于37 ℃摇床150 r/min振荡培养45 min,涂布于含氨苄抗性的LB平板培养基上,37 ℃条件下培养12~16 h,随机挑取5个单菌落放入含氨苄抗性的LB液体培养基220 r/min震荡培养8 h,菌液PCR扩增。收集菌液送至生工生物工程(上海)股份有限公司进行测序。
1.2.4 AK1载体的构建引物设计合成见“1.2.2”,扩增回收同“1.2.3”,选择pEGFP-N1真核表达载体进行质粒提取。利用EcoRⅠ、BamHⅠ对AK1基因与pEGFP-N1质粒进行双酶切,双酶切体系为50 μL,具体加入量分别为:11 μL ddH2O,5 μL 10×Buffer,2 μL EcoRⅠ,2 μL BamHⅠ,30 μL重组质粒(目的片段)。37 ℃酶切6 h后使用普通琼脂糖凝胶DNA回收试剂盒回收pEGFP-N1载体片段和AK1目的片段,AK1基因与pEGFP-N1载体的酶切回收片段经过T4连接酶连接后转化。AK1-pEGFP-N1载体进行双酶切鉴定后送至生工生物工程(上海)股份有限公司测序。
1.2.5 AK1基因生物信息学分析采用BioEdit软件对AK1基因的核苷酸序列进行比对,分析碱基组成、氨基酸数目及组成;相对分子质量和等电点运用在线网站expasy的protparam程序(
静原鸡胸肌、腿肌总RNA通过10 g/L的琼脂糖凝胶电泳检测,结果如图1所示,可清晰看到3个条带,无明显降解。核酸蛋白仪检测RNA的D260 nm/D280 nm在1.8~2.2之间,完整性较好(RIN≥6.5),可用于后续试验。
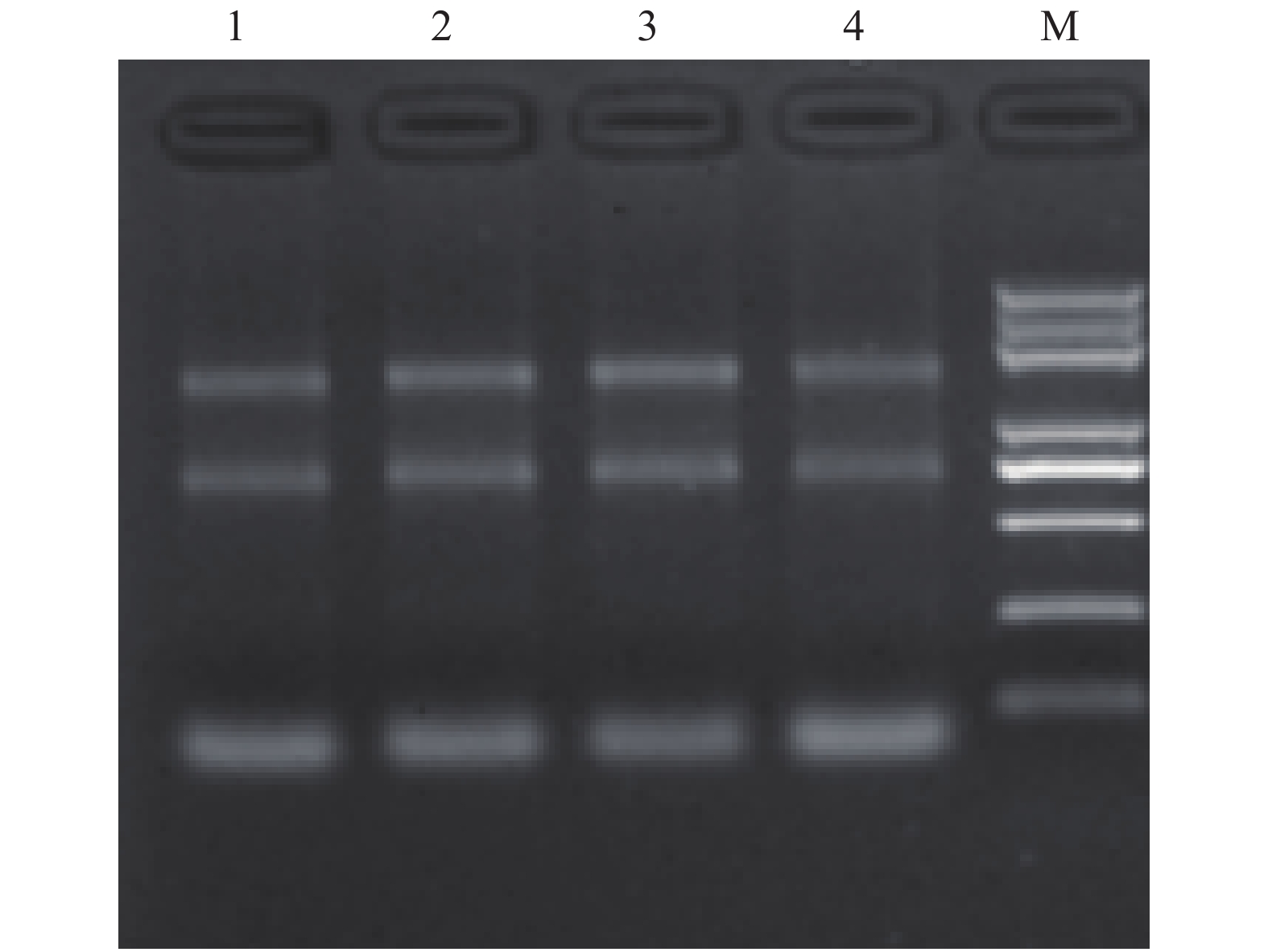
|
图 1 静原鸡不同组织总RNA提取 Fig. 1 Total RNA extraction from different tissues of Jingyuan chicken 1、2:胸肌;3、4:腿肌;M:Trans2K Plus DNA Marker 1, 2: Chest muscle; 3, 4: Leg muscle; M: Trans2K Plus DNA Marker |
PCR产物经10 g/L的琼脂糖凝胶电泳检测,经凝胶成像仪检测发现扩增片段条带整齐明亮且无引物二聚体等杂带,表明引物特异性较好,扩增条件合适。CDS区扩增产物条带长度大小约为741 bp,与预期目的片段长度大小相符(图2),可以进行回收纯化;回收后产物连接pMD18-T载体进行克隆,菌液PCR鉴定片段大小与预期目的片段一致。

|
图 2 静原鸡AK1基因PCR扩增电泳图 Fig. 2 Electrophoresis of PCR amplification of AK1 gene in Jingyuan chicken M:DL2000 DNA Marker;1~5:扩增片段 M: DL2000 DNA Marker; 1–5: Amplified fragments |
AK1基因CDS区加酶切位点扩增产物条带长度大小约为759 bp,与预期目的片段长度大小相符(图3),可以进行回收纯化及菌液扩增。
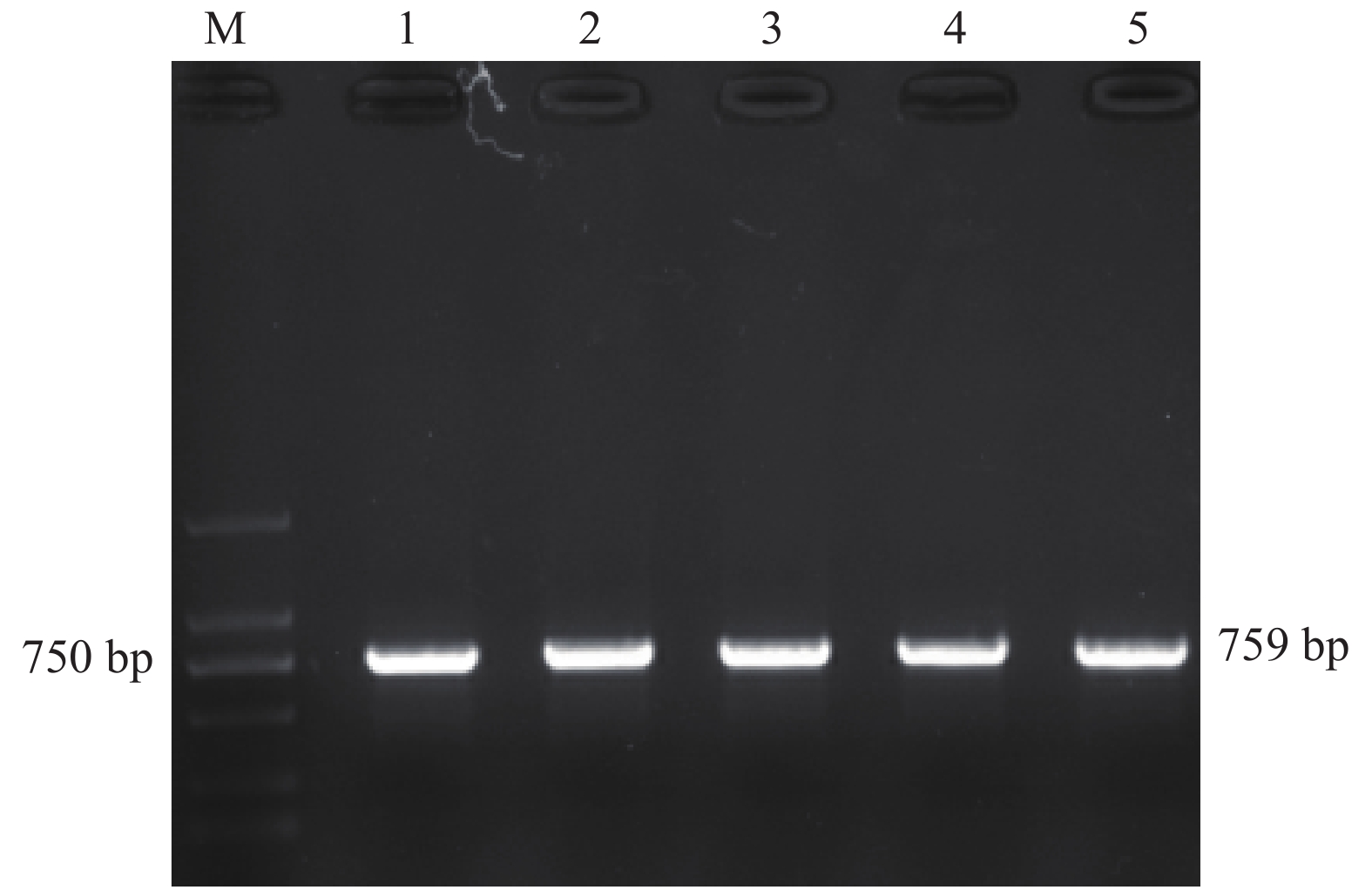
|
图 3 静原鸡AK1基因加酶切位点PCR扩增电泳图 Fig. 3 Electrophoresis of PCR amplification of AK1 gene with restriction site in Jingyuan chicken M:DL2000 DNA Marker;1~5:扩增片段 M: DL2000 DNA Marker; 1–5: Amplified fragments |
重组质粒AK1-pEGFP-N1经EcoRⅠ和BamHⅠ 37 ℃双酶切6 h后,经10 g/L的琼脂糖凝胶电泳检测得到4 033和759 bp的2个片段(图4),一个为质粒pEGFP-N1本身的片段,为4033 bp,一个为目的基因AK1的片段,约为759 bp,酶切结果说明AK1基因与pEGFP-N1载体正确重组。将菌液通过甘油保存后送至生工生物工程(上海)股份有限公司测序。
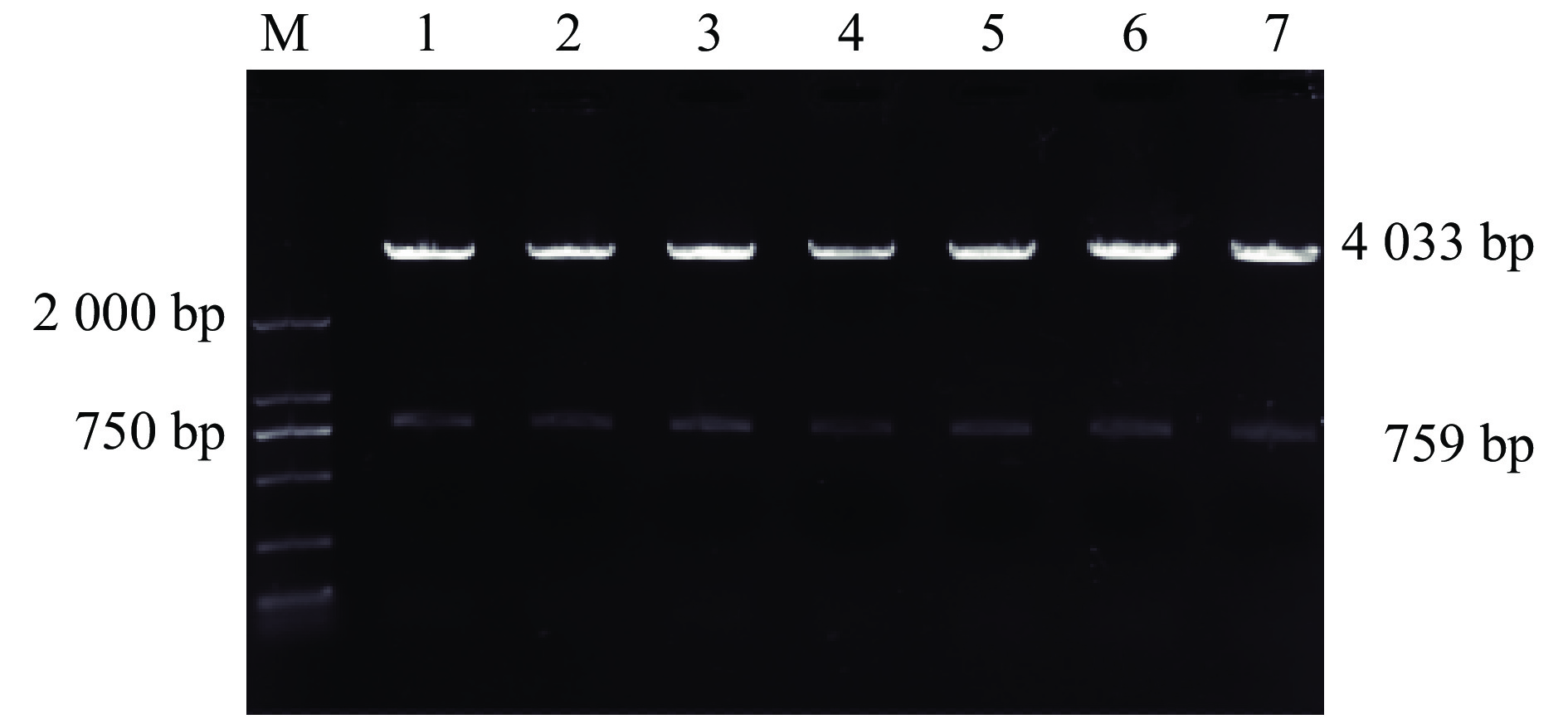
|
图 4 静原鸡AK1-pEGFP-N1载体酶切电泳图 Fig. 4 Restrictive enzyme digestion and electrophoresis of AK1-pEGFP-N1 vector in Jingyuan chicken M:DL2000 DNA Marker;1~7:扩增片段 M: DL2000 DNA Marker; 1–7: Amplified fragments |
测序后对静原鸡AK1基因序列进行校正、拼接,AK1基因CDS区全长585 bp,共编码194个氨基酸(图5)。核苷酸组成分析(图6)发现AK1基因CDS区鸟嘌呤(G)核苷酸数量占比最多(33.68%),胸腺嘧啶(T)核苷酸占比最少(16.41%),腺嘌呤(A)和胞嘧啶(C)数目相当,且G+C含量(60.00%)高于A+T含量(40.00%)。编码区DNA单链和双链相对分子质量分别为177991 和356652 。

|
图 5 AK1基因编码区全长序列与对应的氨基酸序列 Fig. 5 The full length coding sequence of AK1 gene and corresponding amino acid sequence |
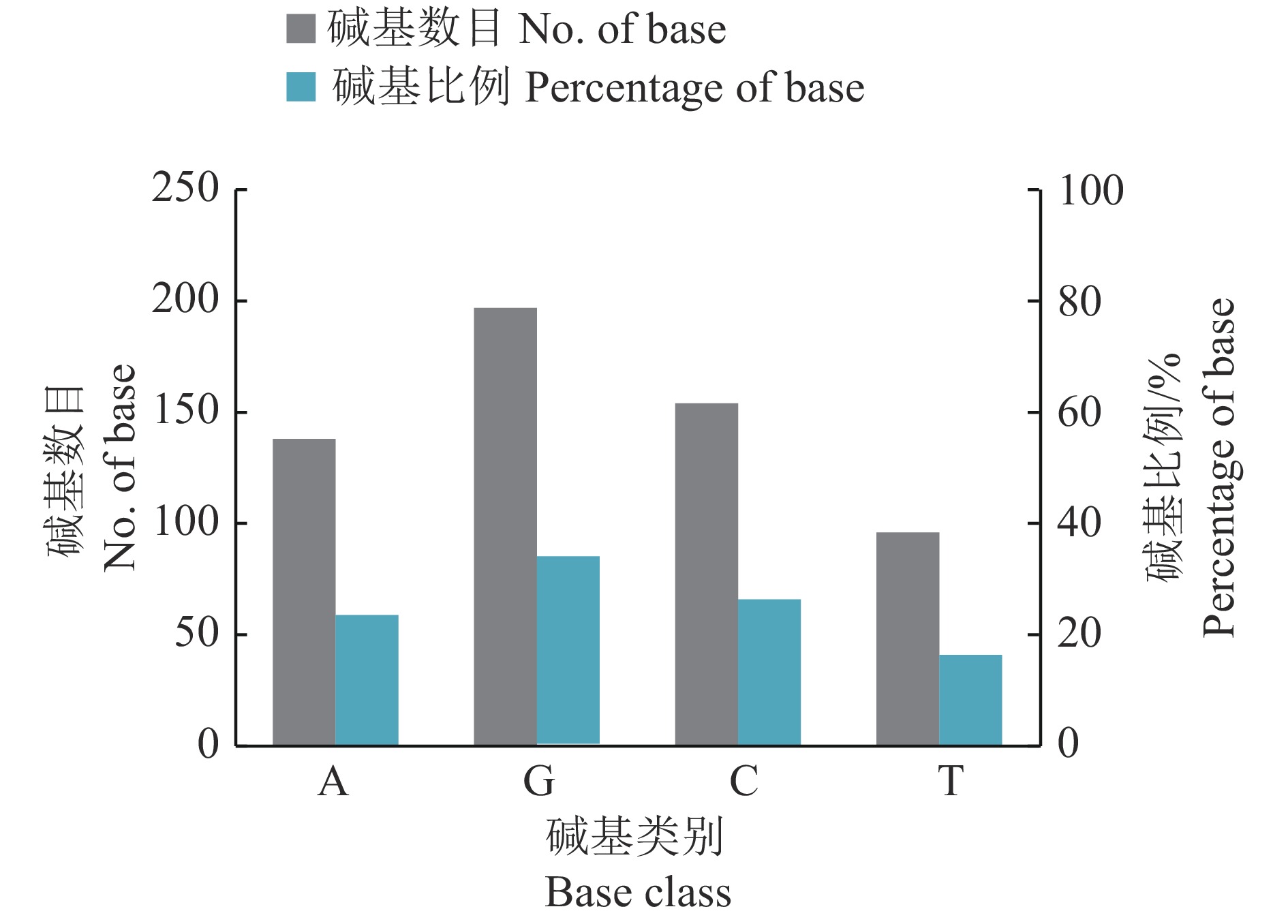
|
图 6 AK1基因CDS区核苷酸组成 Fig. 6 Nucleotide composition in CDS region of AK1 gene |
静原鸡AK1基因编码蛋白质的各种氨基酸中赖氨酸(Lys)数目占比最多(11.3%),天冬酰胺(Asn)和半胱氨酸(Cys)数目占比最少(1.0%)(表2)。氨基酸残基中正电荷残基总数(Arg+Lys)为32个,负电荷残基总数(Asp+Glu)为29个。理化性质分析结果显示,静原鸡AK1蛋白的原子组成为C962H1566N262O291S7,相对分子质量为21683,理论等电点为8.68,不稳定指数为21.56,脂肪指数为85.88。
|
|
表 2 AK1基因编码蛋白的氨基酸组成 Table 2 The composition of amino acid coded by AK1 gene |
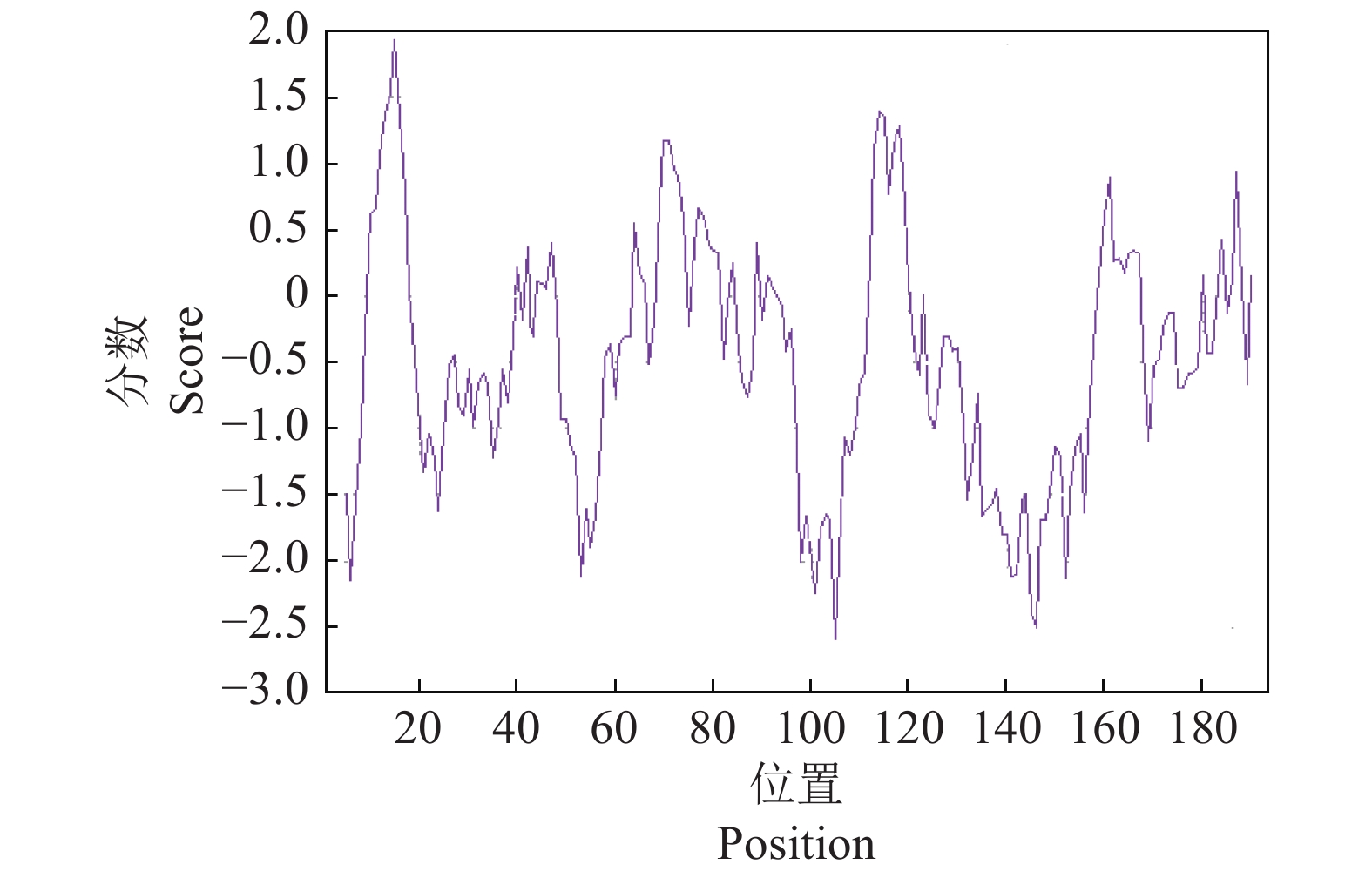
使用在线分析网站对静原鸡AK1基因编码蛋白对水分子的亲和力进行研究的结果(图7)表明,第15位缬氨酸(Val)疏水性最强(最高分数1.933),第105位谷氨酸(Glu)亲水性最强(最低分数−2.589),总体亲水性均值小于0(−0.469),说明该蛋白具有较强的亲水区域。
|
图 7 静原鸡AK1蛋白的疏水性/亲水性分析 Fig. 7 Hydrophobic/hydrophilic analysis for AK1 protein in Jingyuan chicken |
采用在线软件TMHMM-2.0的预测结果表明静原鸡AK1基因的编码蛋白不存在跨膜结构域,不是跨膜蛋白。CpG岛预测显示,AK1基因编码蛋白存在2个CpG岛。
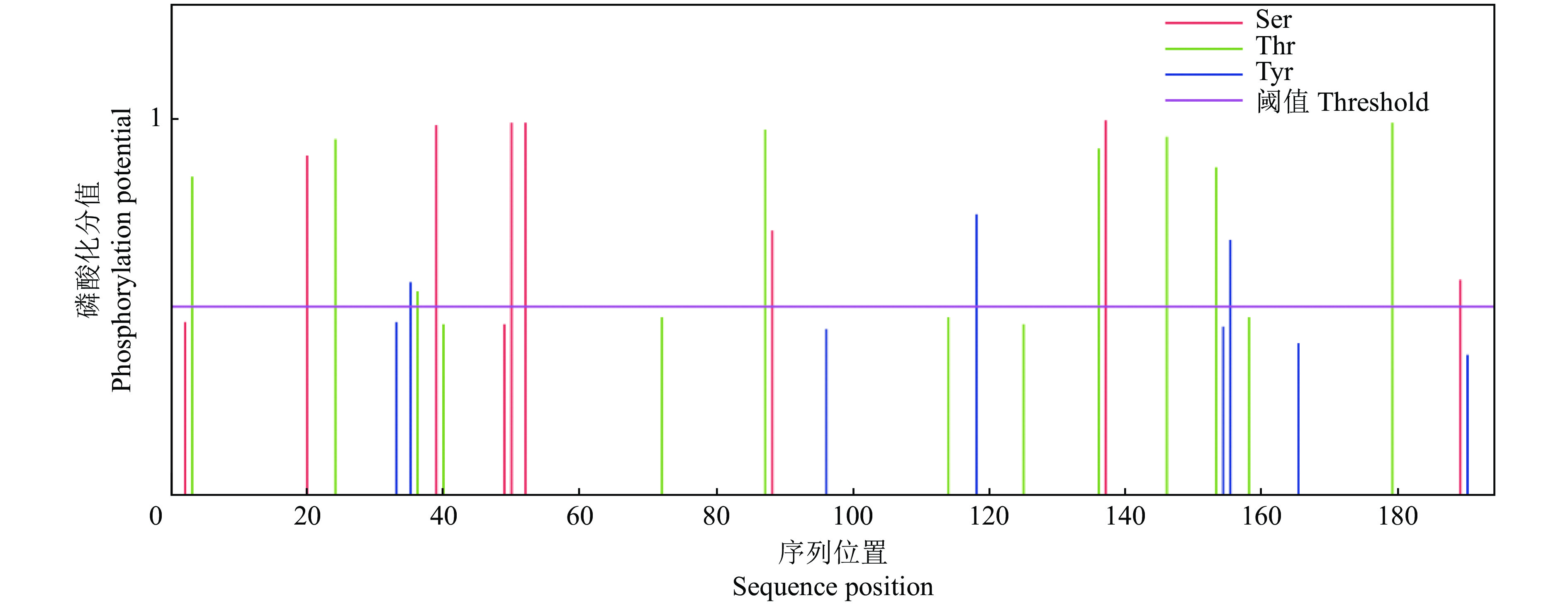
2.5.5 AK1基因编码蛋白的磷酸化位点静原鸡AK1蛋白可能存在7个丝氨酸(Ser)磷酸化位点,分别位于氨基酸序列上第20、39、50、52、88、137、189位,8个苏氨酸(Thr)磷酸化位点,分别位于第3、24、36、87、136、146、153、179位,3个酪氨酸(Tyr)磷酸化位点,分别位于第35、118、155位(图8)。
|
图 8 静原鸡AK1蛋白磷酸化位点 Fig. 8 The phosphorylation sites of AK1 protein in Jingyuan chicken |
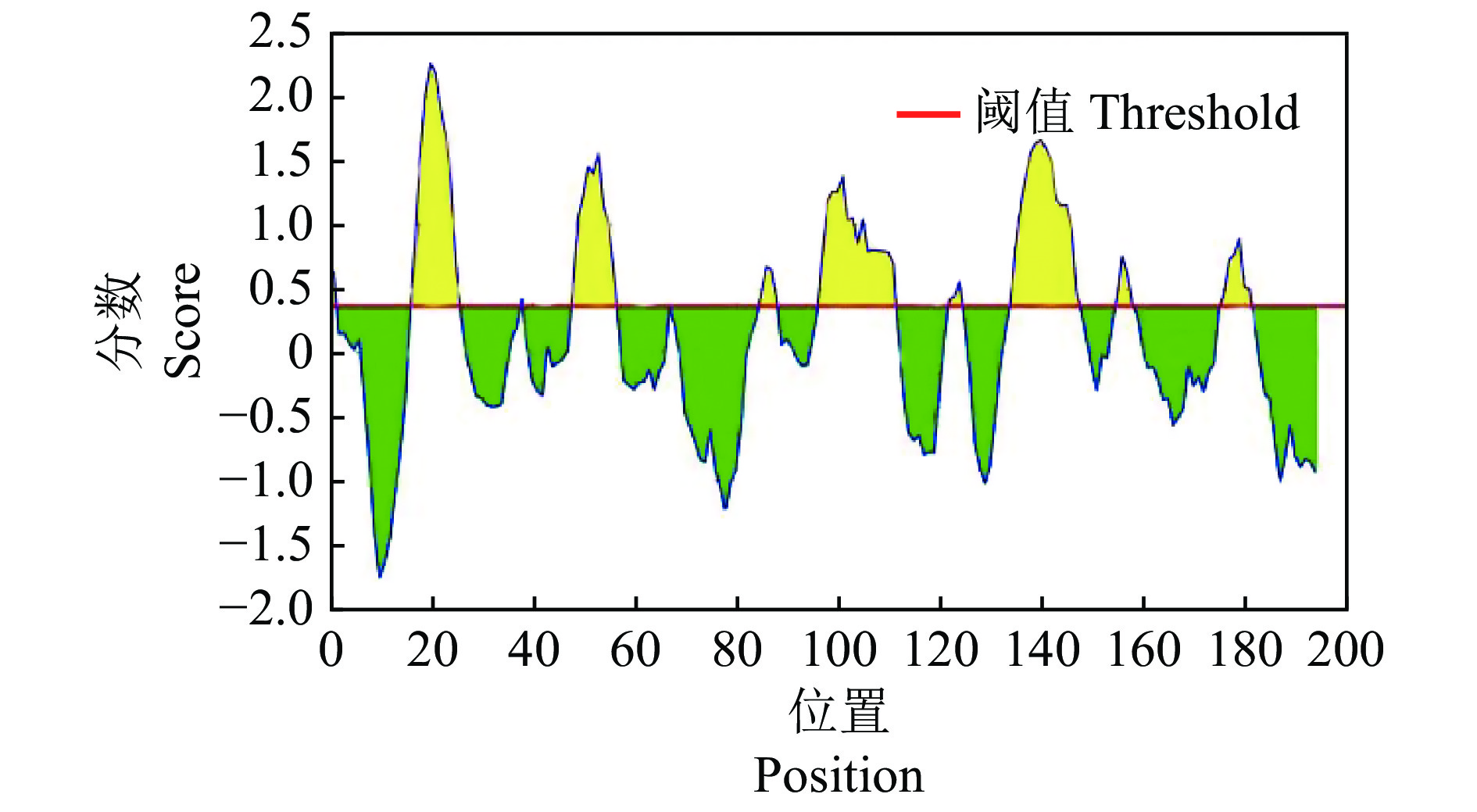
利用immuneepitope在线软件预测AK1基因编码蛋白的抗原表位(图9),结果发现静原鸡AK1蛋白存在10个B细胞抗原表位,分别位于1、17~25、38、48~56、85~88、97~111、122~124、134~147、155~158、176~181位氨基酸残基。
|
图 9 AK1蛋白B抗原表位预测 Fig. 9 Prediction of B epitope of AK1 protein |
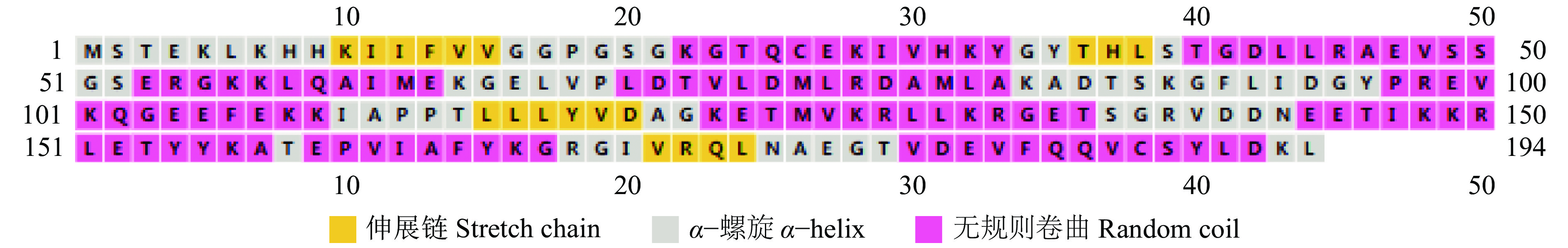
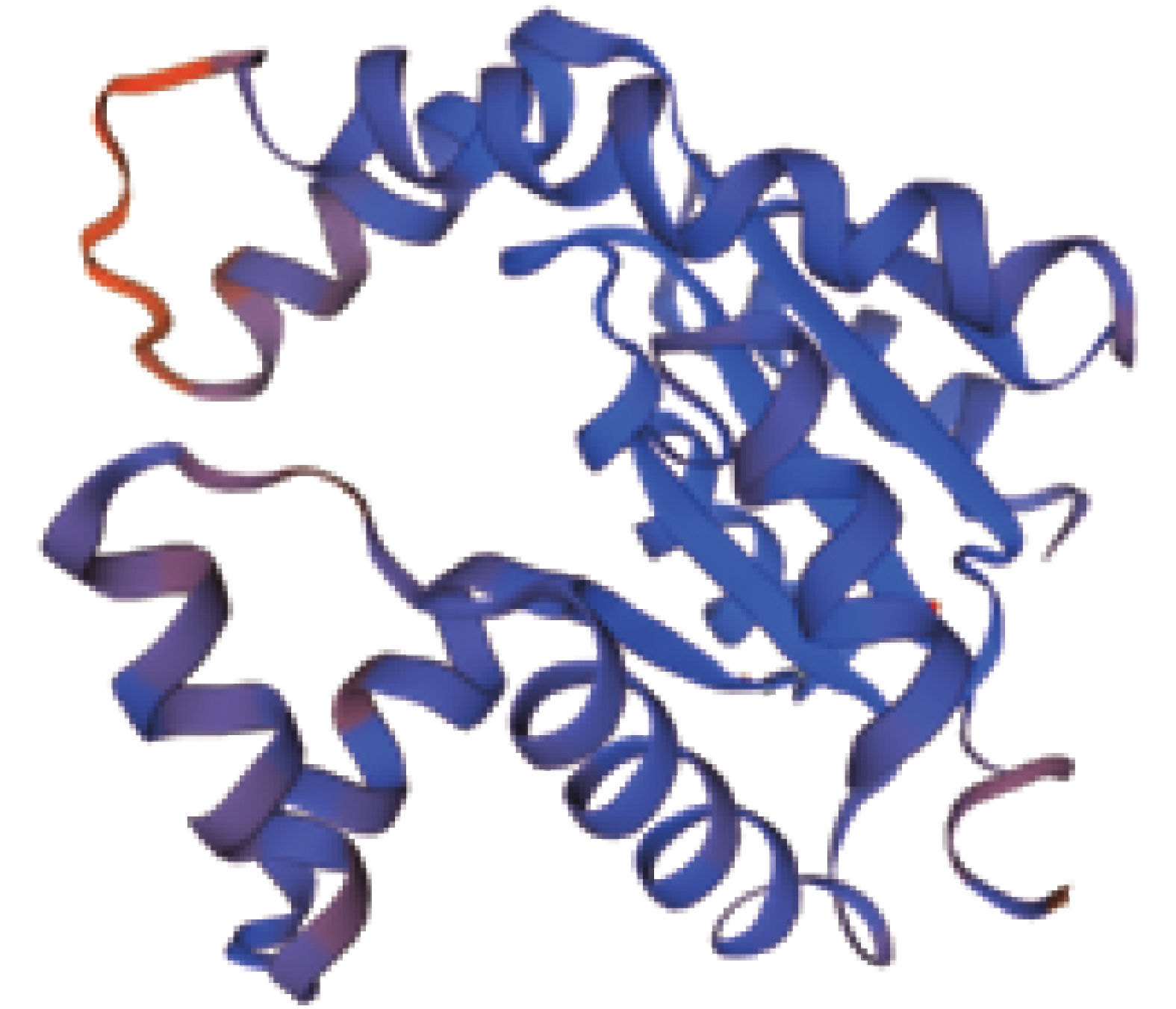
二级结构预测结果(图10)显示,静原鸡AK1蛋白含有8.76%的伸展链,46.91%的α–螺旋,44.33%的无规则卷曲。三级结构预测结果仍以α–螺旋和无规则卷曲为主(相似性为86.39%)(图11)。
|
图 10 静原鸡AK1蛋白质二级结构 Fig. 10 The secondary structure of AK1 protein in Jingyuan chicken |
|
图 11 静原鸡AK1蛋白质预测三级结构 Fig. 11 The predicted tertiary structure of AK1 protein in Jingyuan chicken |
通过string数据库对AK1基因进行共表达分析,发现在原鸡中AK1和AMPD1、PKM2存在共表达,共表达系数分别为0.116和0.063。PKM2与AMPD1共表达系数为0.067,AMPD1与AMPD3共表达系数为0.082。在其他有机体中AK1与AMPD3、AMPD1、NTPCR、PNPT1、CD39L1、PKM2、APRT、ADSL、ADK和TPK1均存在共表达。
2.5.9 AK1基因编码蛋白亚细胞定位通过在线工具psortⅡ预测AK1基因编码产物的亚细胞定位,其分布在细胞质的可能性为52.2%,分布在细胞骨架的可能性为17.4%,分布在细胞核中的可能性为13.0%,分布在线粒体、过氧化物酶体、内质网中的可能性分别为8.7%、4.3%、4.3%。由此推断,AK1基因编码产物主要在细胞质中发挥生物学作用。
2.5.10 AK1基因的GO富集分析通过string数据库对AK1基因进行GO富集分析,发现AK1基因参与4个分子功能GO条目,参与11个生物学过程GO条目,参与1个细胞组分GO条目(表3)。
|
|
表 3 AK1基因的GO注释分析 Table 3 GO annotation analysis of AK1 gene |
随着生命科学的发展,为揭示复杂的基因组信息结构及遗传语言的根本规律就出现了生物信息学,生物信息学为大数据“插上翅膀”,不仅给生命科学、农学、遗传学、细胞生物学和生物医学带来巨大的推动力且具有诱人的前景,它已经渗透到人类基因组研究的各个层面,如基因组、转录组学、蛋白质组学、代谢组学、疾病潜在靶点基因预测以及系统发育分析的研究[12-13]。
腺苷酸激酶(AK)普遍存在于生物体,催化腺嘌呤核苷酸的相互转化:Mg2++ATP+AMP=Mg2++2ADP,在不同哺乳动物组织中已经鉴定出6种1型AK同工酶(AK1)[14],它们的主要功能是维持细胞的能量稳态,处理与细胞能量利用相关的代谢信号,并为核酸合成提供核苷酸[15-16]。AK1是一种小型胞质酶,在骨骼肌、红细胞和脑等高周转率细胞中表达,其活性依赖于Mg2+或Mn2+离子,在没有AK1的情况下腺嘌呤核苷酸大量减少[17]。鸡AK1基因约为6000碱基对,由7个外显子组成,Suminami等[18]在鸡AK1和牛线粒体腺苷酸激酶(AK2)之间的点阵图发现,AK1基因可能是通过缺失1个或多个外显子从AK2基因进化而来的。有研究表明鸡AK1的一级结构与猪AK1的一级结构有85%的相似性,因此,提出猪AK1的二级和三级结构[19]也将适用于鸡AK1,而且发现AK1外显子4相对应的区域与AK2A构象的相似性最高,已知该区域有助于ATP结合和催化功能[20]。本研究发现静原鸡AK1基因CDS区共编码194个氨基酸,理论等电点为8.68(>7),不稳定指数为21.56(<40),脂肪指数为85.88,推断该蛋白是碱性稳定蛋白[21],蛋白的稳定性会直接影响生物的生命活动和细胞周期,因此,AK1蛋白具有稳定的细胞周期和生命活动。AK1蛋白总体亲水性均值为−0.469(<0),说明该蛋白是可溶性蛋白。信号肽和跨膜结构域预测发现,AK1蛋白不存在信号肽和跨膜结构,说明该蛋白不是一个膜蛋白,不能通过膜受体来发挥作用,对其进行纯化可能较为简单。磷酸化位点分析发现AK1蛋白存在8个苏氨酸(Thr)磷酸化位点、7个丝氨酸(Ser)磷酸化位点和3个酪氨酸(Tyr)磷酸化位点,这些位点可以调节一些细胞的代谢和信号转导,该蛋白可能需要通过翻译后的磷酸化和去磷酸化影响细胞生长、分化以及基因表达[22],这与Carrasco等[11]发现AK1磷酸化可能是在质膜线粒体和KATP通道之间传递信号所必需的的研究结果一致。蛋白二三级结构预测发现AK1蛋白以α–螺旋和无规则卷曲为主,且二级结构为混合模型[23],因此可能通过影响蛋白质肽链中配体和受体结合的活性[24],进而影响蛋白的功能。赵骁等[25]等研究发现如果β–转角和无规则卷曲在蛋白中占比居多,则会出现抗原表位较多的现象,因此,AK1蛋白抗原表位预测发现其具有10个B细胞抗原表位。基因共表达分析发现,在原鸡中AK1和AMPD1、PKM2存在共表达,而AMPD1和PKM2都是肌苷酸(Inosinc acid, IMP)从头合成途径的关键基因,因此AK1可能存在与AMPD1与PKM2相似的功能,可将AK1基因作为与IMP相关的功能基因进行研究。CpG岛常位于基因转录调控区附近,静原鸡AK1基因存在2个CpG岛,这为后期AK1基因转录区CpG岛甲基化状态的研究十分重要。亚细胞定位发现AK1蛋白位于细胞质中,与基因进行GO细胞组分分析和Choo等[26]研究结果一致,由此推断该蛋白主要在细胞质中发挥生物学作用。
综上,本研究通过生物信息分析对前期转录组筛选的静原鸡不同部位与IMP相关的关键差异基因AK1进行分析并通过分子生物学的方法构建其真核表达载体AK1-pEGFP-N1。
静原鸡AK1基因CDS区全长585 bp,AK1蛋白含有194个氨基酸,是具有较强的亲水区域的非跨膜蛋白,AK1蛋白可能存在7个丝氨酸(Ser)磷酸化位点,8个苏氨酸(Thr)磷酸化位点,3个酪氨酸(Tyr)磷酸化位点,并且具有10个B细胞抗原表位,2个CpG岛,预测其在细胞质中发挥作用,与AMPD1、PKM2、ADSL存在共表达,AK1蛋白二级结构和三级结构均以α–螺旋和无规则卷曲为主(相似性为86.39%)。
| [1] |
王建保. 朝那鸡列入区级畜禽遗传保护品种[J]. 固原日报, 2009(1): 9-25. (  0) 0) |
| [2] |
张娟, 母童, 赵平, 等. 静原鸡ELOVL5基因遗传多样性研究
[J]. 浙江农业学报, 2019, 31(2): 200-206. DOI:10.3969/j.issn.1004-1524.2019.02.04 (  0) 0) |
| [3] |
母童, 张娟, 赵平, 等. 静原鸡ELOVL2和ELOVL5基因表达的组织特异性研究
[J]. 浙江农业学报, 2017, 29(8): 1290-1296. DOI:10.3969/j.issn.1004-1524.2017.08.09 (  0) 0) |
| [4] |
JONES M E, LIPMANN F. Aceto-CoA-kinase: ATP + CoA + Ac ⇄Ac~S CoA + 5-AMP + PP[J]. Methods in Enzymology, 1955, 1: 585-591. DOI:10.1016/0076-6879(55)01101-4 (  0) 0) |
| [5] |
ZELEZNIKAR R J, HEYMAN R A, GRAEFF R M, et al. Evidence for compartmentalized adenylate kinase catalysis serving a high energy phosphoryl transfer function in rat skeletal muscle[J]. Journal of Biological Chemistry, 1990, 265: 300-311. DOI:10.1016/S0021-9258(19)40230-5 (  0) 0) |
| [6] |
VAN ROMPAY A R, JOHANSSON M, KARLSSON A. Phosphorylation of nucleosides and nucleoside analogs by mammalian nucleoside monophosphate kinases[J]. Pharmacolocy & Therapeutics, 2000, 87(2/3): 189-198. (  0) 0) |
| [7] |
TANABE T, YAMADA M, NOMA T, et al. Tissue- specific and developmentally regulated expression of the genes encoding adenylate kinase isozymes[J]. International Journal of Biochemistry & Cell Biology, 1993, 113(2): 200-207. (  0) 0) |
| [8] |
SCHULZ G E, ELZINGA M, MARX F, et al. Three-dimensional structure of adenylkinase[J]. Nature, 1974, 250(5462): 120-123. DOI:10.1038/250120a0 (  0) 0) |
| [9] |
SACHSENHEIMER W, SCHULZ G E. Two conformations of crystalline adenylatekinase[J]. Journal of Molecular Biology, 1977, 114(1): 23-36. DOI:10.1016/0022-2836(77)90280-7 (  0) 0) |
| [10] |
HANCOCK C R, JANSSEN E, TERJUNG R L. Skeletal muscle contractile performance and ADP accumulation in adenylate kinase-deficient mice[J]. American Journal of Physiology-Cell Physiology, 2005, 288(6): C1287-C1297. DOI:10.1152/ajpcell.00567.2004 (  0) 0) |
| [11] |
CARRASCO A J, DZEJA P P, ALEKSEEV A E, et al. Adenylate kinase phosphotransfer communicates cellular energetic signals to ATP-sensitive potassium channels[J]. Proceedings of the National Academy of Sciences of the United States of America, 2001, 98(13): 7623-7628. DOI:10.1073/pnas.121038198 (  0) 0) |
| [12] |
易继财. 生物类专业生物信息学课程教学探索: 华南农业大学生物类专业生物信息学课程的教改实践与思考[J]. 安徽农业科学, 2018, 46(26): 231-233. DOI:10.3969/j.issn.0517-6611.2018.26.071 (  0) 0) |
| [13] |
吴风瑞, 陈德宇, 姜双林, 等. PBL教学法在硕士研究生生物信息学教学中的应用[J]. 阜阳师范学院学报(自然科学版), 2017, 34(2): 109-111. (  0) 0) |
| [14] |
PANAYIOTOU C, SOLAROLI N, KARLSSON A. The many isoforms of human adenylate kinases[J]. International Journal of Biochemistry & Cell Biology, 2014, 49: 75-83. (  0) 0) |
| [15] |
JACOBASCH G. Biochemical and genetic basis of red cell enzyme deficiencies[J]. Best Practice & Research Clinical Haematology, 2000, 13(1): 1-20. (  0) 0) |
| [16] |
ABRUSCI P, CHIARELLI L R, GALIZZI A, et al. Erythrocyte adenylate kinase deficiency: Characterization of recombinant mutant forms and relationship with nonspherocytic hemolytic anemia[J]. Experimental Hematology, 2007, 35(8): 1182-1189. DOI:10.1016/j.exphem.2007.05.004 (  0) 0) |
| [17] |
PUCAR D, BAST P, GUMINA R J, et al. Adenylate kinase AK1 knockout heart: Energetics and functional performance under ischemia-reperfusion
[J]. American Journal of Physiology Heart and Circulatory Physiology, 2002, 283(2): H776-H782. DOI:10.1152/ajpheart.00116.2002 (  0) 0) |
| [18] |
SUMINAMI Y, KISHI F, TORIGOE T, et al. Structure and complete nucleotide sequence of the gene encoding chicken cytosolic adenylate kinase[J]. Journal of Biochemistry, 1988, 103(4): 611-617. DOI:10.1093/oxfordjournals.jbchem.a122315 (  0) 0) |
| [19] |
PAI E F, SACHSENHEIMER W, SCHIRMER R H, et al. Substrate positions and induced-fit in crystalline adenylate kinase[J]. Journal of Molecular Biology, 1977, 114(1): 37-45. DOI:10.1016/0022-2836(77)90281-9 (  0) 0) |
| [20] |
FRY D C, KUBY S A, MILDVAN A S. ATP-binding site of adenylate kinase: Mechanistic implications of its homology with ras-encoded p21, F1-ATPase, and other nucleotide-binding proteins[J]. Proceedings of the National Academy of Sciences of the United States of America, 1986, 83(4): 907-911. DOI:10.1073/pnas.83.4.907 (  0) 0) |
| [21] |
GURUPRASAD K, REDDY B V, PANDIT M W. Correlation between stability of a protein and its dipeptide composition: A novel approach for predicting in vivo stability of a protein from its primary sequence[J]. Protein Engineering, 1990, 4(2): 155-161. DOI:10.1093/protein/4.2.155 (  0) 0) |
| [22] |
ZOR T, MAYR B M, DYSON H J, et al. Roles of phosphorylation and helix propensity in the binding of the KIX domain of CREB-binding protein by constitutive (c-myb) and inducible (CREB) activators[J]. Journal of Biological Chemistry, 2002, 277(44): 42241-42248. DOI:10.1074/jbc.M207361200 (  0) 0) |
| [23] |
KYTE J, DOOLITTLE R F. A simple method for displaying the hydropathic character of a protein[J]. Journal of Molecular Biology, 1982, 157(1): 105-132. DOI:10.1016/0022-2836(82)90515-0 (  0) 0) |
| [24] |
郑海军, 朱荣, 葛春蕾, 等. 人白细胞介素−29的生物信息学分析[J]. 中国生物制品学杂志, 2013, 26(2): 209-212. (  0) 0) |
| [25] |
赵骁, 张峰波, 王红英, 等. 生物信息分析细粒棘球绦虫EgA31蛋白T细胞及B细胞的优势抗原表位[J]. 中国组织工程研究, 2019, 23(7): 1078-1083. DOI:10.3969/j.issn.2095-4344.1001 (  0) 0) |
| [26] |
CHOO H J, KIM B W, KWON O B, et al. Secretion of adenylate kinase 1 is required for extracellular ATP synthesis in C2C12 myotubes[J]. Experimental and Molecular Medicine, 2008, 40(2): 220-228. DOI:10.3858/emm.2008.40.2.220 (  0) 0) |
 2021, Vol. 42
2021, Vol. 42


